Účinné látky: Rupatadin
Pafinur 1 mg / ml perorální roztok
Příbalové informace Pafinur jsou k dispozici pro velikosti balení:- Pafinur 10 mg tablety
- Pafinur 1 mg / ml perorální roztok
Indikace Proč se používá Pafinur? K čemu to je?
Pafinur obsahuje léčivou látku rupatadin, což je antihistaminikum.
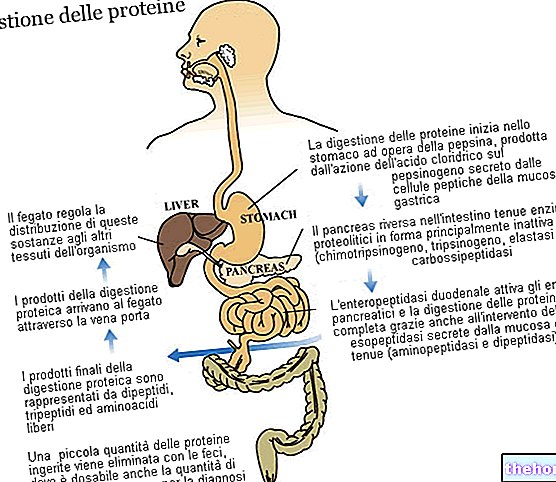
Pafinur perorální roztok zmírňuje příznaky alergické rýmy, jako je kýchání, rýma, ucpaný nos, svědění očí a nos u dětí ve věku 6 až 11 let.
Kontraindikace Kdy by Pafinur neměl být používán
Nepoužívejte Pafinur
- Jestliže jste alergický / á (přecitlivělý / á) na rupatadin nebo na kteroukoli další složku přípravku Pafinur.
Opatření pro použití Co potřebujete vědět před užitím Pafinuru
Pokud trpíte selháním ledvin nebo jater, požádejte o radu svého lékaře. Použití přípravku Pafinur se v současné době nedoporučuje u pacientů s poruchou funkce ledvin nebo jater.
Pokud máte nízké hladiny draslíku v krvi a / nebo máte určitý abnormální srdeční rytmus (známé prodloužení QTc intervalu na EKG), který se může objevit u některých forem srdečních chorob, požádejte o radu svého lékaře.
Tento léčivý přípravek není určen k použití u dětí mladších 6 let nebo vážících méně než 25 kg.
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Pafinur
Užívání Pafinuru s jinými léky
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte nebo jste v nedávné době užíval, a to i o lécích, které jsou dostupné bez lékařského předpisu.
Pokud užíváte Pafinur, neužívejte léky obsahující ketokonazol nebo erythromycin.
Pokud užíváte léky tlumící centrální nervový systém nebo statiny, poraďte se před užitím Pafinuru se svým lékařem.
Užívání Pafinuru s jídlem a pitím
Pafinur lze užívat s jídlem nebo bez jídla.
Pafinur by neměl být užíván v kombinaci s grapefruitovou šťávou, protože to může zvýšit hladinu Pafinuru v těle.
Pafinur v doporučené dávce (10 mg) nezvyšuje ospalost způsobenou alkoholem.
Varování Je důležité vědět, že:
Těhotenství a kojení
Neužívejte Pafinur během těhotenství a kojení, pokud to lékař výslovně neurčí.
Před použitím jakéhokoli léku se poraďte se svým lékařem nebo lékárníkem.
Řízení dopravních prostředků a obsluha strojů
Při doporučeném dávkování se neočekává žádný účinek přípravku Pafinur na schopnost řídit nebo obsluhovat stroje. Nicméně, když poprvé začnete užívat Pafinur, měli byste před řízením nebo obsluhou strojů sledovat, jak na vás léčba působí.
Důležité informace o některých pomocných látkách
Tento léčivý přípravek obsahuje sacharózu a může mít škodlivý účinek na zuby. Pokud vám lékař řekl, že nesnášíte některé cukry, kontaktujte svého lékaře před užitím tohoto léku.
Tento léčivý přípravek obsahuje methylparahydroxybenzoát, který může způsobit alergické reakce (včetně opožděných).
Dávka, způsob a doba podání Jak používat Pafinur: Dávkování
Vždy používejte Pafinur přesně podle pokynů svého lékaře. V případě pochybností se poraďte se svým lékařem nebo lékárníkem.
Pafinur perorální roztok je k perorálnímu podání.
Dávkování u dětí s hmotností 25 kg a více: 5 ml (5 mg rupatadinu) perorálního roztoku jednou denně, s jídlem nebo bez jídla.
Váš lékař vás bude informovat o délce léčby přípravkem Pafinur.
Návod k použití:
- Lahev otevřete stisknutím uzávěru a otočením proti směru hodinových ručiček.
- Vezměte injekční stříkačku, vložte ji do propíchnutelného víčka a lahvičku otočte dnem vzhůru.
- Naplňte injekční stříkačku předepsanou dávkou.
- Podávejte přímo z dávkovací stříkačky.
- Po použití stříkačku umyjte.
Předávkování Co dělat, pokud jste užili příliš mnoho přípravku Pafinur
Jestliže jste použil (a) více přípravku Pafinur, než jste měl (a)
Pokud jste omylem užili vysokou dávku léku, okamžitě to sdělte svému lékaři nebo lékárníkovi.
Jestliže jste zapomněl (a) použít Pafinur
Nezdvojnásobujte následující dávku, abyste nahradil (a) vynechanou dávku.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Pafinur
Podobně jako všechny léky, může mít i Pafinur nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Časté nežádoucí účinky (mohou postihnout až 1 z 10 uživatelů) jsou ospalost, bolest hlavy a infekce horních cest dýchacích. Méně časté nežádoucí účinky (mohou postihnout až 1 ze 100 uživatelů) jsou závratě, chřipka a ekzém.
Kromě výše uvedených nežádoucích účinků byly při podávání 10 mg tablet rupatadinu dospělým a mladistvým (nad 12 let) hlášeny následující nežádoucí účinky:
- Časté nežádoucí účinky (mohou postihnout až 1 z 10 uživatelů) jsou závratě, sucho v ústech, pocit slabosti a únava.
- Méně časté nežádoucí účinky (mohou postihnout až 1 ze 100 uživatelů) jsou zvýšená chuť k jídlu, podrážděnost, potíže se soustředěním, krvácení z nosu, sucho v nose, bolest v krku, kašel, sucho v krku, rýma, pocit malátnosti, bolesti žaludku, průjem, poruchy trávení, zvracení , zácpa, vyrážka, bolest zad, kloubů, svalů, žízeň, celková malátnost, horečka, změny hodnot krevních testů indikující funkci jater a přibývání na váze.
- Vzácné nežádoucí účinky (mohou postihnout až 1 z 1000 uživatelů) jsou bušení srdce a zrychlení srdeční frekvence.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Expirace a retence
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Uchovávejte Pafinur mimo dosah a dohled dětí.
Nepoužívejte Pafinur po uplynutí doby použitelnosti, uvedené na lahvičce a krabičce za EXP. Datum exspirace se vztahuje k poslednímu dni v měsíci Platnost po prvním otevření je stejná jako datum exspirace na krabičce a na lahvi.
Léčivé přípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Složení a léková forma
Co Pafinur obsahuje
- Léčivou látkou je rupatadin. Jeden ml obsahuje 1 mg rupatadinu (jako fumarát).
- Dalšími složkami jsou propylenglykol, bezvodá kyselina citrónová, bezvodý fosforečnan sodný, sacharin sodný, sacharóza, methylparahydroxybenzoát (E-218), chinolinová žluť (E-104), banánová příchuť, čištěná voda.
Jak vypadá Pafinur a obsah balení
Pafinur je čirý žlutý perorální roztok. Pafinur je balen v plastové lahvičce z jantaru s propíchnutelným víčkem a dětským bezpečnostním uzávěrem. Součástí balení je 5 ml stříkačka pro perorální podání s odstupňováním 0,25 ml.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Chcete-li mít přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
PAFINUR 1 MG / ML Orální roztok
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jeden ml perorálního roztoku obsahuje:
1 mg rupatadinu (jako fumarát)
Pomocné látky:
sacharóza 300 mg / ml;
methylparahydroxybenzoát (E218) 1,00 mg / ml.
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Perorální roztok.
Průhledný roztok žluté barvy.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Pafinur 1 mg / ml perorální roztok je indikován k symptomatické léčbě alergické rýmy (včetně perzistentní alergické rýmy) u dětí ve věku 6 až 11 let (viz bod 5.1).
04.2 Dávkování a způsob podání
Děti ve věku od 6 do 11 let.
Dávkování u dětí s hmotností 25 kg a více: 5 ml (5 mg rupatadinu) perorálního roztoku jednou denně, s jídlem nebo bez jídla.
Bezpečnost a účinnost rupatadinu u dětí ve věku 2 až 5 let a tělesné hmotnosti nižší než 25 kg nebyla dosud stanovena (viz také bod 4.4).
Podávání přípravku dětem mladším než 2 roky se nedoporučuje z důvodu nedostatku údajů v této populaci (viz bod 4.4).
U dospělých a dospívajících (starších 12 let) je vhodnější podání rupatadinu 10 mg tablety.
Pacienti s poruchou funkce ledvin nebo jater: Protože nejsou žádné klinické zkušenosti u pacientů s poruchou funkce ledvin nebo jater, použití rupatadinu u těchto pacientů se v současné době nedoporučuje.
Návod k použití:
- Lahev otevřete stisknutím uzávěru a otočením proti směru hodinových ručiček.
- Vezměte injekční stříkačku, vložte ji do propíchnutelného víčka a lahvičku otočte dnem vzhůru.
- Naplňte injekční stříkačku předepsanou dávkou.
- Podávejte přímo z dávkovací stříkačky.
- Po použití stříkačku umyjte.
04.3 Kontraindikace
Přecitlivělost na rupatadin nebo na kteroukoli pomocnou látku.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Účinnost a bezpečnost perorálního roztoku rupatadinu u dětí mladších 6 let nebyla dosud stanovena.
Podávání rupatadinu s grapefruitovou šťávou se nedoporučuje (viz bod 4.5).
Srdeční bezpečnost 10 mg tablet rupatadinu byla hodnocena u dospělých v důkladné studii QT / QTc.
Rupatadin až v desetinásobku terapeutické dávky neměl žádný účinek na EKG, a proto nevyvolával žádné obavy o bezpečnost srdce.
Rupatadin by však měl být používán s opatrností u pacientů se známým prodloužením QT intervalu, u pacientů s nekorigovanou hypokalémií, u pacientů s probíhajícími proarytmickými stavy, jako je klinicky významná bradykardie, akutní ischémie myokardu.
Zvýšení hladiny kreatinfosfokinázy v krvi, alaninaminotransferázy a aspartátaminotransferázy a abnormality testů jaterních funkcí jsou méně časté nežádoucí účinky hlášené u 10mg tablet rupatadinu u dospělých.
Tento léčivý přípravek obsahuje sacharózu a může mít škodlivý účinek na zuby. Pacienti se vzácnými dědičnými problémy s intolerancí fruktózy, malabsorpcí glukózy / galaktózy nebo nedostatkem sacharázy a izomaltázy by tento léčivý přípravek neměli užívat.
Tento léčivý přípravek obsahuje methylparahydroxybenzoát, který může způsobit alergické reakce (včetně opožděných).
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Nebyly provedeny žádné interakční studie u dětí s perorálním roztokem rupatadinu.
Studie interakcí byly provedeny pouze u dospělých a dospívajících (starších 12 let) s 10 mg tabletami rupatadinu.
Interakce s ketokonazolem nebo erythromycinem: Souběžné podávání 20 mg rupatadinu a ketokonazolu nebo erythromycinu zvyšuje systémovou expozici rupatadinu 10krát, respektive 2-3krát. Tyto změny nebyly spojeny s účinkem na QT interval nebo se zvýšením nežádoucích účinků ve srovnání do doby, kdy byly léky podávány samostatně.
Rupatadin by však neměl být používán v kombinaci s těmito léky a jinými inhibitory izoenzymu CYP3A4.
Interakce s grapefruitovým džusem: Souběžné podávání grapefruitové šťávy zvýšilo systémovou expozici 10 mg tablet rupatadinu 3,5krát. Důvodem je, že grapefruit obsahuje jednu nebo více sloučenin, které inhibují CYP3A4 a které mohou zvýšit plazmatické koncentrace léčiv metabolizovaných prostřednictvím CYP3A4, jako je rupatadin. Grapefruit má také bylo navrženo, aby ovlivňovalo transportní systémy léčiv ve střevě, jako je P-glykoprotein. Grapefruitovou šťávu byste neměli užívat současně.
Interakce s alkoholem: Po podání alkoholu měla dávka 10 mg rupatadinu v některých psychomotorických testech okrajové účinky, přestože se tyto účinky významně nelišily od účinků způsobených samotnou konzumací alkoholu. Dávka 20 mg zvyšuje poškození způsobené příjmem alkoholu.
Interakce s látkami tlumícími CNS: jako u jiných antihistaminik nelze vyloučit interakce s depresivními látkami na centrální nervový systém.
Interakce se statiny: V klinických studiích s rupatadinem nebylo běžně hlášeno asymptomatické zvýšení CPK. Riziko interakcí se statiny, z nichž některé jsou také metabolizovány cytochromem P450 (CYP3A4), není známo. Z tohoto důvodu by měl být rupatadin podáván opatrně, pokud je podáván současně se statiny.
04.6 Těhotenství a kojení
Těhotenství
Údaje o omezeném počtu exponovaných těhotenství nenaznačují žádné nežádoucí účinky rupatadinu na těhotenství nebo na zdraví plodu / novorozence. Zatím nejsou k dispozici žádné další relevantní epidemiologické údaje. Studie na zvířatech nenaznačují přímé ani nepřímé škodlivé účinky na těhotenství, embryonální / fetální vývoj, porod nebo postnatální vývoj (viz bod 5.3). Jako preventivní opatření je vhodnější vyhnout se užívání rupatadinu během těhotenství.
Čas krmení
Rupatadin se vylučuje do mléka zvířat. Není známo, zda se rupatadin vylučuje do lidského mléka. S přihlédnutím k výhodám kojení pro dítě a výhodám léčby rupatadinem pro ženu je třeba rozhodnout, zda přerušit kojení nebo přerušit / zdržet se léčby rupatadinem.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Nebylo prokázáno, že by 10 mg rupatadinu narušovalo schopnost řídit nebo obsluhovat stroje. Před řízením nebo obsluhou strojů je však třeba opatrnosti, dokud se u pacienta nevytvoří subjektivní reakce na rupatadin.
04.8 Nežádoucí účinky
Klinických studií s perorálním roztokem rupatadinu u dětí ve věku 6 až 11 let se zúčastnilo 371 pacientů. Mezi nimi bylo 51 pacientů léčeno 2,5 mg rupatadinu, 140 pacientů bylo léčeno 5 mg rupatadinu a 180 pacientů dostávalo placebo.
Frekvence nežádoucích účinků jsou přičítány následovně:
- Časté (≥ 1/100 a
- Méně časté (≥ 1/1 000 a
- Vzácné (≥ 1/10 000 let
Frekvence nežádoucích účinků hlášených u pacientů léčených rupatadinem během klinických studií byly následující:
• Infekce a infestace
- Běžný: infekce horních cest dýchacích
- Méně časté: vliv
• Poruchy nervového systému:
- Běžný: bolest hlavy, ospalost
- Méně časté: závrať
• Poruchy kůže a podkožní tkáně
- Méně časté: ekzém
Během klinických studií byl rupatadin 10 mg tablety podáván více než 2025 dospělým a dospívajícím pacientům, z nichž 120 dostávalo rupatadin po dobu nejméně 1 roku.
Frekvence nežádoucích účinků hlášených u pacientů léčených rupatadinem 10 mg tablety během klinických studií byla následující:
• Infekce a infestace
- Méně časté: faryngitida, rýma
• Poruchy metabolismu a výživy
- Méně časté: zvýšená chuť k jídlu
• Poruchy nervového systému:
- Běžný: ospalost, bolest hlavy, závratě
- Méně časté: porucha pozornosti
• Srdeční poruchy
Vzácný: tachykardie a palpitace *
• Respirační, hrudní a mediastinální poruchy
- Méně časté: epistaxe, suchost nosu, kašel, sucho v krku, orofaryngeální bolest
• Gastrointestinální poruchy
- Běžný: suchá ústa
- Méně časté: nevolnost, bolest v nadbřišku, průjem, dyspepsie, zvracení, bolest břicha, zácpa
• Poruchy kůže a podkožní tkáně
- Méně časté: vyrážka
• Poruchy svalové a kosterní soustavy, pojivové tkáně a kostí
- Méně časté: bolest zad, artralgie, myalgie
• Celkové poruchy a reakce v místě aplikace
- Běžný: únava, astenie
- Méně časté: žízeň, pocit nevolnosti, horečka, podrážděnost
• Diagnostické testy
- Méně časté: zvýšená hladina kreatinfosfokinázy v krvi, alaninaminotransferáza, aspartátaminotransferáza, abnormální funkce jater, zvýšení tělesné hmotnosti
* v postmarketingových zkušenostech s rupatadinem 10 mg tablety byla hlášena tachykardie a palpitace.
04.9 Předávkování
U dospělých a dětí nebyly hlášeny žádné případy předávkování. Ve studii klinické bezpečnosti u dospělých byl rupatadin v denní dávce 100 mg po dobu 6 dnů dobře snášen. Nejčastější nežádoucí reakcí byla somnolence. Pokud „dojde k náhodnému požití velmi vysokých dávek, měla by být zahájena symptomatická léčba spojená s nezbytnými podpůrnými opatřeními“.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: jiná antihistaminika pro systémové použití.
ATC kód: R06A X28.
Rupatadin je antihistaminikum druhé generace, dlouhodobě působící antagonista histaminu se selektivní antagonistickou aktivitou na periferním H1 receptoru. Některé z metabolitů (desloratadin a jeho hydroxylované metabolity) si zachovávají antihistaminovou aktivitu a mohou částečně přispět k celkové účinnosti léčiva.
Studie in vitro prováděné s rupatadinem ve vysokých koncentracích prokázaly inhibici degranulace žírných buněk indukovanou imunologickými a neimunologickými podněty a inhibici uvolňování cytokinů, zejména TNFa, v lidských žírných buňkách a monocytech. Klinický význam těchto pozorování je ještě třeba potvrdit.
Perorální roztok rupatadinu měl podobný farmakokinetický profil u dětí ve věku 6 až 11 let ve srovnání s dospělými (> 12 let): po 4 týdnech léčby byl také pozorován farmakodynamický účinek (potlačení oblasti s pupínky, antihistaminový účinek) . Randomizovaná, dvojitě zaslepená, placebem kontrolovaná, potvrzující studie u dětí s perzistentní alergickou rýmou ve věku 6 až 11 let prokázala, že perorální roztok rupatadinu má lepší profil při snižování nosních příznaků (rýma a svědění nosu, úst, hrdla a / nebo uši) ve srovnání s placebem u dětí s přetrvávající alergickou rýmou po 4 a 6 týdnech léčby. Kromě toho bylo během studie ve srovnání s placebem pozorováno také významné zlepšení kvality života.
Klinické studie u dobrovolníků (n = 375) a pacientů (n = 2650) s alergickou rýmou a chronickou idiopatickou kopřivkou neprokázaly žádný významný účinek na elektrokardiogram, když byly tablety rupatadinu podávány v dávkách mezi 2 a 100 mg.
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s perorálním roztokem Pafinur ve všech podskupinách pediatrické populace s alergickou rýmou a chronickou kopřivkou (viz bod 4.2).
05.2 Farmakokinetické vlastnosti
Pediatrická populace
V podskupině dětí (průměrný věk: 10 let) byl rupatadin rychle absorbován po podání průměrné dávky 5 mg rupatadinu s průměrným T 0,5 hodiny po podání. Průměrná C byla 0,5 hodiny po podání. 2,5 ng / ml po jednorázové perorální dávce Pokud jde o expozici, průměrná celková plocha pod křivkou (AUC) byla 8,86 ng • h / ml. Všechny tyto hodnoty jsou podobné hodnotám získaným u dospělých a dospívajících.
Průměrný eliminační poločas rupatadinu u dětí byl 3,12 hodiny, kratší než ten, který byl hlášen u tablet u dospělých a dospívajících.
Účinky příjmu potravy
S perorálním roztokem rupatadinu nebyly provedeny žádné studie interakcí s jídlem. Vliv jídla byl ovlivněn u dospělých a mladistvých tabletami rupatadinu 10 mg. Příjem potravy zvýšil systémovou expozici (AUC) rupatadinu přibližně o 23%. Maximální plazmatická koncentrace (Cmax) nebyla příjemem potravy ovlivněna. Tyto rozdíly nemají žádný klinický význam.
Metabolismus a eliminace
Ve studii exkrece dospělých bylo 34,6% podaného rupatadinu nalezeno v moči a 60,9% ve stolici odebrané během 7 dnů. Při perorálním podání rupatadin podléhá významnému presystémovému metabolismu. Množství nezměněné účinné látky nalezené v moči a stolici bylo zanedbatelné. To znamená, že rupatadin je téměř úplně metabolizován. Studie in vitro na metabolismu v lidských jaterních mikrozomech ukazují, že rupatadin je primárně metabolizován cytochromem P450 (CYP 3A4).
05.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické studie na základě konvenčních studií farmakologické bezpečnosti, toxicity po opakovaném podávání, genotoxicity a karcinogenního potenciálu neodhalily žádné zvláštní riziko pro člověka.
Dávka vyšší než 100násobek klinicky doporučené dávky (10 mg) rupatadinu neprodloužila interval QTc nebo QRS ani nezpůsobila arytmii u různých druhů zvířat, jako jsou krysy, morčata a psi. Rupatadin je jedním z jeho hlavních aktivních metabolitů. u lidských subjektů 3-hydroxydesloratadin neovlivnil potenciál srdečního účinku v izolovaných psích Purkinje vláknech v koncentracích nejméně 2000krát vyšších, než je Cmax dosažená po podání dávky 10 mg u lidských subjektů. Ve studii hodnotící účinek na klonovaný lidský HERG kanál rupatadin inhiboval kanál v koncentraci 1685násobku Cmax dosaženého po podání 10 mg rupatadinu. Studie tkáňové distribuce u potkanů provedené s radioaktivně značeným rupatadinem prokázaly, že rupatadin se nehromadí v srdci tkáň.
Studie fertility na potkanech prokázaly významné snížení plodnosti samců a samic při dávce 120 mg / kg / den, což vedlo k Cmax rupatadinu 268krát vyšší, než je hodnota dosažená po podání terapeutické dávky u lidí (10 mg / den) . Fetální toxicita (vývojové zpoždění, neúplná osifikace, drobné změny skeletu) byla u potkanů detekována pouze při toxických dávkách pro matku (25 a 120 mg / kg / den).
U králíků nebyla u dávek do 100 mg / kg prokázána žádná vývojová toxicita.
Úrovně dávek, při kterých nebyly pozorovány žádné vývojové nežádoucí účinky (NOAEL), byly identifikovány při dávce 5 mg / kg / den u potkanů a 100 mg / kg / den u králíků, což vedlo k 45násobnému a 116násobně vyššímu Cmax, než je naměřeno u mužů v terapeutických dávkách (10 mg / den).
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Propylenglykol
Bezvodá kyselina citronová
Fosforečnan sodný bezvodý
Sacharin sodný
Sacharóza
Methylparahydroxybenzoát (E218)
Chinolinová žluť (E104)
Banánová příchuť (Směs aromatických látek, aromatických přípravků a přírodních aromatických látek a propylenglykolu)
Čištěná voda
06.2 Neslučitelnost
Irelevantní.
06.3 Doba platnosti
30 měsíců.
Platnost po prvním otevření je stejná jako datum spotřeby na krabičce a na lahvi.
06.4 Zvláštní opatření pro skladování
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
06.5 Charakter vnitřního obalu a obsah balení
120 ml jantarová polyetyléntereftalátová (PET) lahvička s propíchnutelným víčkem z polyetylenu s nízkou hustotou (LDPE) uzavřená žlutým bezpečnostním uzávěrem z polyetylenu s vysokou hustotou (HDPE) v papírové krabičce také obsahující injekční stříkačku pro perorální podání 5 ml (polypropylen, polyetylen ) odměrný po 0,25 ml.
06.6 Návod k použití a zacházení
Žádné zvláštní pokyny.
Nepoužitý léčivý přípravek a odpad z tohoto přípravku musí být zlikvidován v souladu s místními předpisy.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Biohorm, S.A.
Avinguda Camí-Reial, 51-57
08184 Palau-solità i Plegamans (Španělsko)
Prodejce na prodej
Rottapharm S.p.A.
Unie galerie, 5
20122 Milán
08.0 REGISTRAČNÍ ČÍSLO
AIC č. 037888094 „1 mg / ml perorální roztok“ 1 lahvička v PET o objemu 120 ml s odstupňovanou stříkačkou a dětským bezpečnostním uzávěrem
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Datum první registrace: 6. března 2014