Účinné látky: inzulín (inzulín lispro)
Humalog Mix50 100 U / ml KwikPen injekční suspenze
Příbalové informace Humalog jsou k dispozici pro velikosti balení:- Humalog 100 U / ml injekční roztok v zásobní vložce
- Humalog Mix25 100 U / ml injekční suspenze v injekční lahvičce
- Humalog Mix25 100 U / ml injekční suspenze v zásobní vložce
- Humalog Mix50 100 U / ml injekční suspenze v zásobní vložce
- Humalog BASAL 100 U / ml injekční suspenze v zásobní vložce
- Humalog 100 U / ml KwikPen injekční roztok
- Humalog Mix25 100 U / ml KwikPen injekční suspenze
- Humalog Mix50 100 U / ml KwikPen injekční suspenze
- Humalog BASAL 100 U / ml KwikPen injekční suspenze
Proč je Humalog používán? K čemu to je?
Humalog Mix50 KwikPen se používá k léčbě diabetu. Jedná se o předmíchané zavěšení. Účinnou látkou v něm je inzulín lispro. 50% inzulínu lispro obsaženého v přípravku Humalog Mix50 KwikPen se rozpustí ve vodě a díky malé modifikaci molekuly inzulínu působí rychleji než normální lidský inzulín. 50% inzulínu lispro obsaženého v Humalog Mix50 KwikPen je přítomen v suspenzi společně s protamin sulfátem, takže jeho působení je prodlouženo.
Jeho nemoc, cukrovka, vyplývá ze skutečnosti, že jeho slinivka břišní neprodukuje dostatek inzulinu, který by kontroloval hladinu glukózy v krvi. Humalog Mix50 nahrazuje inzulín, který si vaše tělo vyrábí a používá se k dlouhodobé kontrole glukózy. Humalog Mix50 působí velmi rychle a déle než rozpustný inzulín. Humalog Mix50 byste si měli obvykle aplikovat do 15 minut před jídlem.
Váš lékař vám může předepsat užívání přípravku Humalog Mix50 KwikPen i dlouhodobě působící inzulín. Každý typ inzulinu je dodáván s příslušným letákem obsahujícím informace pro jeho správné použití. Neměňte typ inzulinu, pokud to není předepsáno lékařem. Při změně typu inzulinu buďte velmi opatrní.
Kontraindikace Kdy Humalog nepoužívat
NEPOUŽÍVEJTE Humalog Mix50 KwikPen
- Pokud si myslíte, že začíná hypoglykémie (nízká hladina cukru v krvi). Dále v této příbalové informaci naleznete pokyny pro léčbu mírné hypoglykémie (viz bod: Jestliže užijete více přípravku Humalog, než byste měli).
- Jestliže jste alergický / á (přecitlivělý / á) na inzulín lispro nebo na kteroukoli další složku tohoto přípravku
Opatření pro použití Co potřebujete vědět před užitím přípravku Humalog
- Pokud je vaše hladina glukózy v krvi dobře kontrolována inzulínovou terapií, nemusíte si všimnout varovných příznaků, když se hladina cukru v krvi příliš snižuje. Varovné příznaky jsou uvedeny dále v této příbalové informaci. Musí dávat velký pozor na dobu jídla, frekvenci a oddanost fyzických cvičení a musí také sledovat hladinu cukru v krvi a často ji měřit.
- Někteří lidé, kteří měli hypoglykémii po přechodu ze zvířecího na lidský inzulín, uvedli, že varovné příznaky hypoglykemické reakce byly méně nápadné nebo odlišné. Pokud máte často hypoglykémii nebo máte potíže s rozpoznáním, poraďte se se svým lékařem.
- Pokud je odpověď na některou z následujících otázek ANO, sdělte to prosím svému lékaři, lékárníkovi nebo diabetologické sestře.
Byl jsi v poslední době nemocný?
Máte problémy s játry nebo ledvinami?
Cvičíte více než obvykle?
- Vaše požadavky na inzulín se mohou změnit, pokud pijete alkohol.
- Varujte také svého lékaře, lékárníka nebo diabetologickou sestru, pokud plánujete cestovat do zahraničí. Rozdíly v časových pásmech mezi zeměmi mohou vést ke změně času, kdy si vezmete inzulínové injekce i jídlo., Ve srovnání s tím, když je doma.
- Někteří pacienti s dlouhodobým diabetem 2. typu a srdečním onemocněním nebo s předchozí cerebrovaskulární příhodou, kteří byli léčeni pioglitazonem a inzulínem, hlásili vývoj srdečního selhání. Pokud se u vás objeví příznaky srdečního selhání, jako je neobvyklá dušnost, rychlý přírůstek hmotnosti nebo lokalizovaný otok (edém), sdělte to co nejdříve svému lékaři.
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Humalog
Vaše potřeba inzulínu se může změnit, pokud užíváte
- antikoncepční pilulka,
- kortizon,
- substituční terapie hormonů štítné žlázy,
- orální hypoglykemická činidla,
- kyselina acetylsalicylová,
- sulfonamidová antibiotika,
- oktreotid,
- beta2-agonisté (např. ritodrin, salbutamol, terbutalin),
- beta-blokátory,
- některá antidepresiva (inhibitory monoaminooxidázy, selektivní inhibitory zpětného vychytávání serotoninu),
- danazol,
- některé inhibitory enzymu konvertujícího angiotensin (ACE) (např. kaptopril, enalapril) a
- antagonisté receptoru angiotensinu II.
Informujte svého lékaře, pokud užíváte nebo jste v nedávné době užíval jiné léky, a to i ty, které jsou dostupné bez lékařského předpisu (viz bod „Upozornění a opatření“).
Varování Je důležité vědět, že:
Těhotenství a kojení
Jste těhotná, plánujete otěhotnět nebo kojíte? Potřeba inzulinu se obecně snižuje během prvního trimestru těhotenství a zvyšuje se během následujících šesti měsíců. Pokud kojíte, možná budete muset upravit množství inzulínu, které užíváte, nebo vaši dietu. Požádejte o radu svého lékaře.
Řízení dopravních prostředků a obsluha strojů
Vaše schopnost soustředit se a reagovat může být narušena, pokud máte hypoglykemickou reakci. Tento možný problém mějte na paměti ve všech situacích, kdy byste mohli ohrozit sebe nebo ostatní (například při řízení auta nebo obsluze strojů). O vhodnosti řízení byste se měli poradit se svým lékařem, pokud máte:
- časté epizody hypoglykémie
- snížené nebo žádné varovné příznaky hypoglykémie
Dávka, způsob a doba podání Jak používat Humalog: Dávkování
Vždy zkontrolujte na obalu a štítku předplněného pera název a typ inzulinu, který vám podá lékárník. Ujistěte se, že balení Humalog Mix50 KwikPen odpovídá balení, které vám předepsal lékař.
Vždy používejte přípravek Humalog Mix50 KwikPen přesně podle pokynů svého lékaře. Pokud máte pochybnosti, měli byste se poradit se svým lékařem.
Dávkování
- Humalog Mix50 byste si měli aplikovat zpravidla 15 minut před jídlem. Pokud je to nutné, můžete také podat injekci bezprostředně po jídle. Pokud jde o množství, čas a frekvenci podávání, přesně dodržujte pokyny lékaře: vztahují se výhradně na vás. Přesně je dodržujte a nechte si je pravidelně kontrolovat v diabetologickém centru.
- Pokud změníte typ inzulinu, který používáte (například ze zvířecího nebo lidského inzulinu na přípravek Humalog), možná budete potřebovat jiné (větší nebo menší) množství léku než dříve. Změna může nastat při první injekci nebo může být provedena postupně během několika týdnů nebo měsíců.
- Humalog Mix50 si aplikujte pod kůži. Nepodávejte lék jiným způsobem. Humalog Mix50 by za žádných okolností neměl být podáván intravenózně.
Příprava pera Humalog Mix50 KwikPen
- Bezprostředně před použitím by se mělo pero 10krát otočit mezi dlaněmi a 10krát převrátit o 180 °, aby se obsah resuspendoval, dokud se inzulín neobjeví rovnoměrně zakalený nebo zakalený. Pokud se tak nestane, opakujte výše uvedený postup, dokud nejsou složky smíchány. Náplně jsou vybaveny malou skleněnou kuličkou, která usnadňuje míchání. Netřepejte energicky, protože to může způsobit pěnění, které může ohrozit správné měření dávky. Kazety by měly být často vyšetřovány a neměly by být používány, pokud jsou pozorovány plovoucí zbytky nebo bílé částice ulpívající na dně nebo stěnách kazety, což jí dodává zmrazený vzhled. Zkontrolujte to před každou injekcí.
Příprava pera (viz návod k použití)
- Nejprve si umyjte ruce.
- Přečtěte si pokyny k použití předplněného inzulínového pera a pečlivě je dodržujte. Zde jsou některé důležité body.
- Vždy používejte novou jehlu (jehly nejsou součástí balení).
- Před každým použitím pero nabijte. To vám umožní zkontrolovat, zda inzulín uniká, a odstranit z něj vzduchové bubliny. V peru mohou zůstat malé vzduchové bubliny; nejsou nebezpečné, ale pokud jsou příliš velké, mohou způsobit, že dávka bude méně přesná.
Injekce přípravku Humalog Mix50
- Před podáním injekce si vydezinfikujte kůži podle pokynů, které jste dostali. Vpíchněte lék pod kůži, jak jste byli poučeni. Nepodávejte injekci přímo do žíly. Po injekci nechte jehlu v kůži po dobu 5 sekund. abyste se ujistili, že jste si podali celou dávku. Místo, kde jste si podali injekci, nemažte. Ujistěte se, že místo vpichu je vzdáleno alespoň jeden centimetr od předchozího času a nezapomeňte místo vpichu střídat, jak vám bylo řečeno.
Po injekci
- Jakmile injekci dokončíte, vyjměte jehlu z pera pomocí vnějšího krytu jehly. To vám umožní udržovat inzulín sterilní, zabráníte rozlití léčiva, zabráníte proudění vzduchu do pera a zabráníte ucpání jehly Nesdílejte své jehly s ostatními. Sdílejte své pero s ostatními. Nasaďte víčko zpět na pero.
Následné injekce
- Pokaždé, když použije pero, musí použít novou jehlu. Před každou injekcí odstraňte všechny vzduchové bubliny.Můžete zkontrolovat, kolik inzulinu zbývá, držením pera ve svislé poloze s jehlou směřující dolů. Dělení na kazetě bude ukazovat přibližně zbývající jednotky.
- Nemíchejte v peru žádné jiné inzulíny. Jakmile je pero prázdné, již jej nepoužívejte. Zbavte se toho, prosím, moudře. Personál lékárníka nebo diabetologického centra vám řekne, jak na to.
Předávkování Co dělat, když jste užil příliš mnoho přípravku Humalog
Jestliže jste užil (a) více přípravku Humalog Mix50 KwikPen, než jste měl
Jestliže užijete více přípravku Humalog Mix50 KwikPen, než byste měli, může dojít ke snížení hladiny cukru v krvi.
Zkontrolujte si hladinu cukru v krvi. Pokud je hladina cukru v krvi nízká (mírná hypoglykémie), jezte glukózové tablety, trochu cukru nebo slazený nápoj. Poté jezte ovoce, sušenky nebo sendvič, jak vám doporučil lékař, a odpočívejte. Často to stačí k vyrovnání „mírné hypoglykémie nebo menšího předávkování inzulínem. Pokud si všimnete, že se zhoršuje a zadýcháváte se a kůže bledne, okamžitě to sdělte svému lékaři. Injekce glukagonu může léčit poměrně závažnou hypoglykémii • Po injekci glukagonu vezměte glukózu nebo cukr. Pokud se mu glukagonu nedostane pozitivní reakce, musí být hospitalizován. Zeptejte se svého lékaře na používání glukagonu.
Jestliže jste zapomněli použít Humalog Mix50 KwikPen
Jestliže užijete méně přípravku Humalog Mix50 KwikPen, než potřebujete, může dojít ke zvýšení hladiny cukru v krvi. Zkontrolujte si hladinu cukru v krvi.
Neléčená hypoglykémie (nízká hladina cukru v krvi) nebo hyperglykémie (vysoká hladina cukru v krvi) může být velmi závažná a způsobit bolesti hlavy, nevolnost, zvracení, dehydrataci, bezvědomí, kóma a dokonce smrt (viz odstavce A a B oddílu 4 „Možná strana efekty “).
Tři jednoduché kroky, jak se vyhnout situacím hypoglykémie nebo hyperglykémie:
- Vždy mějte náhradní stříkačky a náhradní lahvičku Humalogu.
- Vždy mějte u sebe doklad o tom, že jste diabetik.
- Noste cukr vždy s sebou.
Jestliže jste přestal užívat Humalog Mix50 KwikPen
Jestliže užijete méně přípravku Humalog Mix50 KwikPen, než potřebujete, může dojít ke zvýšení hladiny cukru v krvi. Neměňte typ inzulinu, pokud to není předepsáno lékařem.
Máte -li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Humalog
Podobně jako všechny léky, může mít i Humalog Mix50 nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Místní alergie je běžná (≥ 1/100 až <1/10). U některých lidí může být kůže v místě vpichu červená, oteklá a svědivá. Tato reakce obvykle zmizí během několika dnů až několika týdnů. Pokud k tomu dojde , řekněte to svému lékaři.
Systémová alergie je vzácná (≥ 1/10 000 až <1/1 000). Příznaky jsou:
- vyrážka po celém těle
- potíže s dýcháním
- dušnost
- snížení krevního tlaku
- rychlý srdeční tep
- pocení
Pokud si myslíte, že vám Humalog způsobuje tento typ alergie na inzulín, ihned to sdělte svému lékaři.
Lipodystrofie (zesílení nebo mírná deprese kůže) je méně častá (≥ 1/1 000 až <1/100). Pokud máte pocit, že vaše kůže houstne nebo že je v místě vpichu mírná deprese, sdělte to prosím svému lékaři.
Byly hlášeny otoky (např. Otoky paží, kotníků; zadržování tekutin), zejména na začátku inzulínové terapie nebo během změny terapie ke zlepšení kontroly glykémie.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48100 41 Praha 10 Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
Běžné problémy s diabetem
A. Hypoglykémie
Hypoglykemie (nízká hladina cukru v krvi) znamená, že v krvi není dostatek cukru. Hypoglykémii může způsobit:
- předávkování přípravkem Humalog nebo „jiným inzulínem“;
- zpoždění nebo zmeškané jídlo nebo změna stravy;
- nadměrné cvičení nebo fyzická práce prováděná bezprostředně před nebo po jídle;
- „infekce nebo jiná porucha (zejména průjem nebo zvracení);
- změna potřeby inzulínu;
- zhoršení již existující poruchy ledvin nebo jater.
Alkohol a některé léky mohou interferovat s vaší hladinou cukru v krvi.
První příznaky hypoglykemie se obvykle objevují rychle a zahrnují:
- únava
- nervozita nebo agitovanost
- bolest hlavy
- rychlý srdeční tep
- nevolnost
- studený pot
Pokud nejste schopni rozpoznat varovné příznaky hypoglykémie, vyhýbejte se situacím, jako je řízení auta, ve kterých by hypoglykémie mohla ohrozit vás nebo ostatní.
B. Hyperglykémie a diabetická ketoacidóza
Hyperglykémie (příliš mnoho cukru v krvi) znamená, že ve vašem těle není dostatek inzulinu. Hyperglykémii může způsobit:
- neužívání přípravku Humalog nebo jiného inzulinu;
- užívání dávky inzulinu nižší, než je předepsáno lékařem;
- příjem jídla v množství mnohem vyšším, než povoluje dieta;
- horečka, infekce nebo silné emoce.
Hyperglykémie může vést k diabetické ketoacidóze.První příznaky začínají pomalu, po mnoho hodin nebo dnů. Oni rozumí:
- Ospalý
- zarudnutí obličeje
- žízeň
- nedostatek chuti k jídlu
- ovocný dech
- necítím se dobře
Těžké dýchání a zrychlený tep jsou vážnými příznaky. Okamžitě vyhledejte lékařskou pomoc.
C. Nemoci
Pokud máte onemocnění, zvláště pokud se cítíte nebo jste nemocní, mohou se vaše požadavky na inzulín lišit. I když nejí normálně, stále potřebuje inzulín. Nechte si otestovat testy moči a krve; pokud jste nemocní, dodržujte opatření, která již znáte, a sdělte to svému lékaři.
Expirace a retence
Před použitím uchovávejte Humalog Mix50 KwikPen v chladničce (2 ° C - 8 ° C). Chraňte před mrazem.
Během používání uchovávejte Humalog Mix50 KwikPen při pokojové teplotě (15 ° - 30 ° C) a po 28 dnech jej zlikvidujte. Neuchovávejte přípravek v blízkosti zdroje tepla nebo na přímém slunci. KwikPen by neměl být skladován s vloženou jehlou .
Uchovávejte mimo dosah a dohled dětí
Humalog Mix50 KwikPen nepoužívejte po uplynutí doby použitelnosti, uvedené na štítku a krabičce. Datum exspirace se vztahuje k poslednímu dni uvedeného měsíce. Nepoužívejte Humalog Mix50 KwikPen, pokud na dně nebo stěnách kazety ulpívají plovoucí zbytky nebo bílé částice, což jí dodává zmrazený vzhled. Zkontrolujte to před každou injekcí.
Léčivé přípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Co Humalog Mix50 100 U / ml KwikPen injekční suspenze obsahuje
- Léčivou látkou je „inzulín lispro. Insulin lispro se vyrábí v laboratoři pomocí technologie nazývané„ rekombinantní DNA “. Jedná se o modifikovanou formu lidského inzulínu, a proto se liší od ostatních inzulínů lidského nebo zvířecího původu. Inzulin lispro je strukturálně podobný lidskému inzulínu, což je přirozeně se vyskytující hormon produkovaný slinivkou břišní.
- Dalšími složkami jsou protamin sulfát, m-kresol, fenol, glycerol, hydrogenfosforečnan sodný 7H2O, oxid zinečnatý a voda na injekci. K úpravě pH mohl být přidán hydroxid sodný nebo kyselina chlorovodíková. Dokument zpřístupněný AIFA dne 17/10/2014 246
Jak vypadá Humalog Mix50 100 U / ml KwikPen injekční suspenze a obsah balení
Humalog Mix50 100 U / ml KwikPen injekční suspenze je sterilní bílá suspenze a obsahuje 100 jednotek inzulínu lispro na každý mililitr (100 U / ml) injekční suspenze. 50% inzulínu lispro obsaženého v přípravku Humalog Mix50 je rozpuštěno ve vodě.50% inzulínu lispro obsaženého v přípravku Humalog Mix50 je přítomno v suspenzi společně s protamin sulfátem. Každý Humalog Mix50 KwikPen obsahuje 300 jednotek (3 mililitry).Humalog Mix50 KwikPen je k dispozici v balení s 5 předplněnými pery nebo v multipacku se 2 baleními po 5 předplněných perech. Na trhu nemusí být všechny velikosti balení. Humalog Mix50 obsažený v peru je stejný přípravek obsažený v zásobnících Humalog Mix50. Náplň je již v peru. Když je pero prázdné, nemůžete ho znovu použít.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Chcete-li mít přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
HUMALOG MIX50 100 U / ML KWIKPEN, INJECTABLE SUSPENSION
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Humalog Mix50 je bílá, sterilní suspenze.
Jeden ml obsahuje 100 U (odpovídá 3,5 mg) inzulinu lispro (pocházejícího z rekombinantní DNA vyrobené v E-coli). Každé balení obsahuje 3 ml, což odpovídá 300 U inzulínu lispro.
Humalog Mix50 se skládá z 50% roztoku inzulinu lispro a 50% suspenze protispamu lispro.
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Injekční suspenze.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Humalog Mix50 je indikován k léčbě pacientů s diabetes mellitus, kteří potřebují inzulín k udržení normální glukózové homeostázy.
04.2 Dávkování a způsob podání
Dávkování by měl stanovit lékař podle potřeb pacienta.
Humalog Mix50 lze podávat těsně před jídlem. V případě potřeby lze přípravek Humalog Mix50 podat také bezprostředně po jídle. Humalog Mix50 by měl být podáván pouze subkutánní injekcí. Humalog Mix50 by za žádných okolností neměl být podáván intravenózně.
Subkutánní injekce by měla být podána do paží, stehen, hýždí nebo břicha. Místo vpichu by mělo být střídáno tak, aby bylo stejné místo postiženo přibližně jednou za měsíc.
Při subkutánní injekci přípravku Humalog Mix50 je třeba zajistit, aby se jehla nedostala do cévy.Po injekci by se nemělo masírovat místo na kůži. Pacienti by měli být poučeni, aby používali vhodné injekční techniky.
Po subkutánním podání přípravku Humalog Mix50 dochází k rychlému nástupu a časnému vrcholu aktivity Humalogu. To znamená, že přípravek Humalog Mix50 lze podávat velmi blízko jídla. Trvání účinku suspenze protaminu inzulínu lispro (BASAL), která je součástí přípravku Humalog Mix50, je podobné jako u isofanového inzulínu.
Trvání účinku jakéhokoli inzulínu se může u různých jedinců nebo u stejného jedince při různých příležitostech velmi lišit. Stejně jako u všech inzulínových přípravků závisí trvání účinku Humalogu Mix50 na několika faktorech, jako je dávka, místo vpichu, průtok krve, tělesná teplota a fyzická aktivita pacienta.
04.3 Kontraindikace
Přecitlivělost na inzulín lispro nebo na kteroukoli pomocnou látku.
Hypoglykémie.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Humalog Mix50 by za žádných okolností neměl být podáván intravenózně.
Převedení pacienta na inzulínovou terapii na jiný typ nebo značku inzulínu by mělo být provedeno pod přísným lékařským dohledem. Změny koncentrace, značky (výrobce), typu (běžný, isofanový, pomalý atd.), Druhu (zvířecí, lidský, analog lidského inzulínu) a / nebo způsobu produkce (rekombinantní DNA versus zvířecí inzulín) mohou mít za následek potřebu změny dávkování.
Stavy, které mohou způsobit různé nebo méně zjevné včasné varovné příznaky hypoglykémie, zahrnují dlouhotrvající diabetes, zesílení inzulínové terapie, diabetickou neuropatii nebo užívání léků, jako jsou beta-blokátory.
Někteří pacienti, u nichž došlo k hypoglykemickým reakcím po převodu z inzulinu živočišného původu na lidský inzulín, uvedli, že varovné příznaky této příhody byly méně zřejmé nebo se lišily od těch, které se vyskytly během léčby dříve použitým inzulínem. Nekontrolované hypo- a hyperglykemické reakce mohou způsobit bezvědomí, kóma nebo smrt.
Použití neadekvátních dávek nebo přerušení léčby, zejména u pacientů s inzulín-dependentním diabetes mellitus, může vést k hyperglykémii nebo diabetické ketoacidóze, dvěma život ohrožujícím stavům.
V případě renální insuficience se mohou požadavky na inzulín snížit. Potřeba inzulinu se může snížit u pacientů s jaterní insuficiencí v důsledku snížené glukoneogeneze a sníženého inzulínového katabolismu; nicméně u pacientů s chronickou jaterní insuficiencí může zvýšení inzulinové rezistence vést ke zvýšení potřeby inzulinu.
Potřeba inzulínu se může zvýšit v průběhu nemoci nebo emočních poruch.
Úprava dávkování inzulínu může být také nezbytná, pokud pacient zvýší svou fyzickou aktivitu nebo změní obvyklou dietu.Pohyb bezprostředně po jídle může zvýšit riziko hypoglykémie.
Podání inzulínu lispro dětem mladším 12 let by mělo být zvažováno pouze tehdy, pokud se očekává větší přínos, než jaký je výsledkem používání běžného inzulinu.
Použití přípravku Humalog Mix50 v kombinaci s pioglitazonem
Při podávání pioglitazonu v kombinaci s inzulínem byly hlášeny případy srdečního selhání, zejména u pacientů s rizikovými faktory pro rozvoj srdečního selhání. To je třeba mít na paměti při zvažování léčby kombinací pioglitazonu a Humalogu Mix50. Pokud je použita tato kombinace, pacienti by měli být sledováni s ohledem na známky a příznaky srdečního selhání, zvýšení tělesné hmotnosti a otoky Pokud dojde ke zhoršení srdečních symptomů, pioglitazon by mělo být přerušeno.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Potřeba inzulínu se může zvýšit v důsledku současného podávání látek s hyperglykemickou aktivitou, jako jsou orální kontraceptiva, kortikosteroidy nebo během substituční terapie hormony štítné žlázy, danazolem a beta2-agonisty (stejně jako salbutamol, terbutalin, ritodrin).
Potřeba inzulínu se může snížit v důsledku současného podávání látek s hypoglykemickou aktivitou, jako jsou například orální hypoglykemická činidla, salicyláty (například kyselina acetylsalicylová), sulfonamidová antibiotika, některá antidepresiva (inhibitory monoaminooxidázy, selektivní inhibitory zpětného vychytávání serotonin), některé inhibitory angiotensin konvertujícího enzymu (kaptopril, enalapril), antagonisté receptoru angiotensinu II, beta-blokátory, oktreotid nebo alkohol.
Míchání přípravku Humalog Mix50 s jinými inzulíny nebylo studováno.
Pacient by měl varovat ošetřujícího lékaře, pokud kromě Humalog Mix50 KwikPen užívá i jiné léky (viz bod 4.4).
04.6 Těhotenství a kojení
Údaje o velkém počtu těhotných žen vystavených léku nevykazují žádné nežádoucí účinky inzulínu lispro na těhotenství nebo na zdraví plodu / novorozence.
Během těhotenství je nezbytné udržovat dobrou kontrolu nad pacientkami léčenými inzulínem, a to jak u pacientů s gestačním diabetem, tak u pacientů s diabetes mellitus závislým na inzulínu. Potřeba inzulinu se obecně snižuje během prvního trimestru a zvyšuje se ve druhém a třetím trimestru. Diabetické pacientky by měly informovat svého lékaře v případě, že jsou těhotné nebo to plánují. Pečlivá kontrola kontroly glukózy a celkového zdravotního stavu je základním požadavkem těhotných žen s diabetem.
Kojící diabetičky mohou vyžadovat úpravu dávky inzulínu a / nebo diety.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Schopnost pacienta soustředit se a reagovat může být snížena v důsledku hypoglykémie. Tato skutečnost může představovat riziko v situacích, kdy jsou tyto dovednosti obzvláště důležité (například řízení auta nebo obsluha strojů).
Pacienti by měli být poučeni, aby přijali nezbytná opatření, aby se vyhnuli hypoglykemické reakci během řízení, a to je zvláště důležité u osob, které si málo nebo vůbec neuvědomují varovné příznaky hypoglykémie nebo mají časté epizody hypoglykémie. Za takových okolností má příležitost je třeba zvážit řízení.
04.8 Nežádoucí účinky
Hypoglykémie je nejčastějším vedlejším účinkem inzulinové terapie, který může diabetický pacient zažít. Silná hypoglykemie může vést ke ztrátě vědomí a v extrémních případech ke smrti. Pro hypoglykémii není uvedena žádná konkrétní frekvence, protože hypoglykemie je výsledkem dávky inzulínu i dalších faktorů, jako je pacientova dieta a fyzická aktivita.
Lokální alergie u pacientů je běžná (v místě vpichu inzulínu se může objevit 1/100 až svědění. Tyto projevy obvykle vymizí po několika dnech nebo po několika týdnech. V některých případech mohou být tyto projevy způsobeny jinými faktory než " inzulín jako dráždivé látky přítomné v přípravku používaném k dezinfekci kůže nebo nesprávné injekční technice. "Systémová alergie, která je vzácná (1/10 000 až dušnost, mělké dýchání, pokles krevního tlaku, tachykardie, pocení Těžkým případem generalizované alergie může být život -hrozivý.
Lipodystrofie v místě vpichu je neobvyklá (1/1 000 až
Při inzulínové terapii byly hlášeny případy otoků, zvláště když byla předchozí špatná metabolická kontrola zlepšena intenzivnější inzulinovou terapií.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky, ke kterým dochází po registraci léčivého přípravku, je důležité, protože umožňuje průběžné sledování poměru přínosů a rizik léčivého přípravku. Zdravotničtí pracovníci jsou požádáni, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení. V "Příloha V .
04.9 Předávkování
Inzulín nemá vhodnou definici předávkování, protože koncentrace glukózy v séru jsou výsledkem komplexních interakcí mezi hladinami inzulínu, dostupností glukózy a dalšími metabolickými procesy. Hypoglykémie může nastat v důsledku nadměrné aktivity inzulínu ve vztahu k příjmu potravy a výdeji energie .
Hypoglykémie může být spojena s únavou, zmateností, bušením srdce, bolestmi hlavy, studeným pocením a zvracením.
Epizody mírné hypoglykémie reagují na orální podání glukózy, cukru nebo sladkých produktů.
Korekce středně těžké hypoglykémie lze dosáhnout intramuskulárním nebo subkutánním podáním glukagonu a následným požitím orálních sacharidů, jakmile to stav pacienta dovolí. Jedinci, kteří nereagují na glukagon, by měli dostat intravenózní roztok glukózy.
Pokud je pacient v hypoglykemickém kómatu, měl by být glukagon podáván intramuskulárně nebo subkutánně. Pokud však glukagon není k dispozici nebo pokud pacient nereaguje na podání glukagonu, měly by být podány intravenózní roztoky glukózy. Pacient by měl mít jídlo, jakmile získá vědomí.
Vzhledem k tomu, že se hypoglykémie může po zjevném klinickém zotavení opakovat, může být nutné pacienta sledovat a získat spoustu sacharidů.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Humalog Mix50 je předem smíchaná suspenze sestávající z inzulínu lispro (rychle působící analog lidského inzulínu) a suspenze inzulinu lispro protamin (středně působící analog lidského inzulínu). ATC kód: A10AD04.
Hlavní činností inzulínu lispro je regulace metabolismu glukózy.
Kromě toho inzulín působí na různé tkáně různými antikatabolickými a anabolickými aktivitami.Ve svalové tkáni zvyšuje syntézu glykogenu, mastných kyselin, glycerolu, bílkovin a příjem aminokyselin, přičemž snižuje glykogenolýzu, glukoneogenezi, ketogenezi, lipolýzu, katabolismus bílkovin a produkci aminokyselin.
Inzulin lispro má rychlý účinek (nástup přibližně do 15 minut), což umožňuje podání blíže k jídlu (do 0–15 minut) než běžný inzulín, který je nutné podávat 30–45 minut před jídlem. Po subkutánním podání přípravku Humalog Mix50 dochází k rychlému nástupu a časnému vrcholu aktivity inzulínu lispro. Po přibližně 15 hodinách po podání má Humalog BASAL profil aktivity, který je velmi podobný profilu isofanového inzulínu.
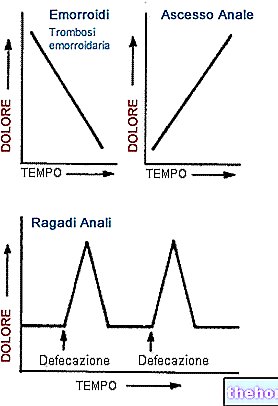
Výše uvedený graf ukazuje množství glukózy v závislosti na čase, které je nezbytné pro subjekt k udržení koncentrace glukózy v plné krvi kolem hodnot glukózy nalačno, a je také znázorněním účinku těchto látek v čase inzulíny na metabolismus glukózy.
Glukodynamická odpověď na inzulín lispro není ovlivněna nedostatečnou funkcí ledvin nebo jater. Glukodynamické rozdíly mezi inzulínem lispro a rozpustným lidským inzulínem, hodnocené během postupu glykemické svorky, byly udržovány v širokém rozmezí funkcí ledvin.
Bylo prokázáno, že inzulín lispro je na základě molarity ekvipotentní vůči lidskému inzulínu, ale jeho účinek je rychlejší a má kratší trvání.
05.2 Farmakokinetické vlastnosti
Farmakokinetika inzulínu lispro naznačuje, že se sloučenina rychle vstřebává a dosahuje maximálních hladin v krvi 30 až 70 minut po subkutánní injekci.Farmakokinetické profily suspenze protaminového inzulinu lispro jsou v souladu s profily středně účinného inzulínu, jako je I .
Farmakokinetické profily přípravku Humalog Mix50 jsou reprezentativní pro jednotlivé farmakokinetické vlastnosti těchto dvou složek. Při hodnocení klinického významu těchto kinetik je třeba vzít v úvahu křivky využití glukózy (viz bod 5.1).
U pacientů s renální insuficiencí udržuje inzulín lispro rychlejší absorpci než rozpustný lidský inzulín. U pacientů s diabetem typu 2 byly v rámci velké změny funkce ledvin kinetické rozdíly mezi inzulínem lispro a rozpustným lidským inzulínem v podstatě zachovány a bylo prokázáno, že jsou nezávislé na funkci ledvin. U pacientů s jaterní insuficiencí udržuje inzulín Lispro rychlejší absorpci a eliminace než rozpustný lidský inzulín.
05.3 Předklinické údaje vztahující se k bezpečnosti
V testech in vitro, včetně vazby na místa inzulínových receptorů a účinků na vyvíjející se buňky, inzulín lispro měl chování velmi podobné lidskému inzulínu. Studie také ukazují, že disociace inzulínu lispro z inzulínových receptorů je ekvivalentní lidskému inzulínu.Akutní, jednoměsíční a dvanáctiměsíční toxikologické studie nepřinesly žádné významné nálezy toxicity.
Ve studiích na zvířatech inzulín lispro nezpůsobil narušenou plodnost, embryotoxicitu ani teratogenitu.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Protamin sulfát; m-kresol (2,20 mg / ml); fenol (1,00 mg / ml); glycerol; hydrogenfosforečnan sodný 7H20; oxid zinečnatý; voda na injekci; pro úpravu pH na 7,0-7,8 lze použít kyselinu chlorovodíkovou a hydroxid sodný.
06.2 Neslučitelnost
Míchání přípravku Humalog Mix50 s jinými inzulíny nebylo studováno. Studie kompatibility nejsou k dispozici, a proto nesmí být léčivý přípravek mísen s jinými přípravky.
06.3 Doba platnosti
Nepoužitá předplněná pera
3 roky.
Po prvním použití
28 dní.
06.4 Zvláštní opatření pro skladování
Nepoužitá předplněná pera
Uchovávejte v chladničce (2 ° C - 8 ° C). Chraňte před mrazem. Nevystavujte nadměrnému teplu nebo přímému slunečnímu světlu.
Po prvním použití
Uchovávejte při teplotě do 30 ° C. Neuchovávejte v chladničce. Předplněné pero by nemělo být skladováno s nasazenou jehlou.
06.5 Charakter vnitřního obalu a obsah balení
Suspenze je obsažena v kazetách z tvrdého skla typu I, zapečetěných halobutylovými diskovými těsněními a hlavami pístu a těsně uzavřených hliníkovými těsněními. Dimethicone nebo silikonová emulze mohou být použity k ošetření pístu náplně a / nebo skla patrony. 3ml náplně jsou uzavřeny v zařízení pro injekční pero, kterému se říká „KwikPen“. Jehly nejsou součástí balení.
Na trhu nemusí být všechny velikosti balení.
5 Humalog Mix50 100 U / ml KwikPen 3ml pera.
2 x 5 Humalog Mix50 100 U / ml KwikPen 3ml pera.
06.6 Návod k použití a zacházení
Nepoužitý léčivý přípravek a odpady z tohoto přípravku musí být zlikvidovány v souladu s místními předpisy.
Návod k použití a zacházení
Bezprostředně před použitím je třeba KwikPen 10krát otočit mezi dlaněmi a 10krát otočit o 180 °, aby se obsah resuspendoval, dokud nebude inzulín rovnoměrně zakalený nebo mléčný. Pokud se tak nestane, opakujte výše uvedený postup, dokud nejsou složky smíchány. Náplně jsou vybaveny malou skleněnou kuličkou, která usnadňuje míchání. Netřepejte energicky, protože to může způsobit pěnění, které může ohrozit správné měření dávky.
Kazety by měly být často vyšetřovány a neměly by být používány, pokud jsou pozorovány plovoucí zbytky nebo bílé částice ulpívající na dně nebo stěnách kazety, což jí dodává zmrazený vzhled.
Manipulace s předplněným perem
Před použitím pera KwikPen byste si měli pečlivě přečíst návod k použití, který je součástí příbalové informace. Pero KwikPen by mělo být používáno podle doporučení v návodu k použití.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Eli Lilly Nederland B.V. - Grootslag 1-5, 3991 RA Houten - Nizozemsko
08.0 REGISTRAČNÍ ČÍSLO
EU/1/96/007/035, 5 Humalog Mix50 100 U/ml KwikPen 3 ml - AIC: 033637238
EU/1/96/007/036, 2 x 5 Humalog Mix50 100 U/ml KwikPen 3 ml - AIC: 033637240
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Datum první registrace: 30. dubna 1996
Datum posledního prodloužení: 30. dubna 2006
10.0 DATUM REVIZE TEXTU
D.CCE ZÁŘÍ 2014