Účinné látky: flutikason (flutikason furoát)
Avamys 27,5 mikrogramů na sprej, nosní sprej, suspenze
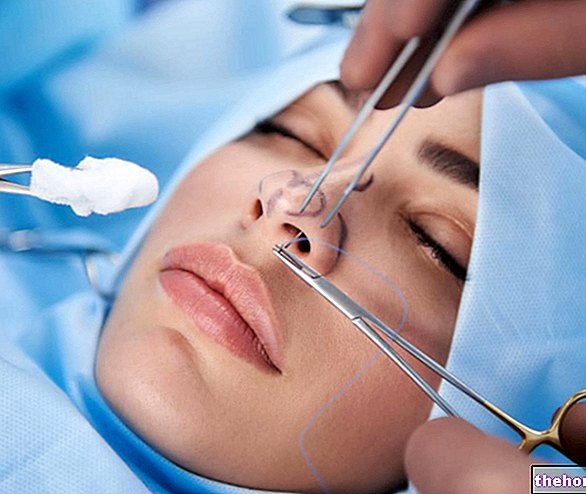
Proč se Avamys používá? K čemu to je?
Avamys (flutikason -furoát) patří do skupiny léků nazývaných glukokortikoidy.
Avamys působí tak, že snižuje zánět způsobený alergií (rýma), a tím snižuje příznaky alergie. Avamys nosní sprej se používá k léčbě příznaků alergické rýmy, včetně ucpaného, rýmového nebo svědivého nosu, kýchání, slzení očí, svědění a zarudnutí očí, u dospělých a dětí od 6 let.
Příznaky alergie se mohou objevit v přesně definovaných obdobích roku a mohou být způsobeny alergiemi na pyl trávy nebo stromů (senná rýma), nebo se mohou vyskytovat po celý rok a být způsobeny alergiemi na zvířata. Roztoči domácího prachu nebo plísně vyjmenujte několik nejběžnějších.
Kontraindikace Kdy by Avamys neměl být používán
Neužívejte Avamys:
- Jestliže jste alergický (á) na flutikason -furoát nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
Opatření pro použití Co potřebujete vědět před užitím přípravku Avamys
Pokud máte jakékoli problémy s játry, sdělte to prosím svému lékaři nebo lékárníkovi.
Děti a dospívající
Nepoužívejte u dětí mladších 6 let.
Užívání Avamys:
- může to způsobit, že děti rostou pomaleji, pokud jsou užívány dlouhodobě. Váš lékař bude pravidelně kontrolovat výšku vašeho dítěte a ujistí se, že užívá nejnižší možnou účinnou dávku.
- může způsobit oční onemocnění, jako je glaukom (zvýšený nitrooční tlak) nebo katarakta (zakalení oční čočky). Informujte svého lékaře, pokud jste v minulosti měl (a) tato onemocnění, nebo pokud si během užívání přípravku Avamys všimnete jakýchkoli změn ve vašem vidění.
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Avamys
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval (a) nebo které možná budete užívat.
Je zvláště důležité informovat svého lékaře, pokud užíváte nebo jste v nedávné době užíval některý z následujících léků:
- steroidy v tabletách nebo steroidy pro injekce
- krémy na bázi steroidů
- léky na astma
- ritonavir, používaný k léčbě HIV
- ketokonazol, používaný k léčbě houbových infekcí
Váš lékař zkontroluje, zda byste měli užívat Avamys s těmito léky.
Avamys by neměl být používán současně s jinými nosními spreji obsahujícími steroidy.
Varování Je důležité vědět, že:
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat.
Neužívejte Avamys, pokud jste těhotná nebo plánujete otěhotnět, pokud vám to lékař nebo lékárník neřekne.
Neužívejte Avamys, pokud kojíte, pokud vám to lékař nebo lékárník neřekne.
Řízení dopravních prostředků a obsluha strojů
Je nepravděpodobné, že by Avamys narušoval vaši schopnost řídit nebo obsluhovat stroje.
Avamys obsahuje benzalkonium -chlorid
U některých pacientů může benzalkonium -chlorid způsobit podráždění nosu. Pokud pocítíte při používání spreje nepříjemné pocity, sdělte to svému lékaři nebo lékárníkovi.
Dávka, způsob a doba podání Jak používat Avamys: Dávkování
Vždy používejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Nepřekračujte doporučené dávky. Pokud máte pochybnosti, poraďte se se svým lékařem nebo lékárníkem.
Kdy použít Avamys
- Vezměte si to jednou denně
- Užívejte každý den ve stejnou dobu
To vám umožní kontrolovat vaše příznaky po celý den a noc.
Jak dlouho trvá, než Avamys začne fungovat
Někteří lidé pocítí plnou účinnost přípravku Avamys několik dní po prvním použití.
Obvykle je však účinný do 8-24 hodin od prvního nazálního podání.
Kolik Avamys použít
Dospělí a děti od 12 let
- Normální počáteční dávka jsou 2 vstřiky do každé nosní dírky jednou denně, každý den.
- Jakmile jsou příznaky pod kontrolou, je možné snížit dávku na 1 vstřik do každé nosní dírky, jednou denně, každý den.
Děti ve věku od 6 do 11 let
- Obvyklá počáteční dávka je 1 vstřik do každé nosní dírky jednou denně.
- Pokud jsou příznaky zvláště závažné, může lékař zvýšit dávku na 2 vstřiky do každé nosní dírky jednou denně, každý den, dokud nejsou příznaky pod kontrolou. Proto může být možné snížit dávku na 1 vstřik do každé nosní dírky, jednou denně, každý den.
Jak používat nosní sprej
Avamys prakticky nemá chuť ani vůni. Stříká se do nosu jako jemná mlha. Dávejte pozor, abyste si jej nestříkli do očí. Pokud k tomu dojde, vypláchněte si oči vodou.
KROK ZA KROKEM NÁVOD K POUŽITÍ NASÁLNÍHO SPREJE
Jak vypadá nosní sprej
Nosní sprej je dodáván v lahvičce ze žlutého skla vložené do plastového zařízení - viz obrázek a. Láhev obsahuje 30, 60 nebo 120 potahů, v závislosti na předepsaném balení.
Okénko na boční straně plastového inhalátoru umožňuje zobrazit množství léčiva zbývajícího v lahvičce. Hladinu kapaliny můžete vidět u nové lahvičky s 30 nebo 60 potahy, ale ne u nové lahve se 120 střety, protože pro v druhém případě je hladina kapaliny nad oknem.
Šest věcí, které potřebujete vědět o používání nosního spreje
- Avamys se dodává v lahvi ze žlutého skla. Pokud potřebujete zkontrolovat, kolik léčiva v lahvičce zbývá, držte nosní sprej ve svislé poloze proti světlu. Tímto způsobem budete moci vidět hladinu léku oknem.
- Při prvním použití nosního spreje je třeba s víčkem na místě důkladně protřepat asi 10 sekund. To je důležité, protože Avamys je hustá suspenze, která se při dobrém protřepání stává tekutou - viz obrázek b. Lék bude stříkat, až když bude tekutý
- Uvolňovací tlačítko musí být pevně stisknuto, aby se mlha uvolnila tryskou
- Pokud máte potíže se stiskem uvolňovacího tlačítka palcem, můžete použít obě ruce
- Pokud přípravek nepoužíváte, vždy držte víčko na nosním spreji. Víko chrání před prachem, těsní tlakem a zabraňuje ucpání hubice. Když je víko na svém místě, nelze uvolňovací tlačítko omylem stisknout.
- K čištění trysky nepoužívejte špendlík ani špičaté předměty. To by zablokovalo nosní sprej.
Příprava nosního spreje k použití
Nosní sprej musí být připraven:
- před jeho prvním použitím
- pokud bylo víčko ponecháno na místě po dobu 5 dnů nebo nebylo intranazální zařízení používáno po dobu 30 dnů nebo déle
Příprava nosního spreje zajišťuje podání celé dávky léku. Postupujte podle následujících kroků:
- Silně protřepejte nosní sprej s víčkem na místě asi 10 sekund
- Sundejte kryt pevným stlačením bočních stran krytu palcem a ukazováčkem
- Držte nosní sprej ve svislé poloze, poté jej nakloňte a namiřte trysku směrem od sebe.
- Pevně stiskněte tlačítko úplně. Opakujte operaci alespoň 6krát, dokud ve vzduchu nepozorujete řídkou mlhu
Nosní sprej je nyní připraven k použití.
Pomocí nosního spreje
- Silně protřepejte nosní sprej.
- 2 Sejměte kryt.
- 3 Vyfoukněte nos, abyste vyčistili nosní dírky, a pak nakloňte hlavu dopředu.
- 4 Umístěte trysku do jedné z nosních dírek. Tryska by měla být umístěna uvnitř nosní dírky směrem ven z nosu, mimo centrální přepážku. To podporuje uvolňování léčiva v pravé části nosu.
- Při nádechu nosem pevně stiskněte tlačítko
- Vytáhněte trysku a vydechněte ústy.
- Pokud je předepsaná dávka 2 vstřiky do každé nosní dírky, opakujte kroky 4 až 6.
- Opakujte kroky 4 až 7 a ošetřete druhou nosní dírku.
- Nasaďte víčko zpět na nosní sprej.
Čištění nosního spreje
Po každém použití:
- Vyčistěte výtok a vnitřní část víka čistou, suchou utěrkou
- K čištění nosního spreje nepoužívejte vodu.
- Na hubici nikdy nepoužívejte špendlík nebo špičatý předmět.
- 4 Po použití vždy nasaďte víčko zpět na sprej.
Pokud se zdá, že nosní sprej nefunguje:
- Zkontrolujte, zda nezůstal nějaký lék. Podívejte se na hladinu drogy oknem. Pokud je hladina léku velmi nízká, nemusí zbývat dostatečné množství, aby nosní sprej fungoval.
- Zkontrolujte, zda není nosní sprej poškozen.
- Pokud si myslíte, že může být tryska zablokovaná, nepoužívejte k čištění špendlík ani žádný ostrý předmět.
- Zkuste jej znovu uvést do provozu podle pokynů v části „Příprava nosního spreje k použití“.
Pokud nosní sprej stále nefunguje nebo pokud vytváří proud tekutého roztoku, vraťte nosní sprej svému lékárníkovi o radu.
Předávkování Co dělat, když jste užil příliš mnoho přípravku Avamys
Jestliže jste užil (a) více přípravku Avamys, než jste měl
Informujte svého lékaře nebo lékárníka.
Jestliže jste zapomněl (a) užít Avamys
Pokud vynecháte dávku, vezměte si ji, když si vzpomenete.
Pokud se blíží podání další dávky, počkejte do té doby. Nezdvojnásobujte následující dávku, abyste nahradil (a) vynechanou dávku.
Máte -li jakékoli další otázky týkající se používání tohoto přípravku nebo pokud máte nějaké potíže s nosním sprejem, požádejte o radu svého lékaře nebo lékárníka.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Avamys
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Alergické reakce: okamžitě kontaktujte svého lékaře
Alergické reakce na přípravek Avamys jsou vzácné a postihují méně než 1 z 1000 lidí. U malého počtu lidí se mohou alergické reakce vyvinout v závažnější, dokonce život ohrožující problém, pokud se neléčí. Příznaky zahrnují:
- sípání, kašel nebo potíže s dýcháním
- pocit náhlé slabosti nebo závratě (což může vést ke kolapsu nebo ztrátě vědomí)
- otok v obličeji
- vyrážka nebo zarudnutí.
V mnoha případech tyto příznaky budou signalizovat méně závažné vedlejší účinky. Měli byste si však být vědomi toho, že mohou být potenciálně závažné - pokud si tedy všimnete některého z těchto příznaků:
Navštivte lékaře co nejdříve.
Velmi časté nežádoucí účinky (mohou postihnout více než 1 z 10 lidí)
- Krvácení z nosu (obvykle mírné), zvláště pokud užíváte Avamys déle než 6 týdnů v řadě.
Časté nežádoucí účinky (mohou postihnout až 1 z 10 lidí)
- Ulcerace nosu - která může způsobit podráždění nebo nepohodlí v nose. Při smrkání můžete také vidět pruhy krve.
- Bolest hlavy
Méně časté nežádoucí účinky (mohou postihnout až 1 ze 100 lidí)
- Bolest, pálení, podráždění nebo suchost uvnitř nosu.
Neznámé nežádoucí účinky (frekvenci nelze z dostupných údajů určit)
- Zpomalení růstu u dětí.
- Dočasné změny vidění při dlouhodobém používání.
Nosní kortikosteroidy mohou změnit normální produkci steroidních hormonů ve vašem těle, zvláště pokud používáte vysoké dávky po dlouhou dobu. U dětí může tento vedlejší účinek způsobit, že rostou pomaleji než u ostatních.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi nebo zdravotní sestře. To se týká i všech možných nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. poskytnout více informací o bezpečnosti tohoto léku.
Expirace a retence
Uchovávejte tento přípravek mimo dohled a dosah dětí
Nejlepší je nosní sprej Avamys skladovat ve svislé poloze. Vždy držte víko.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na štítku a krabičce. Datum exspirace se vztahuje k poslednímu dni v měsíci. Po prvním použití by měl být nosní sprej Avamys použit do dvou měsíců.
Neskladujte Avamys v chladničce nebo mrazničce.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Složení a léková forma
Co Avamys obsahuje
Léčivou látkou je fluticasoni furoas. Každý potah přináší 27,5 mikrogramů flutikason -furoátu.
Dalšími složkami jsou bezvodá glukóza, dispergovatelná celulóza, polysorbát 80, benzalkoniumchlorid, dinátriumedetát, čištěná voda (viz bod 2).
Jak Avamys vypadá a obsah balení
Tento léčivý přípravek je nosní sprej ve formě bílé suspenze obsažené v lahvičce ze žlutého skla, vybavené dávkovací pumpou. Láhev je obsažena v téměř bílém plastovém inhalátoru se světle modrým víčkem a postranním tlačítkem, které aktivuje sprej.
Plastový inhalátor má okénko pro zobrazení obsahu lahve.
Avamys je k dispozici v balení po 30, 60 a 120 sprejích.
Na trhu nemusí být všechny velikosti balení.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
AVAMYS
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Každá aktivace poskytne 27,5 mcg fluticasoni furoátu.
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Nosní sprej, suspenze.
Odpružení bílé barvy.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Avamys je indikován u dospělých, dospívajících a dětí (6 let a starších).
Avamys je indikován k léčbě příznaků alergické rýmy.
04.2 Dávkování a způsob podání
Dávkování
Dospělí a mladiství (12 let a starší):
Doporučená počáteční dávka je dvě vdechnutí (27,5 mikrogramů flutikason -furoátu na každý vdech) do každé nosní dírky jednou denně (celková denní dávka 110 mikrogramů).
Jakmile je dosaženo adekvátní kontroly symptomů, může být pro udržovací terapii účinná dávka snížená na jeden vdech na nosní dírku (celková denní dávka 55 mcg).
Dávka by měla být titrována na nejnižší dávku, při které je zachována účinná kontrola symptomů.
Děti (6 až 11 let):
Doporučená počáteční dávka je jedna vdechnutí (27,5 mikrogramů flutikason -furoátu na každý vdech) do každé nosní dírky jednou denně (celková denní dávka 55 mikrogramů).
Pacienti, kteří nereagují adekvátně na dávku jednoho vdechnutí do každé nosní dírky jednou denně (celková denní dávka 55 mcg), mohou použít dvě vdechy do každé nosní dírky jednou denně (celková denní dávka 110 mcg).
Jakmile je dosaženo adekvátní kontroly symptomů, doporučuje se snížení dávky na jeden vdech na nosní dírku jednou denně (celková denní dávka 55 mcg).
Pro plný terapeutický prospěch se doporučuje pravidelné a plánované používání. Nástup terapeutické aktivity je pozorován od 8 hodin po prvním podání. K dosažení co největšího účinku však může být zapotřebí několikadenní léčba. Pacient by měl být informován, že při pravidelném používání se příznaky zlepší (viz bod 5.1) .Doba trvání léčby by měla být omezena na dobu odpovídající délce expozice alergenům.
Děti do 6 let:
Bezpečnost a účinnost přípravku Avamys u dětí mladších 6 let nebyla stanovena. V současné době jsou dostupné údaje popsány v bodech 5.1 a 5.2. Není však možné dávkování.
Starší pacienti: V této populaci není nutná úprava dávky (viz bod 5.2).
Selhání ledvin
V této populaci není nutná úprava dávky (viz bod 5.2).
Jaterní nedostatečnost
U pacientů s mírnou až středně těžkou poruchou funkce jater není nutná úprava dávky. U pacientů s těžkou poruchou funkce jater nejsou k dispozici žádné údaje. Při dávkování je nutná opatrnost u pacientů s těžkou jaterní insuficiencí, protože u pacientů s jaterní insuficiencí může být větší riziko systémových nežádoucích účinků spojených s kortikosteroidy (viz body 4.4 a 5.2).
Způsob podání
Avamys nosní sprej by měl být podáván pouze intranasálně
Před použitím inhalátor dobře protřepejte. Chcete -li aktivovat inhalátor, držte jej ve svislé poloze a stiskněte uvolňovací tlačítko alespoň 6krát, dokud se neobjeví jemná mlha. Pokud inhalátor ponecháte nezakrytý po dobu 5 dnů nebo jej nebudete používat 30 dní nebo déle, opakujte aktivační proces (uvolněte přibližně 6 obláčky, dokud není pozorována řídká mlha).
Po každém použití inhalátor očistěte a nasaďte víčko.
04.3 Kontraindikace
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Systémové účinky kortikosteroidů
Systémové účinky kortikosteroidů podávaných nazálně se mohou objevit zejména při vysokých dávkách podávaných po delší dobu. Tyto účinky jsou méně pravděpodobné než u léčby perorálními kortikosteroidy a mohou se u jednotlivých pacientů a mezi různými přípravky s kortikosteroidy lišit. Možné systémové účinky mohou zahrnovat Cushingův syndrom, cushingoidní aspekt, adrenální supresi, zpomalení růstu u dětí a dospívajících, kataraktu, glaukom a vzácněji řadu psychologických nebo behaviorálních účinků včetně psychomotorické hyperaktivity, poruch spánku, úzkosti, deprese nebo agrese (zejména u dětí ).
Léčba vyššími než doporučenými dávkami nazálních kortikosteroidů může mít za následek klinicky významnou adrenální supresi. Pokud existují důkazy o vyšších než doporučených dávkách, měla by být zvážena potřeba dalších systémových kortikosteroidů během období stresu nebo plánovaného chirurgického zákroku. Dávkování 110 mikrogramů flutikason-furoátu jednou denně nebylo spojeno s potlačením osy hypotalamus-hypofýza-nadledviny (HPA) u dospělých, dospívajících nebo pediatrických pacientů. Dávka intranazálního flutikason-furoátu by však měla být snížena, stejně jako u všech intranazálních kortikosteroidů „Celková systémová zátěž kortikosteroidy by měla být vzata v úvahu vždy, když je předepsáno více léčby kortikosteroidy současně.
Pokud existuje nějaký důvod domnívat se, že je narušena funkce nadledvin, je třeba věnovat zvláštní pozornost převedení pacientů ze systémové léčby steroidy na flutikason -furoát.
Poruchy zraku: Kortikosteroidy nasální nebo inhalační cestou mohou vést k rozvoji glaukomu a / nebo katarakty. U pacientů se změnou vidění nebo s anamnézou zvýšeného nitroočního tlaku, glaukomu a / nebo katarakty je proto nutné pečlivé sledování.
Zpoždění růstu
U dětí užívajících nosní kortikosteroidy v licencovaných dávkách byla hlášena retardace růstu. U dětí léčených flutikason -furoátem 110 mikrogramů denně po dobu 1 roku bylo pozorováno snížení rychlosti růstu (viz body 4.8 a 5.1). Děti by proto měly být léčeny nejnižší možnou účinnou dávkou pro adekvátní kontrolu symptomů. (viz bod 4.2). Doporučuje se pravidelné sledování růstu dětí, které jsou dlouhodobě léčeny intranazálními kortikosteroidy. Pokud je pozorován zpomalený růst, měla by být léčba znovu vyšetřena, aby se pokud možno snížila dávka intranazálního kortikosteroidu na minimální dávku, která umožňuje zachování účinné kontroly symptomů rýmy. Kromě toho by měla být zvážena potřeba odeslat pacienta ke specialistovi na dětského lékaře (viz bod 5.1).
Pacienti na terapii ritonavirem
Souběžné podávání ritonaviru se nedoporučuje kvůli riziku „zvýšené systémové expozice flutikason -furoátu (viz bod 4.5).
Pacienti s jaterní insuficiencí
Metabolismus přípravku Avamys je charakterizován rozsáhlým efektem prvního průchodu, proto je pravděpodobné, že se systémová expozice intranazálnímu flutikason -furoátu u pacientů se závažným onemocněním jater zvýší. To může vést ke zvýšené frekvenci systémových nežádoucích účinků (viz body 4.2 a 5.2) Při léčbě těchto pacientů se doporučuje opatrnost.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Interakce s inhibitory CYP3A4
Flutikason -furoát je rychle odstraňován rozsáhlým metabolizmem prvního průchodu zprostředkovaným cytochromem P450 3A4.
Na základě údajů získaných s jiným glukokortikoidem (flutikason-propionát), který je metabolizován CYP3A4, se současné podávání s ritonavirem nedoporučuje, protože existuje riziko zvýšené systémové expozice flutikason-furoátu.
Při současném podávání flutikason-furoátu a silných inhibitorů CYP3A4 se doporučuje opatrnost, protože nelze vyloučit zvýšení systémové expozice. Ve studii lékových interakcí mezi intranazálním flutikason-furoátem a ketokonazolem, silným inhibitorem CYP3A4, bylo pozorováno více subjektů s měřitelnými koncentracemi flutikason-furoátu ve skupině s ketokonazolem (6 z 20 subjektů) ve srovnání se skupinou s placebem (1 z 20 subjektů) .Toto malé zvýšení expozice nevedlo ke statisticky významnému rozdílu v 24hodinových sérových hladinách kortizolu mezi těmito dvěma skupinami (viz bod 4.4).
Údaje o indukci a inhibici enzymů naznačují, že neexistuje žádný teoretický základ pro predikci metabolických interakcí mezi flutikason -furoátem a cytochromem P450 zprostředkovaným metabolismem jiných sloučenin v klinicky relevantních dávkách podávaných intranasálně. Nebyly proto provedeny žádné klinické studie hodnotící interakce flutikason -furoátu s jinými léky.
04.6 Těhotenství a kojení
Těhotenství
Nejsou k dispozici dostatečné údaje o použití flutikason-furoátu u těhotných žen. Ve studiích na zvířatech bylo prokázáno, že glukokortikoidy způsobují malformace, jako je rozštěp patra a zpomalení nitroděložního růstu. Člověk, protože doporučené dávky pro intranasální použití mají za následek minimální systémovou expozici (viz. bod 5.2) Flutikason -furoát by měl být v těhotenství podáván pouze tehdy, pokud přínos pro matku převáží potenciální riziko pro plod nebo dítě.
Čas krmení
Není známo, zda se intranasálně podávaný flutikason -furoát vylučuje do lidského mléka. Podávání flutikason -furoátu kojícím ženám by mělo být zvažováno pouze tehdy, pokud je očekávaný přínos pro matku větší než jakékoli možné riziko pro dítě.
Plodnost
Nejsou k dispozici žádné údaje o fertilitě u lidí.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Avamys nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje.
04.8 Nežádoucí účinky
Souhrn bezpečnostního profilu Nejčastěji hlášenými nežádoucími účinky během léčby flutikason -furoátem jsou epistaxe, nazální ulcerace a bolest hlavy. Nejzávažnějšími vedlejšími účinky jsou vzácné případy reakcí z přecitlivělosti, včetně anafylaxe (méně než 1 případ z 1000 pacientů).
Tabulkový seznam nežádoucích účinků Ve studiích bezpečnosti a účinnosti bylo více než 2 700 pacientů léčeno flutikason -furoátem na sezónní a celoroční alergickou rýmu. Pediatrická expozice flutikasonu ve studiích bezpečnosti a účinnosti u sezónní a celoroční alergické rýmy zahrnovala 243 pacientů 12 až
K určení četnosti nežádoucích účinků byla použita data z velkých klinických studií.
Pro klasifikaci frekvencí byla přijata následující konvence:
Velmi časté ≥ 1/10; Časté ≥1 / 100 -
Popis vybraných nežádoucích účinků
Epistaxe
* Epistaxe byla obecně mírné až střední intenzity. U dospělých a dospívajících byl výskyt epistaxe vyšší při dlouhodobém užívání (déle než 6 týdnů) než při krátkodobém užívání (až 6 týdnů). Po 6 týdnech).
Systémové efekty
Po nasálních kortikosteroidech se mohou objevit systémové účinky, zvláště pokud jsou předepisovány ve vysokých dávkách po delší dobu (viz bod 4.4) U dětí užívajících nosní kortikosteroidy byla hlášena retardace růstu.
Pediatrická populace
Bezpečnost u dětí mladších 6 let nebyla dostatečně stanovena. Frekvence, typ a závažnost nežádoucích účinků pozorovaných u pediatrické populace jsou podobné jako u dospělé populace.
Epistaxe
* V pediatrických klinických studiích prováděných po dobu až 12 týdnů byl výskyt epistaxe podobný u pacientů léčených flutikason -furoátem a pacientů léčených placebem.
Zpoždění růstu
** V roční klinické studii hodnotící růst u dětí před pubertou, kteří dostávali 110 mcg flutikason-furoátu jednou denně, byl v rychlosti růstu ve srovnání s placebem pozorován průměrný léčebný rozdíl -0,27 cm za rok (viz Klinická účinnost a bezpečnost).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky, které se vyskytnou po registraci léčivého přípravku, je důležité. Umožňuje průběžné sledování poměru přínosů a rizik tohoto léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení. "Příloha V.
04.9 Předávkování
Ve studii biologické dostupnosti byly po dobu tří dnů podávány intranazální dávky až 2 640 mcg denně, přičemž nebyly pozorovány žádné nežádoucí systémové reakce (viz bod 5.2).
Akutní předávkování pravděpodobně nevyžaduje žádnou jinou terapii než sledování pacienta.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: nosní přípravky, kortikosteroidy.
ATC kód: R01AD12.
Mechanismus účinku:
Flutikason-furoát je syntetický trifluorovaný kortikosteroid, který má velmi vysokou afinitu ke glukokortikoidnímu receptoru a má silný protizánětlivý účinek.
Klinická účinnost a bezpečnost:
Sezónní alergická rýma u dospělých a dospívajících:
Ve srovnání s placebem nosní sprej flutikason -furoát 110 mcg jednou denně významně zlepšil nosní příznaky (včetně rýmy, ucpaného nosu, kýchání a svědění nosu) a oční příznaky (včetně svědění / pálení, slzení, dokonce i intenzivního slzení a zarudnutí očí). 4 studie. Účinnost byla udržována po dobu 24 hodin mezi jedním podáním a dalším podáním jednou denně.
Nástup terapeutického přínosu byl pozorován počínaje 8 hodin po prvním podání, přičemž další zlepšení byla pozorována několik dní poté.
Nosní sprej Fluticasone furoate významně zlepšil pacientům vnímání celkové odpovědi na terapii a kvalitu života související s nemocí (Rhinoconjunctivie Quality of Life Questionnaire - RQLQ) ve všech 4 studiích.
Celoroční alergická rýma u dospělých a dospívajících:
Nosní sprej flutikason -furoát 110 mcg jednou denně významně zlepšil nosní symptomy i vnímání pacientů celkovou reakcí na léčbu ve srovnání s placebem ve třech studiích.
V jedné studii nosní sprej flutikason-furoát 110 mcg jednou denně významně zlepšil oční symptomy i kvalitu života související s nemocí (RQLQ) ve srovnání s placebem.
Účinnost byla udržována po dobu 24 hodin mezi dávkami s dávkováním jednou denně.
Ve dvouleté studii hodnotící oční bezpečnost flutikason-furoátu (110 mikrogramů jednou denně intranazálně) byli dospělí a mladiství s celoroční alergickou rýmou léčeni flutikason-furoátem (n = 367) nebo placebem (n = 181). Primární výsledky [doba ke zvýšení zadní subkapsulární neprůhlednosti (≥ 0,3 od výchozí hodnoty v klasifikačním systému pro opacity čoček, verze III (stupeň LOCS III)) a doba ke zvýšení nitroočního tlaku (IOP; ≥ 7 mmHg ve srovnání s výchozím stavem)] nebyly statisticky významné mezi oběma skupinami. Zvýšení zadní subkapsulární opacity (≥ 0,3 oproti výchozímu stavu) bylo častější u subjektů léčených flutikason -furoátem 110 mcg [14 (4%)] ve srovnání s placebem [4 (2%)] a bylo přechodné v povaha pro deset subjektů ve skupině s flutikason -furoátem a dva subjekty ve skupině s placebem.Zvýšení nitroočního tlaku (≥ 7 mmHg oproti výchozímu stavu) bylo častější u subjektů léčených 110 mcg flutikason -furoátem: 7 (2%) pro flutikason -furoát 110 mcg jednou denně a 1 (a 104, 95% subjektů v obou léčebných skupinách mělo zadní hodnoty subkapsulární opacity v rozmezí ± 0,1 výchozích hodnot pro každé oko I a v týdnu 104 mělo ≤ 1% subjektů v obou léčebných skupinách zvýšení výchozí subkapsulární opacity o ≥ 0,3 oproti výchozímu stavu. V týdnech 52 a 104 měla většina subjektů (> 95%) hodnoty IOP v rozmezí ± 5 mmHg výchozí hodnoty. Zvýšení zadní subkapsulární opacity nebo IOP nebylo doprovázeno nežádoucími účinky katarakty nebo glaukomu.
Pediatrická populace:
Trvalá a sezónní alergická rýma u dětí:
Pediatrické dávkování je založeno na vyhodnocení údajů o účinnosti u pediatrické populace alergické rýmy.
U sezónní alergické rýmy se osvědčil nosní sprej flutikason -furoát 110 mcg jednou denně. V žádném koncovém bodě však nebyly pozorovány žádné významné rozdíly mezi nosním sprejem flutikason -furoátem 55 mcg jednou denně a placebem.
U celoroční alergické rýmy vykazoval nosní sprej flutikason -furoát 55 mcg jednou denně po dobu 4 týdnů léčby konzistentnější profil účinnosti než dávkování 110 mcg jednou denně po dobu 4 týdnů léčby.Post-hoc analýza provedená na stejné 6týdenní a 12týdenní studii a 6týdenní studii bezpečnosti na ose hypotalamus-hypofýza-nadledviny (HPA) podpořila účinnost podávaného nosního spreje fluticasoni furoate 110 mikrogramů. jednou denně.
6týdenní studie zkoumající účinek nosního spreje flutikason-furoát 110 mcg jednou denně na funkci nadledvin u dětí ve věku od 2 do 11 let neprokázala žádný významný účinek na profily kortizolu. Sérum po dobu 24 hodin ve srovnání s placebem.
Roční randomizovaná, dvojitě zaslepená, multicentrická, placebem kontrolovaná klinická studie s paralelními skupinami hodnotila účinek nosního spreje flutikason-furoát 110 mcg denně na rychlost růstu u 474 dětí před pubertou. (5 až 7,5 roku věk pro ženy a 5 až 8,5 let pro muže) se stadiometrem. Průměrná rychlost růstu během 52týdenního léčebného období byla pomalejší u pacientů léčených flutikason-furoátem (5,19 cm / rok) oproti placebu (5,46 cm / rok) Průměrný rozdíl v důsledku léčby byl -0,27 cm za rok [95% CI -0,48 až -0,06].
Trvalá a sezónní alergická rýma u dětí (do 6 let):
Byly provedeny studie bezpečnosti a účinnosti u sezónní i celoroční alergické rýmy u celkem 271 pacientů ve věku 2 až 5 let, z nichž 176 bylo vystaveno působení flutikasonu.
Bezpečnost a účinnost v této věkové skupině nebyla dobře stanovena.
05.2 Farmakokinetické vlastnosti
Vstřebávání
Flutikason -furoát podléhá neúplné absorpci a rozsáhlému first -pass metabolismu v játrech a střevě, což má za následek zanedbatelnou systémovou expozici. Intranazální podání 110 μg jednou denně obvykle nevede k měřitelným plazmatickým koncentracím (pg / ml) Absolutní biologická dostupnost intranasálně podávaného flutikason -furoátu je Po podání 110 mikrogramů by bylo systémově dostupných 0,50% jako méně než 1 mikrogram flutikason -furoátu (viz bod 4.9).
Rozdělení
Vazba flutikason -furoátu na plazmatické bílkoviny je větší než 99%. Flutikason-furoát je široce distribuován s distribučním objemem v ustáleném stavu v průměru 608 litrů.
Biotransformace
Flutikason-furoát se rychle vylučuje ze systémového oběhu (celková plazmatická clearance 58,7 l / h) především jaterním metabolismem na neaktivní metabolit 17β-karboxylové kyseliny (GW694301X), enzymem cytochromu P450 CYP3A4. Hydrolýzou S-fluormethylkarbothioátu funkce za vzniku metabolitu 17β-karboxylové kyseliny. Vzdělávání in vivo neukázaly štěpení furoátové části za vzniku flutikasonu.
Odstranění
K eliminaci dochází primárně fekální cestou po orálním a intravenózním podání, což svědčí o vylučování flutikason -furoátu a jeho metabolitů žlučí. Po intravenózním podání trvá poločas eliminační fáze v průměru 15,1 hodiny. Vylučování močí představuje přibližně 1%, respektive 2% orální a intravenózní dávky.
Pediatrická populace
Koncentrace flutikason -furoátu v krvi není u většiny pacientů kvantifikovatelná (
Senioři
Farmakokinetické údaje poskytl pouze malý počet starších pacientů (≥ 65 let, n = 23/872; 2,6%). Ve srovnání s mladší populací pacientů nebyl u starších osob vyšší výskyt pacientů s kvantifikovatelnými koncentracemi flutikason -furoátu.
Selhání ledvin
Po intranazálním podání není flutikason -furoát v moči zdravých dobrovolníků detekovatelný. Méně než 1% léčivé látky závislé na dávce se vylučuje močí, a proto se neočekává, že by renální insuficience interferovala s farmakokinetikou flutikason-furoátu.
Jaterní nedostatečnost
Nejsou k dispozici žádné údaje o intranazálním flutikasonu u pacientů s jaterní insuficiencí. Studie provedená u pacientů se středně těžkou jaterní insuficiencí léčených jednou dávkou 400 mikrogramů inhalovaných orálně vedla ke zvýšení Cmax (42%) a AUC0-∞ (172%) a mírnému snížení (v průměru 23%) kortizolu úrovně pacientů ve srovnání se zdravými subjekty. Na základě této studie se neočekává, že by očekávaná průměrná expozice 110 mikrogramů intranazálního flutikason -furoátu u pacientů se středně těžkou poruchou funkce jater vedla k potlačení kortizolu. Proto se neočekává, že by normální dávka pro dospělé měla za následek útlum kortizolu. relevantní účinek u pacientů se středně těžkou jaterní insuficiencí. Nejsou k dispozici žádné údaje o pacientech s těžkou jaterní insuficiencí. Expozice flutikason -furoátu v této populaci pacientů bude pravděpodobně dále zvýšena.
05.3 Předklinické údaje vztahující se k bezpečnosti
V obecných toxikologických studiích byly výsledky podobné výsledkům pozorovaným u jiných kortikosteroidů a jsou spojeny s "nadměrnou farmakologickou aktivitou. Tato zjištění pravděpodobně nejsou relevantní pro člověka, vzhledem k tomu, že doporučené nosní dávky vedou k" minimální systémové expozici. Při konvenčních testech genotoxicity nebyly pozorovány žádné genotoxické účinky flutikasonu. Ve dvouletých inhalačních studiích na myších a potkanech navíc nedošlo ke zvýšení výskytu nádorů souvisejících s léčbou.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Bezvodá glukóza
Dispergovatelná celulóza
Polysorbát 80
Benzalkoniumchlorid
Edetát dvojsodný
Čištěná voda
06.2 Neslučitelnost
Irelevantní.
06.3 Doba platnosti
3 roky.
Platnost: 2 měsíce od první aktivace.
06.4 Zvláštní opatření pro skladování
Neuchovávejte v chladničce ani nezmrazujte.
Skladujte ve svislé poloze. Vždy mějte čepici nasazenou.
06.5 Charakter vnitřního obalu a obsah balení
14,2 ml v lahvičce z jantarového skla (sklo) typu I nebo typu III vybavené dávkovací rozprašovací pumpou.
Tento léčivý přípravek je k dispozici ve třech baleních: lahvička s 30, 60 nebo 120 obaly.
Na trhu nemusí být všechny velikosti balení.
06.6 Návod k použití a zacházení
Žádné zvláštní pokyny k likvidaci.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Glaxo Group Ltd
980 Great West Road, Brentford, Middlesex, TW8 9GS
Spojené království
08.0 REGISTRAČNÍ ČÍSLO
EU/1/07/434/001
038343012
EU/1/07/434/002
038343024
EU/1/07/434/003
038343036
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Datum první registrace: 11. ledna 2008
Datum posledního obnovení: 11. ledna 2013
10.0 DATUM REVIZE TEXTU
Duben 2014