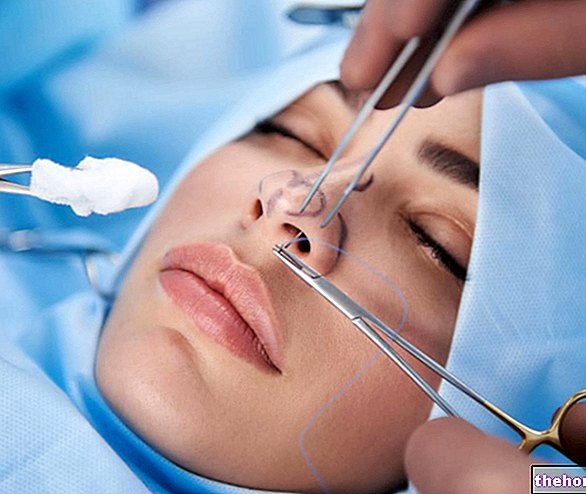
Účinné látky: botulotoxin typu A
BOTOX® 100 Allergan Units, prášek pro injekční roztok
BOTOX® 200 Allergan Units, prášek pro injekční roztok
Proč se používá Botox? K čemu to je?
Co je BOTOX
BOTOX je lék uvolňující svaly, který se vstřikuje do svalů, stěny močového měchýře nebo pod kůži. Funguje tak, že částečně blokuje nervové impulsy v každém svalu, kam se vstřikuje, a snižuje nadměrné kontrakce těchto svalů.
Když je BOTOX injekčně aplikován pod kůži, působí na potní žlázy, aby snížil množství produkovaného potu.
Při injekci do stěny močového měchýře působí BOTOX na muskulaturu močového měchýře, aby se snížila ztráta moči (inkontinence moči). Předpokládá se, že v případě chronické migrény je BOTOX schopen blokovat signály bolesti, které nepřímo blokují rozvoj migrény. Jak však BOTOX funguje u chronické migrény, nebylo zcela objasněno.
K čemu je BOTOX
U dospělých se přípravek BOTOX používá k ovládání:
- trvalé svalové křeče v očních víčkách a obličeji
- trvalé svalové křeče na krku a ramenou
- trvalé svalové křeče v zápěstí a ruce u pacientů s mrtvicí
- nadměrné pocení podpaží, které narušuje běžné denní činnosti, když jiná místní léčba nepomáhá
- hyperaktivní močový měchýř s inkontinencí moči - náhlé nutkání vyprázdnit močový měchýř a nutnost chodit na toaletu častěji než obvykle - když jiné léky (nazývané anticholinergika) nepomohly
- inkontinence moči v důsledku poruch močového měchýře spojených s poraněním míchy nebo roztroušenou sklerózou.
BOTOX se používá ke snížení příznaků chronické migrény u dospělých:
- s bolestí hlavy po dobu 15 dnů nebo více za měsíc, z toho nejméně 8 dní s migrénou a kteří neměli adekvátní odpověď nebo netolerují léky proti migréně podávané k profylaxi.
Chronická migréna je onemocnění postihující nervový systém. Pacienti obvykle trpí bolestmi hlavy často doprovázenými nadměrnou citlivostí na světlo, hlasitými zvuky nebo vůněmi / pachy, ale také nevolností a / nebo zvracením. Hlava se vyskytuje po dobu 15 dnů nebo déle měsíc Bylo prokázáno, že BOTOX významně snižuje příznaky a zlepšuje kvalitu života pacientů trpících chronickou migrénou.
BOTOX by vám měl předepsat pouze tehdy, pokud vám byla diagnostikována chronická migréna neurologem, který se na tento obor specializuje. BOTOX by měl být podáván pod dohledem neurologa. BOTOX se nepoužívá k akutní migréně, chronickým tenzním bolestem hlavy nebo u pacientů s bolestmi hlavy z nadužívání drog.
U dětí ve věku 2 let a starších s dětskou mozkovou obrnou, které nemohou chodit, se přípravek BOTOX používá k ovládání:
- deformace chodidla způsobená přetrvávajícími křečemi svalů nohou. BOTOX uvolňuje trvalé svalové křeče v nohou.
Kontraindikace Kdy by neměl být použit Botox
Nepoužívejte BOTOX
- jestliže jste alergický / á (přecitlivělý / á) na botulotoxin typu A nebo na kteroukoli další složku přípravku BOTOX;
- pokud máte navrhovanou „infekci v místě vpichu“;
- pokud se léčíte s močovou inkontinencí a vyvine se u vás „infekce močových cest nebo se u vás objeví“ náhlá neschopnost vyprázdnit močový měchýř (a pravidelně nepoužíváte katétr);
- pokud se léčíte s močovou inkontinencí a nehodláte v případě potřeby použít katétr.
Zvláštní pozornost věnujte přípravku BOTOX
Před použitím BOTOX
Informujte svého lékaře, pokud:
- měli v minulosti problémy s injekcemi (například mdloby);
- máte zánět ve svalech nebo v oblasti kůže, kam lékař hodlá podat injekci;
- máte výraznou slabost nebo ztrátu svalového tonusu, kam lékař zamýšlí aplikovat;
- jste někdy měl (a) problémy s polykáním nebo s jídlem nebo tekutinami, které se náhodně dostaly do plic, zvláště pokud se léčíte s trvalými svalovými křečemi v oblasti krku a ramen;
- trpíte jakýmikoli jinými svalovými problémy nebo chronickými onemocněními postihujícími svaly (jako je myasthenia gravis nebo Eaton Lambertův syndrom);
- trpí určitými chorobami nervového systému (jako je amyotrofická laterální skleróza nebo motorická neuropatie);
- máte oční onemocnění zvané glaukom s uzavřeným úhlem (vysoký nitrooční tlak) nebo vám bylo sděleno, že máte riziko vzniku tohoto typu glaukomu;
- podstoupili jakoukoli operaci nebo zranění, které mohlo jakýmkoli způsobem změnit sval, který má být injekčně podán;
- je léčen pro hyperaktivní močový měchýř s inkontinencí moči a je to muž, který má známky a příznaky obstrukce moči, jako jsou potíže s močením nebo slabý nebo přerušovaný průtok
Po ošetření přípravkem BOTOX
Kontaktujte svého lékaře a okamžitě vyhledejte lékařskou pomoc, pokud dojde k následujícímu:
- potíže s dýcháním, polykáním nebo schopností mluvit;
- kopřivka, otok včetně otoku obličeje nebo hrdla, sípání, pocit na omdlení a dušnost (možné příznaky závažné alergické reakce).
Opatření pro použití Co potřebujete vědět, než začnete užívat Botox
Pokud jste léčeni přípravkem BOTOX příliš často nebo je dávka příliš vysoká, může vaše tělo začít vytvářet protilátky, které mohou účinek přípravku BOTOX snížit.
Pokud jste delší dobu před léčbou přípravkem BOTOX nepraktikovali mnoho fyzických aktivit, měla by být jakákoli aktivita postupně po ošetření obnovena.
Tento lék pravděpodobně nezlepší stupeň pohybu v kloubech, kde okolní sval ztratil schopnost se natáhnout.
Pokud se přípravek BOTOX používá k léčbě trvalých křečí očních víček, může snížit mrkání a poškodit povrch očí. Aby se tomu zabránilo, může být nutné ošetření očními kapkami, očními mastmi, měkkými kontaktními čočkami nebo dokonce ochrannými prostředky. chránit oko. Váš lékař vám řekne, zda je to nutné.
Pokud používáte BOTOX ke kontrole ztráty moči, bude vám lékař muset před a po léčbě nasadit antibiotika, aby se předešlo infekcím močových cest.
Pokud jste před injekcí nepoužili katétr, lékař vás uvidí asi 2 týdny po injekci. Budete požádáni, abyste se tam vymočili a celkový objem moči zbývající v močovém měchýři se poté změří ultrazvukem. Váš lékař rozhodne, zda se budete během následujících 12 týdnů muset vrátit ke stejnému testu. Poraďte se svým lékařem, pokud nemůžete kdykoli močit, protože možná budete muset začít používat katétr. U pacientů s močovou inkontinencí způsobenou poruchami močového měchýře spojenými s poraněním míchy nebo roztroušenou sklerózou bude přibližně třetina pacientů, kteří před léčbou nepoužili katétr, muset použít katétr po léčbě. U pacientů s inkontinencí moči v důsledku hyperaktivního močového měchýře bude asi 6 ze 100 pacientů muset po léčbě použít katétr.
Interakce Jaké léky nebo potraviny mohou ovlivnit účinek Botoxu
Informujte svého lékaře nebo lékárníka, pokud:
- užíváte antibiotika (používaná k léčbě infekcí), anticholinesterázová léčiva, léky na srdeční rytmus nebo svalové relaxanci. Některé z těchto léků mohou zvýšit účinek přípravku BOTOX.
- nedávno jste byl léčen léčivým přípravkem obsahujícím botulotoxin (účinná látka v přípravku BOTOX), protože to může výrazně zvýšit účinek přípravku BOTOX.
- používá jakékoli protidestičkové činidlo (produkty podobné aspirinu) a / nebo antikoagulancia (ředidla krve).
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte nebo jste v nedávné době užíval, a to i o lécích, které jsou dostupné bez lékařského předpisu.
Varování Je důležité vědět, že:
Těhotenství a kojení
BOTOX by neměl být používán během těhotenství a u žen ve fertilním věku, které nepoužívají antikoncepci, pokud to není nezbytně nutné. Pokud jste těhotná, plánujete otěhotnět nebo otěhotníte během léčby, požádejte svého lékaře o radu. Váš lékař s vámi prodiskutuje, zda byste měli v léčbě pokračovat.
BOTOX se nedoporučuje kojícím ženám.
Před užitím jakéhokoli léku se poraďte se svým lékařem nebo lékárníkem.
Řízení dopravních prostředků a obsluha strojů
BOTOX může způsobit závratě, ospalost, únavu nebo problémy se zrakem. Pokud se u vás vyskytl některý z těchto účinků, neřiďte dopravní prostředky ani neobsluhujte stroje. Pokud si nejste jisti, požádejte o radu svého lékaře.
Dávka, způsob a doba podání Jak používat Botox: Dávkování
BOTOX by měli injekčně podávat pouze lékaři se specifickými dovednostmi, jak tento lék používat.
Způsob a cesta podání
BOTOX se vstřikuje do svalů (intramuskulárně), do stěny močového měchýře pomocí specifického nástroje (cystoskop) pro injekci do močového měchýře nebo do kůže (intradermálně). Injektuje se přímo do postižené oblasti; Váš lékař obvykle aplikuje přípravek BOTOX na několik míst v každé postižené oblasti.
Obecné informace o dávkování
- Počet injekcí na sval a dávka se liší podle indikací. Váš lékař však rozhodne, v jakém množství, jak často a do jakých svalů si injekci přípravku BOTOX podáte. Doporučuje se, aby lékař použil nejnižší účinnou dávku.
- Dávkování pro starší osoby je stejné jako pro dospělé.
Dávka přípravku BOTOX a doba jeho účinku se liší podle poruchy, se kterou se léčíte. Podrobnosti o každé poruše jsou uvedeny níže.
Bezpečnost a účinnost přípravku BOTOX při léčbě přetrvávajících svalových křečí očních víček, obličeje, krku a ramen u dětí (do 12 let) nebyla prokázána.Bezpečnost a účinnost přípravku BOTOX při léčbě chronické migrény u dětí (do 18 let) nebyly studovány.
Bezpečnost a účinnost přípravku BOTOX při léčbě nadměrného pocení v podpaží nebyla studována u dětí mladších 12 let. Zkušenosti s používáním přípravku BOTOX v léčbě nadměrného pocení v podpaží u dospívajících ve věku od 12 do 17 let jsou velmi omezené.
Účinnost přípravku BOTOX v této věkové skupině nebyla potvrzena. Pro více informací kontaktujte svého lékaře.
Bezpečnost a účinnost přípravku BOTOX při léčbě spasticity horní končetiny související s cévní mozkovou příhodou nebyla u dětí a dospívajících mladších 18 let stanovena.
Bezpečnost a účinnost přípravku BOTOX při léčbě inkontinence moči u pediatrických pacientů mladších 18 let nebyla stanovena.
Pro trvalé svalové křeče očních víček a obličeje
Dávkování
V první léčebné relaci může lékař provést více injekcí do postižených svalů 1,25 až 2,5 jednotek BOTOXu do každého místa vpichu.
Maximální dávka pro první ošetření je 25 jednotek na postiženou oblast (např. Na oko). V případě dalších léčebných sezení lze maximální celkovou dávku v případě potřeby zvýšit až na 100 jednotek.
Trvání účinku léčby
Zlepšení obvykle uvidíte do 3 dnů po injekci. Maximální účinek je obvykle zaznamenán 1 až 2 týdny po léčbě.
Když účinek začne mizet, lze léčbu v případě potřeby opakovat, ne však častěji než každé 3 měsíce.
Pro trvalé svalové křeče krku a ramen
Dávkování
Lékař může provést více injekcí do postižených svalů až 50 jednotek BOTOXu pro každé místo vpichu.
Maximální dávka pro první ošetření je 200 jednotek. U následných léčebných sezení lze maximální dávku zvýšit až na 300 jednotek.
Trvání účinku léčby
Zlepšení obvykle uvidíte do 2 týdnů po injekci.
Maximální účinek je obvykle zaznamenán přibližně 6 týdnů po léčbě.
Když účinek začne odeznívat, lze léčbu v případě potřeby opakovat, ale ne častěji než každých 10 týdnů.
Pro trvalé svalové křeče zápěstí a rukou u pacientů s mrtvicí
Dávkování
Lékař může provést více injekcí do postižených svalů. Dávka a počet injekcí se liší v závislosti na řadě faktorů, včetně vašich potřeb, svalů, které mají být léčeny, velikosti svalů, závažnosti křečí atd.
Trvání účinku léčby
Zlepšení obvykle uvidíte během prvních 2 týdnů po injekci.
Maximální účinek je obvykle zaznamenán mezi 4 a 6 týdny po léčbě.
Když účinek začne odeznívat, lze léčbu v případě potřeby opakovat, ale ne častěji než každých 12 týdnů.
Pro nadměrné pocení podpaží
Dávkování
Váš lékař může podat injekci BOTOXU na více míst v oblasti podpaží.Celková dávka na podpaží je 50 jednotek BOTOXu.
Trvání účinku léčby
Zlepšení obvykle uvidíte během prvního týdne po injekci.
Účinek obvykle trvá v průměru 7,5 měsíce po první injekci a přibližně 1 ze 4 pacientů stále vykazuje léčebný účinek po jednom roce.
Když účinek začne mizet, lze léčbu v případě potřeby opakovat, ale ne častěji než každých 16 týdnů.
Pro trvalé křeče svalů nohou u dětí s dětskou mozkovou obrnou
Dávkování
Lékař může provést více injekcí do postižených svalů. Dávka bude záviset na hmotnosti dítěte.
Trvání účinku léčby
Zlepšení obvykle uvidíte během prvních 2 týdnů po injekci.
Když účinek začne mizet, je možné opakovat následnou léčbu, ne však častěji než každé 3 měsíce. Lékař může najít dávku, která ospravedlňuje ošetření až s odstupem 6 měsíců.
Pro inkontinenci moči v důsledku hyperaktivního močového měchýře
Dávkování
Lékař provede několik injekcí do stěny močového měchýře. Celková dávka je 100 jednotek BOTOXu. Před injekcemi vám může být podáno lokální anestetikum (váš močový měchýř bude na chvíli naplněn anestetickým roztokem a poté vyprázdněn.) Můžete také dostat sedativum.
Budete muset počkat 30 minut po léčbě, abyste zjistili, zda jste schopni spontánně močit.
Trvání účinku léčby
Během prvních 2 týdnů po injekci obvykle dojde ke zlepšení.
Účinek obecně trvá 5 - 6 měsíců po injekci.
Pokud účinky začnou odeznívat, můžete se v případě potřeby vrátit k léčbě, ale ne častěji než každé 3 měsíce.
Pro inkontinenci moči v důsledku poruch močového měchýře spojených s poraněním míchy nebo roztroušenou sklerózou
Dávkování
Lékař provede několik injekcí do stěny močového měchýře. Celková dávka je 200 jednotek BOTOXU. Před injekcí vám může být podáno lokální nebo celkové anestetikum. Můžete také dostat sedativa.
Trvání terapeutického účinku
Zlepšení obvykle uvidíte do 2 týdnů po injekci.
Účinek obecně trvá 8–10 měsíců po injekci.
Když účinky začnou odeznívat, můžete se v případě potřeby vrátit k léčbě, ale ne častěji než každé 3 měsíce.
K léčbě bolesti hlavy u dospělých trpících chronickou migrénou
Dávkování
Váš lékař může podat více injekcí do určitých svalů obličeje, hlavy a krku až do 5 jednotek přípravku BOTOX do každého místa vpichu. Injekce by měly být rozprostřeny do 7 specifických svalových oblastí hlavy / krku s polovičním počtem injekcí podaných vlevo a polovinou na pravou stranu hlavy a krku.
Celkový rozsah dávky je mezi 155 a 195 jednotkami na jedno ošetření.
Trvání účinku léčby
Když účinek začne mizet, lze léčbu opakovat, ale ne častěji než každých 12 týdnů.
Předávkování Co dělat, pokud jste užili příliš mnoho Botoxu
Známky předávkování přípravkem BOTOX se nemusí objevit několik dní po injekci. Pokud jste přípravek BOTOX spolkli nebo omylem aplikovali, měli byste kontaktovat svého lékaře, který vás může několik týdnů sledovat.
Pokud jste dostali předávkování přípravkem BOTOX, můžete mít některé z následujících příznaků, a pokud ano, okamžitě kontaktujte svého lékaře, který rozhodne, zda jít do nemocnice:
- potíže s dýcháním, polykáním nebo mluvením v důsledku svalové paralýzy;
- potraviny nebo kapaliny náhodně přicházející do styku s plícemi, které mohou způsobit zápal plic (infekce plic) v důsledku svalové paralýzy;
- pokles víček, dvojité vidění;
- obecná slabost.
Máte -li jakékoli další otázky týkající se používání přípravku BOTOX, zeptejte se svého lékaře nebo lékárníka.
Nežádoucí účinky Jaké jsou vedlejší účinky Botoxu
Podobně jako všechny léky, může mít i BOTOX nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Obecně se nežádoucí účinky objevují během prvních dnů po léčbě. Ty obvykle trvají jen krátce, ale mohou trvat několik měsíců a ve vzácných případech i déle.
POKUD MÁTE JAKÉKOLI OBTÍŽNOSTI V DECHOVÁNÍ, POŽÍVÁNÍ NEBO ŘEČENÍ PO PŘIJETÍ OŠETŘENÍ BOTOXEM, OKAMŽITĚ KONTAKTUJTE SVÉHO LÉKAŘE.
Pokud se u vás objeví kopřivka, otok včetně otoku obličeje nebo hrdla, sípání, pocit na omdlení a dušnost, okamžitě kontaktujte svého lékaře.
Nežádoucí účinky jsou zařazeny do následujících kategorií v závislosti na tom, jak často se vyskytují:
Níže jsou uvedeny vedlejší účinky, které se liší v závislosti na části těla, do které se injekčně aplikuje BOTOX:
Injekce do víčka a obličeje
Velmi častý nežádoucí účinek:
- poklesnutí víčka.
Časté nežádoucí účinky:
- otok obličeje;
- lokalizované poškození rohovky (čistý povrch pokrývající přední část oka);
- potíže s úplným zavřením oka;
- nadměrné trhání;
- podráždění;
- suché oko, podráždění očí a citlivost na světlo;
- modřiny pod kůží.
Méně časté nežádoucí účinky:
- závrať;
- poruchy vidění;
- rozmazané vidění;
- dvojité vidění;
- únava;
- zánět rohovky (čistý povrch pokrývající přední část oka);
- slabost obličejových svalů;
- uvolnění svalů jedné strany obličeje;
- vyrážka;
- abnormální pohyb očních víček dovnitř nebo ven.
Vzácný nežádoucí účinek:
- otok víčka.
Velmi vzácné nežádoucí účinky:
- vřed, poškození rohovky (čistý povrch pokrývající přední část oka);
- vysoký tlak v oku.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Injekce do krku a ramene
Velmi časté nežádoucí účinky:
- potíže s polykáním;
- bolest;
- svalová slabost.
Časté nežádoucí účinky:
- závrať;
- chřipkový syndrom;
- ospalost
- svalové křeče;
- snížená citlivost kůže;
- pocit slabosti;
- pocit obecné malátnosti;
- pocit nevolnosti;
- bolest hlavy;
- ztuhlost nebo bolestivost svalů;
- otok a podráždění horních cest dýchacích (rýma);
- ucpaný nos nebo rýma, kašel, bolest v krku, lechtání nebo podráždění hrdla;
- suchá ústa.
Méně časté nežádoucí účinky:
- dušnost;
- dvojité vidění;
- horečka;
- pokles víčka;
- změna hlasu.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Injekce do zápěstí a ruky u pacientů s mrtvicí
Časté nežádoucí účinky:
- svalová slabost;
- zvýšené svalové napětí;
- podlitiny a krvácení pod kůží způsobující červené oblasti (modřiny nebo purpura);
- krvácení nebo pálení v místě vpichu;
- bolest v rukou a prstech;
- bolest v místě podání injekce;
- horečka;
- chřipkový syndrom.
Méně časté nežádoucí účinky:
- Deprese;
- pokles krevního tlaku ve stoje, který způsobuje závratě, točení hlavy nebo mdloby;
- pocit závratě nebo 'točení' (vertigo);
- nedostatečná koordinace pohybů;
- ztráta paměti;
- generalizovaná slabost;
- bolest;
- bolest nebo zánět kloubů;
- snížená citlivost kůže;
- necitlivost nebo brnění;
- otoky končetin, jako jsou ruce a nohy;
- zánět kůže (dermatitida);
- bolest hlavy;
- pocit obecné nevolnosti;
- pocit nevolnosti;
- zvýšená citlivost v místě vpichu;
- vyrážka;
- necitlivost nebo brnění kolem úst;
- potíže se spánkem (nespavost);
- svědění.
Některé z těchto neobvyklých vedlejších účinků mohou také souviset s vaší nemocí.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Injekce na nadměrné pocení podpaží
Velmi časté nežádoucí účinky:
- bolest v místě vpichu.
Časté nežádoucí účinky:
- bolest v místě vpichu;
- bolest hlavy;
- necitlivost nebo brnění;
- návaly horka;
- zvýšené pocení jinde než v podpaží;
- neobvyklý zápach kůže;
- svědění;
- ztráta vlasů;
- otok pod kůží;
- bolest v končetinách, jako jsou ruce a prsty;
- bolest;
- reakce a otoky, krvácení nebo pálení a zvýšená citlivost v místě vpichu.
Méně časté nežádoucí účinky:
- svalová slabost;
- pocit slabosti;
- svalová bolest;
- problémy s klouby;
- pocit nevolnosti
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Injekce nohou u dětí s dětskou mozkovou obrnou
Velmi časté nežádoucí účinky:
- virová infekce;
- ušní infekce.
Časté nežádoucí účinky:
- ospalost;
- svalová slabost;
- bolest v končetinách, jako jsou ruce a prsty;
- problémy s chůzí;
- necitlivost nebo brnění;
- svalová bolest;
- inkontinence moči (neschopnost kontrolovat vyprazdňování močového měchýře);
- pocit obecné malátnosti;
- pády;
- vyrážka;
- bolest v místě vpichu;
- pocit slabosti.
Po léčbě přípravkem BOTOX byly vzácně hlášeny úmrtí někdy spojené s aspirační pneumonií u dětí s dětskou mozkovou obrnou.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Injekce do stěny močového měchýře pro inkontinenci moči v důsledku hyperaktivního močového měchýře
Velmi časté nežádoucí účinky:
- infekce močového ústrojí;
- bolestivé močení po injekci *.
Časté nežádoucí účinky:
- bakterie v moči, bílé krvinky v moči;
- neschopnost vyprázdnit močový měchýř (zadržování moči);
- neúplné vyprázdnění močového měchýře;
- časté močení během dne;
- krev v moči po injekci **.
* Tento vedlejší účinek může také souviset s injekčním postupem. ** Tento vedlejší účinek se týká pouze injekčního postupu
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Injekce do stěny močového měchýře pro inkontinenci moči v důsledku poruch močového měchýře spojených s poraněním míchy nebo roztroušenou sklerózou
Velmi časté nežádoucí účinky:
- infekce močového ústrojí;
- neschopnost vyprázdnit močový měchýř (zadržování moči).
Časté nežádoucí účinky:
- potíže s usínáním (nespavost);
- zácpa;
- svalová slabost;
- svalové křeče;
- krev v moči po injekcích *;
- bolestivé močení po injekcích *;
- otok ve stěně močového měchýře (divertikulum močového měchýře);
- únava;
- problémy s chůzí (poruchy chůze);
- možná nekontrolovaná reflexní reakce těla (jako silné pocení, pulzující bolest hlavy nebo zvýšený puls) přibližně ve spojení s injekcemi (autonomní dysreflexie) *;
- padá.
* Některé z těchto běžných nežádoucích účinků mohou také souviset s injekčním postupem.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Injekce do hlavy a krku k léčbě bolesti hlavy u pacientů trpících chronickou migrénou
Časté nežádoucí účinky:
- bolest hlavy;
- migréna;
- vyrážka;
- svědění;
- bolest v místě vpichu;
- bolest krku;
- slabost obličejových svalů;
- pokles víčka;
- svalová slabost;
- svalová bolest;
- svalové křeče;
- bolest svalů;
- svalová ztuhlost.
Méně časté nežádoucí účinky:
- potíže s polykáním;
- bolest kůže;
- bolest v čelisti;
- otok očních víček.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Obecné informace o dalších vedlejších účincích
Nežádoucí účinky související s šířením BOTOXU vzdáleným od místa vpichu byly hlášeny velmi vzácně a zahrnují:
- svalová slabost;
- zácpa;
- potíže s polykáním;
- náhodný průchod jídla nebo tekutin do plic, který v některých případech může způsobit zápal plic.
Obtížné polykání se může pohybovat od mírných až po těžké a v některých případech vyžaduje léčbu. Ve vzácných případech lidé zemřeli kvůli obtížnému polykání.
Vzácně byly hlášeny srdeční nežádoucí účinky:
- nepravidelný srdeční tep;
- infarkty.
Někteří z těchto lidí zemřeli. Někteří z těchto pacientů však již měli problémy se srdcem.
Vzácně byly hlášeny závažné nebo okamžité alergické reakce, včetně:
- kopřivka;
- otok včetně otoku obličeje nebo hrdla;
- chrastítko;
- pocit na omdlení;
- dušnost.
Případy
- záchvaty nebo křeče po léčbě přípravkem BOTOX, zejména u pacientů, u kterých se tyto příznaky dříve vyskytly. Tyto účinky se objevily hlavně tehdy, když byl přípravek BOTOX použit k léčbě přetrvávajících křečí svalů nohou u dětí s dětskou mozkovou obrnou.
Jako u každé injekce mohou být hlášeny nežádoucí účinky související s inokulem:
- bolest, podlitiny, krvácení nebo infekce v místě vpichu;
- necitlivost nebo brnění;
- snížená citlivost kůže;
- bolestivost;
- otok / otok;
- erytém (zarudnutí);
- teplo krevního tlaku a mdloby způsobené bolestí a / nebo „úzkostí“ jehly. Po injekci přípravku BOTOX měli pacienti také:
- horečka a příznaky podobné chřipce.
Následující seznam uvádí další nežádoucí účinky hlášené při používání přípravku BOTOX, který se používá pro jakýkoli zdravotní stav, protože byl uveden na trh:
- alergická reakce;
- ztráta inervace / kontrakce injekčního svalu;
- dýchací potíže a / nebo respirační selhání;
- aspirační pneumonie (zánět plic způsobený náhodným vdechnutím jídla, pití, slin nebo zvratků);
- chronické svalové onemocnění (myasthenia gravis);
- rozmazané vidění;
- potíže s jasným viděním;
- strabismus;
- mdloby;
- bolest / necitlivost / nebo slabost začínající v páteři;
- pád svalů postihující část obličeje;
- slabost obličejových svalů;
- potíže s pohybem paží a ramen;
- snížená citlivost kůže;
- svalová bolest;
- bolest břicha;
- průjem, zvracení, ztráta chuti k jídlu;
- horečka;
- různé druhy červených skvrnitých vyrážek;
- pocit obecné nevolnosti;
- potíže s mluvením;
- svědění;
- Nadměrné pocení;
- ztráta vlasů;
- snížený sluch;
- zvonění v uchu;
- pocit závratě nebo 'točení' (vertigo);
- necitlivost nebo brnění.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Expirace a retence
Uchovávejte BOTOX mimo dosah a dohled dětí.
Váš lékař by neměl používat přípravek BOTOX po uplynutí doby použitelnosti, uvedené na štítku za EXP. Datum exspirace se vztahuje k poslednímu dni v měsíci.
Uchovávejte v chladničce (2 ° C - 8 ° C) nebo v mrazničce (-5 ° C nebo nižší).
Po rekonstituci se doporučuje okamžité použití roztoku; přípravek však lze uchovávat až 24 hodin v chladničce (2 ° C - 8 ° C).
Složení a léková forma
Co přípravek BOTOX obsahuje
- Léčivou látkou je: Clostridium botulinum botulotoxin typu A. Jedna lahvička obsahuje 50, 100 nebo 200 Allerganových jednotek botulotoxinu typu A.
- Dalšími složkami jsou lidský albumin a chlorid sodný.
Popis vzhledu BOTOXu a obsahu balení
BOTOX je dodáván jako bílý prášek v lahvičce z čirého skla. Před injekcí musí být přípravek rekonstituován ve sterilním injekčním roztoku chloridu sodného 9 mg / ml (0,9%).
Balení může obsahovat 1, 2, 3 a 6 lahviček. Kromě toho je v baleních po 10 lahvičkách také BOTOX 50 a 100 Allergan jednotek botulotoxinu typu A.
Na trhu nemusí být všechny velikosti balení.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Chcete-li mít přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
BOTOX 100 UNITS ALLERGAN PRÁŠEK PRO INJEKČNÍ ŘEŠENÍ
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Botulotoxin * typ A, 100 jednotek Allergan v lahvičce.
* z Clostridium botulinum
Jednotky botulotoxinu nejsou zaměnitelné z jednoho produktu na druhý.
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Prášek pro injekční roztok.
Bílý prášek.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
BOTOX je indikován k léčbě:
• blefarospasmus, hemifaciální křeč a související fokální dystonie;
• cervikální dystonie (křečovitá torticollis);
• fokální spasticita:
- spojené s dynamickou deformitou chodidla v důsledku spasticity u dětských pacientů s dětskou mozkovou obrnou ve věku dvou let nebo starších;
- zápěstí a ruky u dospělých pacientů s mrtvicí.
• Trvalá a závažná primární hyperhidróza podpaží, která narušuje běžné denní činnosti a je odolná vůči topické léčbě.
• Inkontinence moči u dospělých pacientů s neurogenní hyperaktivitou detrusorového svalu močového měchýře způsobenou stabilizovanou lézí míchy od cervikální oblasti až po nižší úrovně nebo s roztroušenou sklerózou.
• Úleva od symptomů u dospělých pacientů, kteří splňují diagnostická kritéria pro chronickou migrénu (bolesti hlavy trvající ≥ 15 dní v měsíci, včetně migrény alespoň 8 dní) a u nichž byla prokázána nedostatečná odpověď nebo netolerují léky na profylaxi migrény (viz bod 4.4) .
04.2 Dávkování a způsob podání
Dávkování
Přečtěte si prosím konkrétní doporučení pro každou indikaci popsanou níže.
Jednotky botulotoxinu nejsou vzájemně zaměnitelné. Doporučené dávky v jednotkách Allergan se liší od dávek jiných přípravků z botulotoxinu.
Následující informace jsou důležité: Pokud se při stejném ošetření používají balení s různou silou BOTOXU, věnujte zvláštní pozornost použití správného množství ředidla k rekonstituci konkrétního počtu jednotek na 0,1 ml. Množství ředidla se pohybuje mezi 50 Allergan Units BOTOX, 100 Allergan Units BOTOX a Allergan Units BOTOX 200. Každá stříkačka musí být řádně označena.
BOTOX by měl být rekonstituován pouze sterilním injekčním roztokem chloridu sodného 9 mg / ml (0,9%). Správné množství ředidla musí být nataženo injekční stříkačkou (viz tabulka ředění níže).
Pokyny k ředění 100 injekčních lahviček pro inkontinenci moči v důsledku neurogenní hyperaktivity detrusorového svalu močového měchýře:
• Rekonstituujte dvě 100 jednotkové lahvičky přípravku BOTOX se 6 ml 0,9% nekonzervovaného fyziologického roztoku a lahvičku jemně promíchejte.
• Z každé lahvičky natáhněte 4 ml pomocí dvou různých 10ml stříkaček.
• Z každé lahvičky natáhněte zbývající 2 ml pomocí třetí 10ml stříkačky.
• rekonstituci dokončete přidáním 6 ml 0,9% fyziologického roztoku bez konzervačních látek do každé ze 10 ml injekčních stříkaček a jemně promíchejte.
Získáte tři 10ml stříkačky obsahující celkem 200 jednotek rekonstituovaného BOTOXU.
Použijte ihned po rekonstituci ve stříkačce. Zlikvidujte veškerý nepoužitý fyziologický roztok.
Tabulka ředění pro jednotku BOTOX 100 Allergan Unit pro všechny ostatní indikace:
Tento produkt je pouze na jedno použití a veškerý nepoužitý zbytkový roztok by měl být zlikvidován.
Pokyny k použití, zacházení a likvidaci lahviček viz bod 6.6.
Starší pacienti
Studie adekvátního dávkování nebyly u starších pacientů provedeny. Doporučuje se podávat nejnižší účinnou dávku s nejdelším klinicky vhodným intervalem mezi léčbami. Buďte zvláště opatrní u starších pacientů s významnou anamnézou a léčených souběžně jinými léky.
Pediatrická populace
Bezpečnost a účinnost přípravku BOTOX při léčbě blefarospasmu, hemifaciálního spasmu nebo cervikální dystonie nebyla u dětí (mladších 12 let) prokázána.
Bezpečnost a účinnost přípravku BOTOX při léčbě inkontinence moči v důsledku neurogenní hyperaktivity detruzoru nebyla u pediatrické populace (populace mladší 18 let) stanovena.
Bezpečnost a účinnost přípravku BOTOX při léčbě chronické migrény nebyla u pediatrické populace (populace mladší 18 let) studována.
Bezpečnost a účinnost přípravku BOTOX v léčbě primární hyperhidrózy podpaží nebyla studována u dětí mladších 12 let. Bezpečnost a účinnost přípravku BOTOX u dospívajících ve věku 12 až 17 let při léčbě závažné axilární hyperhidrózy nebyla stanovena. Aktuálně dostupné údaje jsou popsány v bodech 4.8 a 5.1, ale nelze učinit žádná doporučení ohledně dávkování (viz body 4.8 a 5.1).
Bezpečnost a účinnost přípravku BOTOX při léčbě spasticity horních končetin spojené s cévní mozkovou příhodou nebyla u dětí a dospívajících mladších 18 let stanovena.
Způsob podání
Podívejte se prosím na konkrétní doporučení pro každou indikaci popsanou níže.
BOTOX by měl být podáván pouze příslušně kvalifikovanými lékaři se zkušenostmi s manipulací a používáním požadovaného vybavení.
Optimální hladiny obecné platnosti nebyly stanoveny pro všechny indikace dávkování a počet míst vpichu v každém svalu. V těchto případech by měl lékař stanovit individuální léčebné režimy. Optimální hladiny pro dávkování by měly být stanoveny titrací, ale maximální doporučená dávka by neměla být překročena.
Blefarospasmus / hemifaciální křeč
Rekonstituovaný BOTOX by měl být aplikován pomocí sterilní jehly o průměru 27-30 / 0,40-0,30 mm. Elektromyografické vedení není nutné. Doporučená počáteční dávka je mezi 1,25-2,5 jednotek, které mají být podány do střední a laterální oblasti svalu orbicularis horního víčka a do laterální oblasti svalu orbicularis dolního víčka. Pokud jsou křeče v těchto oblastech v rozporu s viděním, mohou být do oblasti obočí, oblasti laterálního orbikulárního svalu a horní části obličeje vpichnuta další místa. dolní víčko, čímž se snižuje difúze v dolním šikmém svalu, může snížit komplikaci diplopie.
Obecně je počáteční účinek injekcí pozorován do tří dnů a dosahuje maxima 1–2 týdny po léčbě. Každé ošetření trvá přibližně tři měsíce, po kterých lze postup podle potřeby opakovat. V dalších sezeních může být dávka pokud je odpověď na počáteční léčbu považována za nedostatečnou, může být zvýšena až na dvojnásobek. Zdá se však, že zvýšení dávky nad 5 jednotek na místo má jen malý přínos. Počáteční dávka by neměla překročit 25 jednotek na oko. Za normálních okolností není dosaženo žádného dalšího prospěchu z léčby častěji než jednou za tři měsíce.
Při léčbě blefarospasmu by celková dávka neměla překročit 100 jednotek za období 12 týdnů.
Pacienti s hemifaciálním spasmem nebo poruchami sedmého nervu by měli být léčeni stejným způsobem jako pacienti s jednostranným blefarospasmem, s jinými postiženými obličejovými svaly vpichovanými podle potřeby.
Cervikální dystonie
Rekonstituovaný BOTOX by měl být aplikován pomocí jehly příslušné velikosti (typicky 25 - 30 gauge / 0,50 - 0,30 mm).
V klinických studiích léčba cervikální dystonie obvykle spočívala v injekci přípravku BOTOX do sternocleidomastoidu, levatorové lopatky, scalenu, splenu hlavy, semispinálního, velmi dlouhého a / nebo trapézového svalu (svalů). Tento seznam není vyčerpávající. mohou být zapojeny všechny svaly zodpovědné za kontrolu polohy hlavy, a proto vyžadují léčbu.
Hmotnost a stupeň svalové hypertrofie nebo atrofie jsou faktory, které je třeba vzít v úvahu při výběru vhodné dávky. Vzory aktivace svalů se mohou u cervikální dystonie spontánně změnit bez změny klinického projevu dystonie.
V případě potíží s izolací jednotlivých svalů musí být injekce provedena s elektromyografickým vedením. V prvních kontrolovaných klinických studiích ke stanovení bezpečnosti a účinnosti přípravku pro léčbu cervikální dystonie se dávky rekonstituovaného BOTOXU pohybovaly od 140 do 280 jednotek. V novějších studiích se podávané dávky pohybovaly od 95 do 360 jednotek. ( v průměru asi 240 jednotek.) Stejně jako u jiných léků by počáteční dávka u neléčeného pacienta měla být nejnižší účinná dávka. Na každé místo by nemělo být podáno více než 50 jednotek. Do sternocleidomastoidu by nemělo být injikováno více než 100 jednotek. sval Aby se minimalizoval výskyt dysfagie, neměl by být sternocleidomastoid podáván bilaterálně. V prvním cyklu terapie by nemělo být podáno celkem více než 200 jednotek, přičemž v následujících cyklech by měla být provedena odpovídající úprava dávkování na základě počáteční odpovědi.
Celková dávka 300 jednotek na jedno sezení by neměla být překročena. Optimální počet míst vpichu závisí na velikosti svalu.
Klinické zlepšení je obvykle pozorováno během prvních dvou týdnů po injekci. Maximální klinický přínos se obvykle dostavuje přibližně šest týdnů po injekci. Intervaly léčby kratší než 10 týdnů se nedoporučují. Trvání příznivého účinku v klinických studiích ukázalo značnou variabilitu (od 2 do 33 týdnů) s typickým trváním přibližně 12 týdnů.
Infantilní mozková obrna
Rekonstituovaný BOTOX by měl být injikován sterilní jehlou o rozměru 23-26 / 0,60 - 0,45 mm. Přípravek se podává jako frakční dávka jednotlivými injekcemi do mediálního a laterálního vrcholu postiženého svalu gastrocnemia. U hemiplegie je doporučená počáteční celková dávka 4 jednotky / kg tělesné hmotnosti v postižené končetině. U diplegie je počáteční doporučená celková dávka 6 jednotek / kg tělesné hmotnosti rozdělena mezi postižené končetiny. Celková dávka by neměla překročit 200 jednotek.
Ke klinickému zlepšení obvykle dochází během prvních dvou týdnů po injekci.
Další dávky by měly být podány, když se klinický účinek předchozí injekce sníží, ale ne častěji než jednou za tři měsíce. Dávkovací režim lze upravit tak, aby mezi následnými léčebnými cykly byl interval nejméně šest měsíců.
Fokální spasticita horní končetiny spojená s mrtvicí
Rekonstituovaný BOTOX by měl být injikován sterilní jehlou velikosti 25, 27 nebo 30 pro povrchové svaly a delší jehlou pro hlubší svaly. Pro lokalizaci postižených svalů může být užitečné použít techniky elektromyografického vedení nebo nervovou stimulaci. Více míst vpichu zajišťuje rovnoměrnější kontakt BOTOXu s inervačními oblastmi svalu a jsou užitečné zejména v případě větších svalů.
Správné dávkování a počet míst vpichu musí být přizpůsobeny individuálním potřebám na základě velikosti, počtu a umístění příslušných svalů, závažnosti spasticity, jakékoli místní svalové slabosti a reakce pacienta na předchozí léčbu.
Níže jsou uvedeny dávky podávané v kontrolovaných klinických studiích:
V kontrolovaných a nekontrolovaných otevřených klinických studiích byly v určitém léčebném cyklu použity dávky mezi 200 a 240 jednotkami rozdělenými mezi vybrané svaly.
V kontrolovaných klinických studiích byli pacienti sledováni po dobu 12 týdnů po jedné léčbě.
Zlepšení svalového tonusu bylo pozorováno do 2 týdnů a největší účinek byl obecně zaznamenán během 4-6 týdnů.
V pokračující nekontrolované otevřené studii byla většina pacientů ustoupena po intervalu 12-16 týdnů, kdy účinek na svalový tonus klesal.
Tito pacienti obdrželi až 4 očkování s maximální kumulativní dávkou 960 jednotek po dobu 54 týdnů. Pokud to lékař uzná za vhodné, mohou být podány opakované dávky, když se účinek předchozí injekce snižuje. Opakovaná léčba by neměla být provedena dříve než za 12 týdnů. Stupeň a typ svalové spasticity přítomné v době rinokulace může vyžadovat dávku úprava přípravku BOTOX a variace léčených svalů.
Měla by být použita nejnižší účinná dávka.
Primární hyperhidróza podpaží
Rekonstituovaný BOTOX (100 jednotek / 4 ml) se injektuje jehlou velikosti 30.
50 jednotek BOTOXu se naočkuje intradermálně, rovnoměrně distribuovaných na více místech přibližně 1 až 2 cm od sebe, při hyperhidróze každé podpaží.
Oblast hyperhidrózy může být definována pomocí standardních technik barvení, jako je například test jodičnanu škrobu. Dávky vyšší než 50 jednotek na podpaží nelze doporučit.
Ke klinickému zlepšení obvykle dochází během prvního týdne očkování.
BOTOX lze znovu naočkovat, pokud se sníží klinický účinek předchozí injekce a pokud to ošetřující lékař uzná za nutné. Očkování by se nemělo opakovat častěji než každých 16 týdnů (viz bod 5.1).
Inkontinence moči v důsledku neurogenní hyperaktivity detruzoru močového měchýře
V době léčby by pacienti neměli mít žádné infekce močových cest.
Antibiotika by měla být podávána k profylaxi 1-3 dny před léčbou, v den léčby a 1-3 dny po léčbě.
Doporučuje se, aby pacienti přerušili protidestičkovou léčbu nejméně 3 dny před injekčním postupem. Pacienti na antikoagulační léčbě musí být vhodně léčeni, aby se snížilo riziko krvácení.
Před injekcí je možné provést intravezikální instilaci zředěného anestetika (se sedací nebo bez sedace) nebo pokračovat v „celkové anestezii, podle místní praxe operačního zdravotnického zařízení. Pokud se provádí„ lokální instilace anestetika , před dalšími kroky injekčního postupu musí být močový měchýř vyprázdněn a omyt sterilním fyziologickým roztokem.
Doporučená dávka je 200 jednotek BOTOXu, tj. 1 ml injekce (~ 6,7 jednotek) do 30 míst svalu detrusoru.
Rekonstituovaný BOTOX (200 jednotek / 30 ml) se vstříkne do svalu detruzoru pomocí rigidního nebo flexibilního cystoskopu, přičemž se vyhýbá trigonu. Vdechněte do močového měchýře dostatečné množství fyziologického roztoku, abyste získali „adekvátní vizualizaci pro injekce, ale vyhněte se“ nadměrnému roztažení.
K odstranění veškerého přítomného vzduchu musí být injekční jehla před zahájením injekce naplněna přibližně 1 ml roztoku (v závislosti na délce jehly).
Vložte jehlu do svalu detruzoru asi na 2 mm a proveďte 30 injekcí po 1 ml (celkový objem 30 ml) přibližně 1 cm od sebe (viz obrázek). Pro konečnou injekci aplikujte asi 1 ml fyziologického roztoku normální sterilní k podání plné dávky. Jakmile byly injekce provedeny, vypusťte fyziologický roztok používaný k vizualizaci stěny močového měchýře. Pozorujte pacienta nejméně 30 minut po injekci.
Klinické zlepšení je obvykle pozorováno do 2 týdnů. Vyhodnoťte možnost opětovného uvedení pacientů na nový způsob léčby, pokud se sníží klinický účinek předchozí léčby (medián trvání v klinických studiích fáze III byl 256–295 dní u 200 jednotek přípravku BOTOX), ale ne dříve, než uplynou 3 měsíce od předchozí injekce do močového měchýře.
Chronická migréna
Diagnostika chronické migrény a podávání přípravku BOTOX by mělo být prováděno pouze pod dohledem neurologů se zkušenostmi s léčbou chronické migrény.
Doporučená dávka rekonstituovaného přípravku BOTOX pro léčbu chronické migrény je mezi 155 a 195 jednotkami podávanými intramuskulárně (IM) pomocí jehly 0,5 palce 30 s injekcemi rozdělenými mezi 7 specifických oblastí svalů hlavy a krku.
U pacientů s extrémně silnými krčními svaly může být nutné použít 1palcovou jehlu v cervikální oblasti. S výjimkou procerusového svalu, kde by mělo být injekčně aplikováno pouze jedno místo (střední linie), je třeba všechny ostatní svaly aplikovat bilaterálně, polovinu injekcí podat na levou a polovinu na pravou stranu hlavy a v případě převládající bolestivé místo nebo místa, je možné podat další injekce na jednu nebo obě strany maximálně do 3 specifických svalových skupin (okcipitální, temporální a trapézový), až do maximální dávky na sval.
Doporučený plán regenerace je každých 12 týdnů.
Dávkování BOTOXU na sval pro chronickou migrénu:
Pro všechny indikace
V případě selhání léčby po prvním cyklu léčby, například absence jednoho klinického zlepšení oproti výchozímu stavu, jeden měsíc po injekci, je nutné provést následující akce:
• klinické ověření účinku toxinu na injektovaný sval (svaly), které může zahrnovat elektromyografické vyšetření ve specializovaném kontextu;
• analýza příčin selhání, např. špatný výběr svalů k injekci, nedostatečná dávka, nesprávná injekční technika, vzhled pevné kontraktury, příliš slabé svaly antagonistů, tvorba protilátek neutralizujících toxiny;
• přehodnocení vhodnosti léčby botulotoxinem typu A;
• při absenci vedlejších účinků sekundárních k prvnímu průběhu léčby zahájte druhý léčebný postup následovně: i) upravte dávku s přihlédnutím k analýze selhání předchozí terapie; ii) použijte techniku EMG a iii) pozorujte interval tří měsíců mezi dvěma následujícími léčebnými cykly.
V případě selhání terapie nebo snížení účinku po opakovaných injekcích by měly být použity alternativní terapeutické metody.
04.3 Kontraindikace
BOTOX je kontraindikován:
• u subjektů se známou přecitlivělostí na botulotoxin typu A nebo na kteroukoli pomocnou látku;
• v přítomnosti infekce v navrhovaných místech vpichu.
BOTOX pro léčbu inkontinence moči v důsledku neurogenní hyperaktivity detruzoru močového měchýře je také kontraindikován:
• u pacientů, kteří mají v době léčby infekce močových cest;
• u pacientů s akutní retencí moči v době léčby, kteří běžně nepodstupují katetrizaci;
• u pacientů neochotných a / nebo neschopných zahájit katetrizaci po léčbě, je-li to nutné.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Před podáním přípravku BOTOX je nutné si uvědomit relativní normální anatomii postižené oblasti a jakékoli abnormální anatomické situace způsobené předchozím chirurgickým zákrokem a naočkování dříve poraněných anatomických struktur. U pacientů byly hlášeny závažné nežádoucí účinky včetně fatálních následků kteří dostali blíže neurčené injekce přípravku BOTOX přímo do slinných žláz, orlolingválně-faryngeální oblasti, jícnu a žaludku Někteří pacienti měli již existující dysfágii nebo výrazné oslabení.
Doporučené dávky a frekvence podávání přípravku BOTOX by neměly být překročeny.
Zřídka byly hlášeny závažné a / nebo okamžité reakce přecitlivělosti včetně anafylaxe, sérového onemocnění, kopřivky, mírného edému tkáně a dušnosti. Některé z těchto reakcí byly hlášeny po použití přípravku BOTOX samotného nebo s jinými přípravky, u nichž bylo zjištěno, že způsobují podobné reakce.
Pokud k takovým reakcím dojde, vyhněte se ošetřování pacienta novou injekcí přípravku BOTOX a okamžitě zahájte vhodnou lékařskou terapii, například epinefrinem. Byl hlášen případ anafylaxe u pacienta, který zemřel po injekci nevhodně naředěného přípravku BOTOX. S 5 ml 1% lidokainu (viz „Další informace“ v bodě 4.8).
Byly hlášeny nežádoucí účinky v důsledku šíření toxinu vzdáleného od místa podání (viz bod 4.8), které někdy měly za následek smrt, někdy spojené s dysfagií, zápalem plic a / nebo silnou astenií.
U pacientů léčených terapeutickými dávkami může dojít k přehnané svalové slabosti. U pacientů se základními neurologickými poruchami, včetně potíží s polykáním, je zvýšené riziko těchto reakcí. Produkt botulotoxinu by měl být u těchto pacientů používán pod odborným dohledem a měl by být používán pouze tehdy, pokud je přínos léčby považován za převažující nad rizikem. Pacienti s anamnézou dysfagie a aspirační pneumonie by měli být léčeni velmi opatrně.
Pacienti nebo pečovatelé by měli být poučeni, aby okamžitě vyhledali pomoc v případě poruch polykání, řeči nebo dýchání.
Dysfagie byla také hlášena po naočkování do jiných míst, než jsou svaly děložního čípku (viz bod 4.4 „Cervikální dystonie“).
Klinické výkyvy při opakovaném používání přípravku BOTOX (jako u všech botulotoxinů) mohou být způsobeny různými postupy rekonstituce lahvičky, intervaly mezi injekcemi, vstřikovanými svaly a malými rozdílnými hodnotami účinnosti danými použitým biologickým testem.
Tvorba protilátek neutralizujících botulotoxin typu A může snížit účinnost léčby přípravkem BOTOX v důsledku inaktivace biologické aktivity toxinu. Výsledky některých studií naznačují, že používání přípravku BOTOX v častějších intervalech nebo ve vyšších dávkách může mít za následek vyšší výskyt tvorby protilátek.V případě potřeby lze potenciální riziko tvorby protilátek minimalizovat injekcí nejúčinnější dávky. s delším, klinicky vhodným intervalem mezi léčbami.
Jako u každé léčby, která může umožnit pacientům, kteří dříve vedli sedavý životní styl, obnovit své aktivity, sedavému pacientovi by mělo být doporučeno, aby svoji aktivitu obnovoval postupně.
Opatrnosti je třeba při používání přípravku BOTOX v přítomnosti „zánětu v místě (místech) zvoleného pro injekci“ nebo v případě, že je v cílovém svalu pozorována nadměrná slabost nebo atrofie. Opatrnosti je třeba. Také při použití přípravku BOTOX k léčbě pacientů s periferním motorická neuropatická onemocnění (jako je laterální amyotrofická skleróza nebo motorická neuropatie).
BOTOX by měl být používán se zvláštní opatrností a pod pečlivým dohledem u pacientů s klinickými nebo subklinickými známkami poruchy nervosvalového přenosu, např. Myasthenia gravis nebo Lambert-Eatonův syndrom; tito pacienti mohou mít zvýšenou citlivost na látky, jako je BOTOX, což může vést k nadměrné svalové slabosti. U pacientů s neuromuskulárními poruchami může být při typickém dávkování přípravku BOTOX zvýšené riziko klinicky významných systémových reakcí včetně těžké dysfagie a respiračního poškození.
Jako u každé injekce může dojít k poškození souvisejícímu s postupem. Injekce může vést k lokalizované infekci, bolesti, zánětu, parestézii, hypoestézii, bolestivosti, otoku, erytému a / nebo krvácení / tvorbě modřin. Bolest související s používáním jehly a / nebo úzkostí může vést k vazovagální reakci, jako je synkopa, hypotenze , atd. Při injekci v blízkosti slabých anatomických oblastí je třeba postupovat opatrně.
Po podání přípravku BOTOX blízko hrudníku byl hlášen pneumotorax související s injekčním postupem. Při injekci v blízkosti plic, zejména v apikální oblasti, je třeba postupovat opatrně.
Pediatrické použití
Bezpečnost a účinnost přípravku BOTOX v jiných indikacích, než jaké jsou popsány v bodě 4.1 pro pediatrickou populaci, nebyla stanovena.Postmarketingové zprávy o možném vzdáleném šíření toxinu u pediatrických pacientů s komorbiditami, hlavně s paralýzou, byly hlášeny velmi vzácně. Dávka použitá v těchto případech obecně přesahovala doporučenou dávku (viz bod 4.8).
Po léčbě botulotoxinem byly vzácně hlášeny případy spontánních úmrtí někdy spojených s aspirační pneumonií u dětí s těžkou mozkovou obrnou, včetně případů použití mimo indikaci (např. Oblast krku). Při léčbě pacientů s výraznou neurologickou slabostí, dysfagií nebo v nedávné době aspirační pneumonií nebo plicním onemocněním je třeba postupovat velmi opatrně. Léčba u pacientů se špatným základním zdravotním stavem by měla být prováděna pouze tehdy, pokud je potenciální přínos pro pacienta považován za převažující nad riziky.
Blefarospasmus
Snížení mrkání způsobené injekcí botulotoxinu do svalu orbicularis může vést k expozici rohovky, přetrvávajícímu epiteliálnímu defektu a ulceraci rohovky, zvláště u pacientů se 7. nervovou poruchou. Doporučuje se provést pečlivé vyšetření citlivosti rohovky u dříve operovaných očí, vyhnout se injekci do oblasti dolních víček, aby nedošlo k ektropionu, a přijmout účinnou preventivní léčbu jakéhokoli defektu epitelu. To může vyžadovat použití očních kapek, očních mastí, měkkých terapeutických kontaktních čoček nebo zavření oka obvazem nebo jiným způsobem.
V měkkých tkáních víček může snadno dojít k tvorbě modřin. To lze minimalizovat jemným stlačením místa vpichu bezprostředně po injekci.
Vzhledem k anticholinergní aktivitě botulotoxinu je při léčbě pacientů s rizikem glaukomu s úzkým úhlem, včetně pacientů s anatomicky úzkými úhly, nutná zvláštní opatrnost.
Cervikální dystonie
Pacienti s cervikální dystonií by měli být upozorněni na možnost dysfagie, která může být velmi mírná, ale také závažná. Dysfagie může přetrvávat až 2–3 týdny po injekci, ale bylo popsáno, že trvá až 5 měsíců po injekci.
V důsledku dysfagie existuje možnost aspirace, dyspnoe a někdy i nutnost podávání sondou, ve vzácných případech byla hlášena dysfagie následovaná aspirační pneumonií a smrt.
Omezení dávky injikované do sternocleidomastoidního svalu na dávku nižší než 100 jednotek může snížit výskyt dysfagie. U pacientů s menší svalovou hmotou krku nebo pacientů, kteří dostávali injekce na obě strany sternocleidomastoidního svalu, bylo popsáno, že mají zvýšené riziko dysfagie. Dysfagii lze přičíst šíření toxinu do svalstva jícnu. Injekce do svalu levator scapulae mohou být spojeny se zvýšeným rizikem infekce horních cest dýchacích a dysfagie.
Dysfagie může pomoci snížit příjem jídla a vody, což vede ke ztrátě hmotnosti a dehydrataci.U pacientů se subklinickou dysfagií může být po injekci přípravku BOTOX zvýšené riziko závažné dysfagie.
Fokální spasticita spojená s dětskou mozkovou obrnou a spasticitou ruky a zápěstí u dospělých pacientů po mrtvici
BOTOX je léčba fokální spasticity, která byla studována pouze ve spojení s jinými standardními režimy péče, a není určena jako náhrada takových terapeutických modalit. BOTOX pravděpodobně nebude účinný při zlepšování rozsahu pohybu v kloubu postiženém trvalou patologickou kontrakturou.
Postmarketingové zprávy o možném šíření toxinu u pediatrických pacientů s komorbiditami, převážně s dětskou mozkovou obrnou, byly hlášeny vzácně. Obecně byla dávka použitá v těchto případech vyšší než doporučená (viz bod 4.8).
Po léčbě botulotoxinem byly hlášeny vzácné spontánní zprávy o smrti někdy spojené s aspirační pneumonií u dětí s těžkou mozkovou obrnou. Zvláštní péče by měla být věnována léčbě dětských pacientů s významnou neurologickou poruchou, dysfagií nebo nedávnou anamnézou aspirační pneumonie nebo plicního onemocnění.
Primární hyperhidróza podpaží
K vyloučení potenciálních příčin sekundární hyperhidrózy (např. Hypertyreóza, feochromocytom) by měla být provedena anamnéza a fyzické vyšetření pacienta, jakož i další vyšetřování, která mohou být považována za nezbytná. Tím se zabrání symptomatické léčbě hyperhidrózy bez diagnostiky a / nebo léčby základních onemocnění.
Inkontinence moči v důsledku neurogenní hyperaktivity detruzoru
Lékaři by měli při provádění cystoskopie postupovat opatrně.
U pacientů, kteří nepodstupují katetrizaci, by měl být zbytkový objem moči po prázdnotě vyhodnocen do 2 týdnů od léčby a pravidelně podle názoru lékaře po dobu až 12 týdnů. Poraďte pacienty, aby se v případě obtíží s močením poradili se svým lékařem, protože může být vyžadována katetrizace.
Může se objevit autonomní dysreflexie spojená s výkonem. Může být nutná okamžitá kontrola léčeného pacienta.
Chronická migréna
Bezpečnost a účinnost nebyla stanovena v profylaxi bolestí hlavy u pacientů s epizodickou migrénou (bolesti hlavy u chronické tenzní bolesti hlavy. Bezpečnost a účinnost přípravku BOTOX u pacientů s bolestí hlavy způsobenou nadměrným užíváním léků (sekundární porucha bolesti hlavy) nebyla studována.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Účinek botulotoxinu lze teoreticky zvýšit aminoglykosidovými antibiotiky nebo spektinomycinem nebo jinými léky, které interferují s nervosvalovým přenosem (např. Neuromuskulární blokátory).
Účinek souběžného podávání nebo během několika měsíců různých sérotypů botulotoxinu není znám. Podání dalšího botulotoxinu před dokončením účinků dříve podávaného botulotoxinu může způsobit zhoršení nervosvalové slabosti.
Nebyly provedeny žádné interakční studie. Nebyly hlášeny žádné klinicky významné interakce.
04.6 Těhotenství a kojení
Těhotenství
Nejsou k dispozici dostatečné údaje o použití botulotoxinu typu A u těhotných žen. Studie na zvířatech prokázaly reprodukční toxicitu (viz bod 5.3). Možné riziko pro člověka není známo. BOTOX by neměl být používán během těhotenství a u žen ve fertilním věku věk, který nepoužívá antikoncepci, pokud to není nezbytně nutné.
Čas krmení
Neexistují žádné informace o vylučování přípravku BOTOX do mléka.Použití přípravku BOTOX během kojení se nedoporučuje.
Plodnost
Nejsou k dispozici dostatečné údaje o účincích na fertilitu vyplývajících z použití botulotoxinu typu A u plodných žen. Studie na potkanech obou pohlaví prokázaly sníženou plodnost (viz bod 5.3).
04.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyly provedeny žádné studie schopnosti řídit a obsluhovat stroje.BOTOX však může způsobit astenii, svalovou slabost, závratě a poruchy vidění, které by mohly ovlivnit řízení a obsluhu strojů.
04.8 Nežádoucí účinky
Všeobecné
V kontrolovaných klinických studiích byly nežádoucí účinky, o nichž se domnívají, že se týkají přípravku BOTOX, hlášeny u 35% pacientů s blefarospasmem, u 28% pacientů s cervikální dystonií, u 17% pacientů s dětskou mozkovou obrnou, u 11% pacientů s primární axilární hyperhidróza a u 16% pacientů s fokální spasticitou horních končetin spojenou s cévní mozkovou příhodou. druhé ošetření. V klinických studiích chronické migrény byla incidence 26% při první léčbě a při druhé léčbě klesla na 11%.
Nežádoucí účinky se obecně vyskytují během prvních dnů po injekci a obvykle jsou přechodné, mohou trvat několik měsíců nebo ve vzácných případech i déle.
Lokalizovaná svalová slabost představuje očekávaný farmakologický účinek botulotoxinu ve svalové tkáni.
Jak se očekávalo pro jakýkoli injekční postup, s injekcí byla spojena lokalizovaná bolest, zánět, parestézie, hypoestézie, bolestivost, otok / edém, erytém, lokalizovaná infekce, krvácení a / nebo podlitiny. Bolest jehly a / nebo úzkost, která může mít za následek vazovagální odpověď, včetně přechodné symptomatické hypotenze a synkopy Po inokulaci botulotoxinem byl také hlášen syndrom horečky a chřipky.
Nežádoucí účinky - frekvence podle indikace
Frekvence nežádoucích účinků podle indikací, dokumentovaná během klinických studií, je uvedena níže.
Frekvence je definována následovně: velmi časté (> 1/10); časté (> 1/100 až 1/1 000 až 1/10 000 až
Blefarospasmus / hemifaciální křeč
Poruchy nervového systému
Méně časté: závratě, paréza obličeje a paralýza obličeje.
Oční poruchy
Velmi časté: ptóza očních víček.
Časté: bodkovaná keratitida, lagoftalmus, suché oko, fotofobie, podráždění očí a zvýšené slzení.
Méně časté: keratitida, ektropium, diplopie, entropie, poruchy vidění a rozmazané vidění.
Vzácné: edém víčka.
Velmi vzácné: ulcerózní keratitida, změna epitelu rohovky, perforace rohovky.
Poruchy kůže a podkožní tkáně
Časté: modřiny.
Méně časté: vyrážka / dermatitida.
Celkové poruchy a reakce v místě aplikace
Časté: podráždění obličeje a edém.
Méně časté: vyčerpání.
Cervikální dystonie
Infekce a infestace
Časté: rýma a infekce horních cest dýchacích.
Poruchy nervového systému
Časté: závratě, hypertonie, hypoestézie, ospalost a bolest hlavy.
Oční poruchy
Méně časté: diplopie a ptóza očních víček.
Respirační, hrudní a mediastinální poruchy
Méně časté: dušnost a dysfonie.
Gastrointestinální poruchy
Velmi časté: dysfagie (viz bod „Další informace“).
Časté: sucho v ústech a nevolnost.
Poruchy svalové a kosterní soustavy a pojivové tkáně
Velmi časté: svalová slabost.
Časté: muskuloskeletální ztuhlost a bolestivost.
Celkové poruchy a reakce v místě aplikace
Velmi časté: bolest.
Časté: astenie, příznaky podobné chřipce a malátnost.
Méně časté: horečka.
Infantilní mozková obrna
Infekce a infestace
Velmi časté: virová infekce a infekce ucha.
Poruchy nervového systému
Časté: somnolence, nekoordinovaná chůze a parestézie.
Poruchy kůže a podkožní tkáně
Časté: kožní vyrážka.
Poruchy svalové a kosterní soustavy a pojivové tkáně
Časté: myalgie, svalová slabost a bolest končetin.
Poruchy ledvin a močových cest
Časté: inkontinence moči.
Zranění, otravy a procedurální komplikace
Časté: pády.
Celkové poruchy a reakce v místě aplikace
Časté: malátnost, bolest v místě vpichu a astenie.
Fokální spasticita horní končetiny spojená s mrtvicí
Psychiatrické poruchy
Méně časté: deprese a nespavost.
Poruchy nervového systému
Časté: hypertonie.
Méně časté: hypoestézie, bolest hlavy, parestézie, nedostatek koordinace a amnézie.
Poruchy ucha a labyrintu
Méně časté: vertigo.
Cévní patologie
Méně časté: ortostatická hypotenze.
Gastrointestinální poruchy
Méně časté: orální nevolnost a parestézie.
Poruchy kůže a podkožní tkáně
Časté: ekchymóza a purpura.
Méně časté: dermatitida, pruritus a vyrážka.
Poruchy svalové a kosterní soustavy a pojivové tkáně
Časté: bolest končetin a svalová slabost.
Méně časté: artralgie a burzitida.
Celkové poruchy a reakce v místě aplikace
Časté: bolest v místě vpichu, horečka, chřipkový syndrom, krvácení a podráždění v místě vpichu.
Méně časté: astenie, bolest, přecitlivělost v místě vpichu, malátnost a periferní edém.
Některé z neobvyklých příhod mohou souviset s onemocněním.
Primární hyperhidróza podpaží
Poruchy nervového systému
Časté: bolest hlavy a parestézie.
Cévní patologie
Časté: návaly horka.
Gastrointestinální poruchy
Méně časté: nevolnost.
Poruchy kůže a podkožní tkáně
Časté: hyperhidróza (neaaxilární pocení), neobvyklý zápach kůže, pruritus, podkožní bulka a alopecie.
Poruchy svalové a kosterní soustavy a pojivové tkáně
Časté: bolest v končetinách.
Méně časté: svalová slabost, myalgie a artropatie.
Celkové poruchy a reakce v místě aplikace
Velmi časté: bolest v místě vpichu.
Časté: bolest, edém v místě vpichu, krvácení v místě vpichu, přecitlivělost v místě vpichu, podráždění v místě vpichu, astenie a reakce v místě vpichu.
Při léčbě primární axilární hyperhidrózy byl u 4,5% pacientů do 1 měsíce po naočkování hlášen zvýšený neosilární pot, bez přímého odkazu na příslušná anatomická místa.
Tento účinek odezněl přibližně u 30% pacientů do 4 měsíců.
Slabost horních končetin byla také hlášena jako méně častá (0,7%), mírná, přechodná, vyžadující žádnou léčbu a odeznívající bez následků. Tato nežádoucí reakce může souviset s léčbou, injekční technikou nebo obojím. V neobvyklém případě svalové slabosti hlášené po léčbě může být vyžadováno neurologické vyšetření.
Kromě toho může být nutné přehodnotit techniku očkování při následném ošetřování, aby bylo zajištěno intradermální umístění inokula.
V nekontrolované studii bezpečnosti s přípravkem BOTOX (50 U na podpaží) u pediatrických pacientů ve věku 12 až 17 let (N = 144) zahrnovaly nežádoucí účinky, které se vyskytly u více než jednoho pacienta (každé 2 pacienty), bolest v místě vpichu a hyperhidrózu ( neaaxilární pocení).
Inkontinence moči v důsledku neurogenní hyperaktivity detruzoru močového měchýře
Infekce a infestace
Velmi časté: infekce močových cest.
Psychiatrické poruchy
Časté: nespavost.
Gastrointestinální poruchy
Časté: zácpa.
Poruchy svalové a kosterní soustavy a pojivové tkáně
Časté: svalová slabost, svalové křeče.
Poruchy ledvin a močových cest
Velmi časté: retence moči.
Časté: hematurie *, dysurie *, divertikulum močového měchýře.
Celkové poruchy a reakce v místě aplikace
Časté: únava, poruchy chůze.
Zranění, otravy a procedurální komplikace
Časté: autonomní dysreflexie *, pády.
* nežádoucí účinky související s postupem
V klinických studiích byly infekce močových cest hlášeny u 49,2% pacientů léčených 200 U přípravku BOTOX a u 35,7% pacientů léčených placebem (53,0% pacientů s roztroušenou sklerózou léčených 200 U ve srovnání s 29,3% léčených placebem; 45,4 % pacientů s poraněním míchy léčených 200 U ve srovnání s 41,7% léčených placebem). Retence moči byla hlášena u 17,2% pacientů léčených 200 U přípravku BOTOX a u 2,9% pacientů léčených placebem (28,8% pacientů s roztroušenou sklerózou léčených 200 U ve srovnání se 4,5% léčených placebem; 5,4% pacientů s poranění míchy léčené 200 U oproti 1,4% léčeno placebem).
Při opakovaném podávání nebyla pozorována žádná změna typu nežádoucích účinků.
V pivotních studiích nebyl u pacientů s RS žádný rozdíl v roční míře vzplanutí roztroušené sklerózy (MS) (tj. Počtu vzplanutí MS na pacientorok) (BOTOX = 0,23, placebo = 0,20).
U pacientů, kteří nebyli před zahájením léčby katetrizováni, byla katetrizace zahájena u 38,9% po léčbě 200 jednotkami přípravku BOTOX ve srovnání se 17,3% u placeba.
Chronická migréna
Poruchy nervového systému
Časté: bolest hlavy, migréna, paréza obličeje.
Oční poruchy
Časté: ptóza očních víček.
Poruchy kůže a podkožní tkáně
Časté: pruritus, vyrážka.
Méně časté: bolest kůže.
Poruchy svalové a kosterní soustavy a pojivové tkáně
Časté: bolest krku, myalgie, muskuloskeletální bolest, artralgie, muskuloskeletální bolest, svalové křeče, ztuhlost svalů a svalová slabost.
Méně časté: bolest čelisti.
Celkové poruchy a reakce v místě aplikace
Časté: bolest v místě vpichu.
Gastrointestinální poruchy
Méně časté: dysfagie.
Míra ukončení léčby z důvodu nežádoucích účinků v těchto studiích fáze III byla 3,8% u přípravku BOTOX a 1,2% u placeba.
Další informace
Dysfagie se pohybuje od mírné po těžkou, s aspiračním potenciálem příležitostně vyžadujícím lékařskou pomoc (viz bod 4.4).
Nežádoucí účinky (přehnaná svalová slabost, dysfagie, zácpa, aspirační / aspirační pneumonie, v některých případech fatální) související s difúzí toxinu vzdáleného od místa podání byly hlášeny vzácně (viz bod 4.4).
Vzhledem k tomu, že je lék na trhu, byly hlášeny následující další nežádoucí účinky: svalová denervace / atrofie; respirační deprese a / nebo respirační selhání; aspirační pneumonie; dysartrie; strabismus, periferní neuropatie; bolest břicha; rozmazané vidění; poruchy zraku; horečka; paralýza obličeje; paréza obličeje; hypoestézie; nevolnost; myalgie; svědění; hyperhidróza; alopecie (včetně madarózy); průjem; anorexie; ztráta sluchu; tinnitus; závrať; radikulopatie; synkopa; myasthenia gravis; parestézie; multiformní erytém; psoriasiformní dermatitida; zvracení a brachiální plexopatie.
Rovněž byly vzácně hlášeny nežádoucí účinky postihující kardiovaskulární systém, včetně arytmií a infarktu myokardu, z nichž některé byly smrtelné. Někteří z těchto pacientů měli rizikové faktory, včetně kardiovaskulárních onemocnění.
Těžké a / nebo okamžité reakce přecitlivělosti, jako je anafylaxe a sérové onemocnění, jakož i další projevy přecitlivělosti, včetně kopřivky, edému měkkých tkání a dušnosti, byly hlášeny vzácně. Některé z těchto reakcí byly hlášeny po použití přípravku BOTOX samostatně nebo jiné látky, o nichž je známo, že způsobují podobné reakce.
Po léčbě blefarospasmu botulotoxinem byl velmi vzácně hlášen glaukom s uzavřeným úhlem.
Byly hlášeny případy počátečních nebo opakujících se záchvatů, zejména u pacientů s predispozicí k těmto typům reakcí. Přesný vztah těchto událostí k injekcím botulotoxinu nebyl stanoven.
U dětí byly tyto reakce hlášeny převážně u jedinců s dětskou mozkovou obrnou léčených pro spasticitu.
Bolest spojená s použitím jehly a / nebo úzkost může způsobit vazovagální reakci.
04.9 Předávkování
Koncept předávkování přípravkem BOTOX je relativní a závisí na dávce, místě vpichu a charakteristikách pozadí tkáně. Po náhodném očkování BOTOXU nebyly pozorovány žádné případy systémové toxicity. Nadměrné dávky mohou mít za následek lokální nebo vzdálenou, generalizovanou a hlubokou neuromuskulární paralýzu.
Nebyly pozorovány žádné případy požití přípravku BOTOX.
Známky a příznaky předávkování nejsou zřejmé bezprostředně po injekci. V případě náhodného vpichu nebo požití nebo podezření na předávkování by měl být pacient několik týdnů klinicky sledován na jakékoli známky a příznaky svalové slabosti, které mohou být místní nebo vzdálené od místo vpichu, které může zahrnovat ptózu, diplopii, dysfagii, dysartrii, generalizovanou astenii nebo respirační selhání.Tito pacienti by měli podstoupit další lékařské vyšetření a okamžitě zahájit vhodnou lékařskou terapii, která může také vyžadovat hospitalizaci.
Pokud jsou zasaženy svaly orofaryngu a jícnu, může dojít k aspiraci, která může vést k rozvoji aspirační pneumonie. V případě ochrnutí dýchacích svalů nebo dostatečného oslabení bude nutné uchýlit se k intubaci a asistovanému dýchání až do zotavení a kromě další obecné podpůrné péče také zahrnovat potřebu trecheostomie a prodloužené mechanické ventilace.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: jiná periferně působící svalová relaxancia.
ATC kód M03A X01
Botulotoxin typu A blokuje periferní uvolňování acetylcholinu na presynaptických cholinergních nervových zakončeních narušením uvolňování SNAP-25, což je protein, který doplňuje úspěšné shromažďování a uvolňování acetylcholinu z vezikul umístěných v nervových zakončeních.
Po injekci dojde k počátečnímu rychlému navázání toxinu na specifické receptory na povrchu buněk s vysokou afinitou, následuje přenos toxinu přes plazmatickou membránu pomocí endocytózy zprostředkované receptorem a nakonec se toxin uvolní do cytosolu.
Tento druhý proces je doprovázen postupnou inhibicí uvolňování acetylcholinu a klinické příznaky se objevují během 2–3 dnů s maximálním účinkem pozorovaným do 5–6 týdnů po injekci.
K zotavení po intramuskulární inokulaci obvykle dochází do 12 týdnů po injekci, protože nervová zakončení se regenerují a znovu spojují s koncovými ploténkami. Po intradermálním očkování, kde jsou cílem exokrinní potní žlázy, účinek trval průměrně 7,5 měsíce po první injekci u pacientů léčených 50 jednotkami na axilu U 27,5% pacientů však účinek trval 1 rok nebo déle. Obnova sympatických nervových zakončení potních žláz po intradermálním očkování přípravkem BOTOX nebyla studována.
BOTOX, po intradetrusorové injekci, má účinky na eferentní dráhy samotné aktivity detrusoru inhibicí uvolňování acetylcholinu. Kromě toho může BOTOX inhibovat uvolňování aferentních neurotransmiterů a dráhy citlivosti.
KLINICKÉ STUDIE
Primární hyperhidróza podpaží
Dvojitě zaslepená, multicentrická klinická studie byla provedena u pacientů, kteří měli přetrvávající bilaterální primární axilární hyperhidrózu stanovenou na počátku gravimetrickým měřením, rovnající se alespoň 50 mg spontánního potu produkovaného každým podpažím po dobu delší než 5 minut při pokojové teplotě, odpočívat. Tři sta dvacet pacientů bylo randomizováno k obdržení 50 jednotek přípravku BOTOX (N = 242) nebo placeba (N = 78). Respondenti pacienti byli definováni jako pacienti se snížením axilárního pocení o 50% oproti výchozím hodnotám.
V primárním cílovém parametru, 4 týdny po injekci, byla míra odpovědi ve skupině léčené přípravkem BOTOX 93,8%, ve srovnání s 35,9% u pacientů léčených placebem (p
Výskyt reagujících pacientů mezi pacienty léčenými přípravkem BOTOX byl i nadále významně vyšší (str
Do otevřené klinické klinické studie bylo zařazeno 207 způsobilých pacientů, kteří dostali až 3 ošetření přípravkem BOTOX. Konkrétně 174 pacientů dokončilo celé 16měsíční trvání 2 souhrnných studií (4měsíční dvojitě zaslepená studie a 12měsíční sledování otevřené studie). Incidence klinické odpovědi v 16. týdnu po první ( n = 287), druhé (n = 123) a třetí (n = 30) ošetření bylo 85,0%, 86,2% a 80%. Průměrná doba účinku na základě kombinované pokračovací studie s jednorázovou dávkou a otevřené studie byla 7,5 měsíce od první léčby; u 27,5% pacientů navíc účinek trval 1 rok nebo déle.
Zkušenosti s používáním přípravku BOTOX při axilární hyperhidróze u dětí mezi 12 a 18 lety jsou omezené.
Ve Spojených státech byla provedena jednoroční, nekontrolovaná studie bezpečnosti opakovaných dávek u pediatrických pacientů ve věku 12-17 let (N = 144) se závažnou primární hyperhidrózou axil. Pacienti byli převážně ženy (86,1%) a běloši (82,6%). Pacienti byli léčeni dávkou 50 U na podpaží, celkem 100 U na pacienta na ošetření. Nebyly však provedeny žádné studie dávkování u dospívajících, a proto nelze učinit žádná doporučení ohledně dávkování. Účinnost a bezpečnost přípravku BOTOX u této skupiny pacientů nebyla definitivně stanovena.
Inkontinence moči v důsledku neurogenní hyperaktivity detruzoru
Byly provedeny dvě multicentrické, randomizované, dvojitě zaslepené, placebem kontrolované klinické studie fáze III u pacientů s močovou inkontinencí způsobenou neurogenní hyperaktivitou detruzoru, schopnou spontánního močení nebo pomocí katetru. Celkem bylo zařazeno 691 pacientů s poraněním míchy nebo roztroušenou sklerózou, nedostatečně zvládnutým alespoň jedním anticholinergikem. Tito pacienti byli randomizováni, aby dostali 200 jednotek BOTOXU (n = 227), 300 jednotek BOTOXU (n = 223) nebo placebo (n = 241).
V obou studiích fáze III byla pozorována významná zlepšení ve prospěch přípravku BOTOX (200 jednotek a 300 jednotek) oproti placebu v primární proměnné účinnosti změny oproti výchozí hodnotě četnosti týdenní inkontinence v době detekce primární účinnosti. V 6. týdnu, včetně procento pacientů bez epizod inkontinence. Byla pozorována významná zlepšení urodynamických parametrů, včetně zvýšení maximální cystometrické kapacity a snížení maximálního tlaku detruzoru během první nedobrovolné kontrakce detruzoru. Bylo také pozorováno zlepšení. Významné ve srovnání s placebem ve skóre udávaném pacienty kvality života související se zdravím a inkontinencí měřené pomocí dotazníku Inkontinence Quality of Life (I-QOL) (včetně omezování vyhýbání se chování, „psychosociálního dopadu a“ sociálních rozpaků). U 300 jednotek BOTOX ve srovnání s 200 jednotkami nebyl prokázán žádný další přínos a u 200 jednotek BOTOX byl pozorován příznivější bezpečnostní profil.
Výsledky pivotních studií se souhrnnými údaji jsou uvedeny níže:
Primární a sekundární cílové parametry na počátku a změna oproti výchozím hodnotám v souhrnných pivotních studiích:
Střední doba trvání odpovědi ve dvou klíčových studiích na základě žádosti o opakovanou léčbu byla 256–295 dní (36–42 týdnů) ve skupině 200 dávkových jednotek ve srovnání s 92 dny (13 týdnů) s placebem.
U všech koncových bodů účinnosti měli pacienti odpovědi konzistentní s opakovanou léčbou.
V klíčových studiích se u žádného ze 475 pacientů s neurogenní hyperaktivitou detruzoru v analyzovaných vzorcích nevyvinuly neutralizační protilátky.
Chronická migréna
BOTOX blokuje uvolňování neurotransmiterů spojených s patogenezí bolesti.Mechanismus účinku přípravku BOTOX na symptomatickou úlevu u chronické migrény nebyl zcela objasněn.
Klinické a preklinické farmakodynamické studie naznačují, že BOTOX potlačuje periferní senzibilizaci, pravděpodobně tedy také inhibuje centrální senzibilizaci.
Níže uvedená tabulka ukazuje hlavní výsledky získané ze souhrnné analýzy účinnosti po dvou ošetřeních přípravkem BOTOX podávaných v 12týdenních intervalech ve dvou klinických studiích fáze III u pacientů s chronickou migrénou, kteří během základního období 28 dnů zaznamenali nejméně 4 epizody a trpěl bolestí hlavy po dobu ≥ 15 dnů (s nejméně 4 hodinami nepřetržité bolesti hlavy), přičemž nejméně 50% dní s bolestí hlavy bylo jak u migrény, tak u pravděpodobné migrény.
Přestože studie neměly dostatečný význam k prokázání rozdílů v podskupinách, účinek léčby se ve skupině pacientů mužského pohlaví (N = 188) a nekaukazských pacientů (N = 137) objevil méně než v celé populaci studie.
05.2 Farmakokinetické vlastnosti
Obecná charakteristika účinné látky
Distribuční studie provedené na potkanech naznačovaly pomalou svalovou difúzi komplexu 125I-botulinum neurotoxin typu A do svalu gastrocnemius po injekci, následovaný rychlým systémovým metabolizmem a eliminací v moči. Množství radioaktivně značeného materiálu ve svalu se snížilo s poločasem asi 10 hodin. V místě vpichu byla radioaktivita vázána na velké molekuly bílkovin, zatímco v plazmě byla vázána na malé molekuly, což naznačuje rychlý systémový metabolismus substrátu. Do 24 hodin po podání bylo 60% radioaktivity vyloučeno močí. Toxin je pravděpodobně metabolizován proteázami a molekulární složky jsou recyklovány normálními metabolickými cestami.
Vzhledem k povaze přípravku nebyly provedeny klasické studie absorpce, distribuce, biotransformace a eliminace účinné látky.
Charakteristika u pacientů
Předpokládá se, že terapeutické dávky přípravku BOTOX způsobují špatnou systémovou distribuci. Klinické studie prováděné technikami elektromyografie s jedním vláknem prokázaly zvýšenou nervosvalovou elektrofyziologickou aktivitu ve svalech vzdálených od místa vpichu, která není doprovázena žádnými klinickými příznaky.
05.3 Předklinické údaje vztahující se k bezpečnosti
Reprodukční studie
Po vystavení březích myší, potkanů a králíků intramuskulárním injekcím přípravku BOTOX v období organogeneze byla úroveň NOAEL (No Observable Adverse Effect Level) na vývoj 4, 1 respektive 0,125 jednotek / kg. Vyšší dávky byly spojeny se snížením tělesná hmotnost plodu a / nebo opožděná osifikace a potraty byly pozorovány u králíků.
Plodnost a reprodukce
Po podrobení potkanů samců a samic intramuskulárním injekcím BOTOXu byla reprodukční NOEL 4 respektive 8 jednotek / kg. Vyšší dávky byly spojeny se snížením plodnosti závislým na dávce.
Jakmile došlo k oplodnění, nebyly žádné nežádoucí účinky na počet nebo životaschopnost embryí požadovaných nebo počatých od ošetřených samců a samic krys.
Další studie
Kromě reprodukčních toxikologických studií byly pro BOTOX provedeny následující předklinické studie bezpečnosti: akutní toxicita, toxicita po opakovaných dávkách, lokální tolerance, mutagenita, antigenicita, kompatibilita s lidskou krví. Tyto studie neodhalily žádné zvláštní riziko pro člověka při klinicky relevantních úrovních dávek. Maximální doporučená dávka pro léčebné sezení je 300 jednotek (což odpovídá 6 jednotkám / kg u 50 kg osoby). Publikovaná intramuskulární LD50 u mladistvých opic je 39 jednotek / kg.
Po jednorázové intradetrusorové injekci prostatické uretry a proximálního konečníku, semenného váčku a stěny močového měchýře nebo opičí dělohy (~ 3 jednotky / kg) nebyla pozorována žádná systémová toxicita bez nežádoucích účinků.9 měsíců s opakovanými dávkami injekčně aplikovanými do svalu detrusoru (4 injekce), ptóza byla pozorována při 24 jednotkách / kg a úmrtnost při dávkách ≥ 24 jednotek / kg. Degenerace / regenerace svalových vláken byla pozorována v kosterních svalech zvířat, při nichž byla podána dávka nejméně 24 jednotek / kg. Tyto myopatické změny byly považovány za sekundární účinky systémové expozice. Dále byla pozorována degenerace svalových vláken u jednoho zvířete vystaveného dávce 12 jednotek / kg. Léze u tohoto zvířete byla minimální závažnosti a nebyla považována za spojenou s žádnými klinickými projevy. Nebylo možné s jistotou určit, zda to souviselo s léčbou přípravkem BOTOX. Dávka 12 jednotek / kg odpovídá 3krát větší expozici přípravku BOTOX, než je doporučená klinická dávka 200 jednotek pro inkontinenci moči v důsledku neurogenní hyperaktivity detrusorového svalu (u 50 kg osoby).
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Lidský albumin
Chlorid sodný
06.2 Neslučitelnost
Studie kompatibility nejsou k dispozici, a proto tento léčivý přípravek nesmí být mísen s jinými přípravky.
06.3 Doba platnosti
3 roky.
Mikrobiologické a potenční studie ukázaly, že přípravek lze po rekonstituci skladovat až 5 dnů při 2 ° -8 ° C.
Doba a podmínky uchovávání přípravku po otevření před použitím jsou v odpovědnosti uživatele a neměly by být delší než 24 hodin při 2 ° C - 8 ° C.
Po rekonstituci v lahvičce byla prokázána stabilita přípravku po dobu 24 hodin při 2 ° C - 8 ° C.
06.4 Zvláštní opatření pro skladování
Uchovávejte v chladničce (2 ° C - 8 ° C) nebo v mrazničce (-5 ° C nebo nižší).
Podmínky uchovávání rekonstituovaného léčivého přípravku viz bod 6.3.
06.5 Charakter vnitřního obalu a obsah balení
Injekční lahvička z bezbarvého skla typu I, jmenovitá kapacita 10 ml, opatřená chlorobutylovou pryžovou zátkou a hliníkovým těsněním, které je zřetelné.
Balení může mít 1, 2, 3, 6 nebo 10 lahviček.
Na trhu nemusí být všechny velikosti balení.
06.6 Návod k použití a zacházení
Je dobrým zvykem rekonstituovat injekční lahvičku a připravit stříkačku na plastifikovaný absorpční papír, aby se zachytil případný rozlitý produkt.
BOTOX by měl být rekonstituován pouze sterilním injekčním roztokem chloridu sodného 9 mg / ml (0,9%). Příslušné množství ředidla by mělo být nataženo injekční stříkačkou (pokyny k ředění inkontinence moči v důsledku neurogenní hyperaktivity detrusorového svalu viz bod 4.2).
Tabulka ředění pro jednotku BOTOX 100 Allergan Unit pro všechny ostatní indikace:
Pokud se během stejného ošetření používají balení s různou silou BOTOXU, věnujte zvláštní pozornost použití správného množství ředidla k rekonstituci konkrétního počtu jednotek na 0,1 ml. Množství ředidla se pohybuje mezi BOTOX 100 Allergan Units a BOTOX 200 Allergan Units. Každá stříkačka musí být řádně označena.
Protože je BOTOX denaturován šuměním nebo intenzivním mícháním, ředidlo by mělo být pomalu injikováno do lahvičky. Lahvičku je třeba zlikvidovat, pokud síla vakua není taková, aby natáhla ředidlo do lahvičky. Rekonstituovaný BOTOX by měl být čirý bezbarvý nebo světle žlutý roztok bez částic. Rekonstituovaný roztok musí být před použitím vizuálně zkontrolován na čirost a nepřítomnost částic. Po rekonstituci v injekční lahvičce může být BOTOX uchováván v chladničce (2-8 ° C) až 24 hodin před použitím. Datum a čas rekonstituce by mělo být uvedeno na místě určeném na štítku.
Při dalším ředění přípravku BOTOX na inkontinenci moči ve stříkačce musí být použit okamžitě. Tento přípravek je určen pouze k jednorázovému použití a veškerý zbývající nepoužitý roztok by měl být zlikvidován.
Z bezpečnostních důvodů je třeba nepoužité lahvičky rekonstituovat malým množstvím vody a poté autoklávovat. Všechny nepoužité injekční lahvičky, stříkačky a rozlitý materiál by měly být autoklávovány nebo jakýkoli zbytkový BOTOX by měl být deaktivován použitím roztoku chlornanu sodného (0,5%) po dobu 5 minut.
Nepoužitý léčivý přípravek a odpad z tohoto přípravku musí být zlikvidován v souladu s místními předpisy.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Allergan Pharmaceuticals Irsko
Silnice Castlebar
Westport
Hrabství Mayo
Irsko
Obchodní zástupce v Itálii
Allergan SpA, Via Salvatore Quasimodo č. 134/138, Řím
08.0 REGISTRAČNÍ ČÍSLO
AIC č. 034883013 / M „100 jednotek Allergan prášek pro injekční roztok“ 1 injekční lahvička obsahuje 100 jednotek Allergan
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
První povolení: 4. srpna 2000
Obnovení: 28. února 2009
10.0 DATUM REVIZE TEXTU
Rozhodnutí AIFA ze dne 23. ledna 2013