Účinné látky: kyselina zoledronová
Aclasta 5 mg infuzní roztok
Indikace Proč se používá Aclasta? K čemu to je?
Aclasta obsahuje léčivou látku kyselinu zoledronovou. Patří do skupiny léčiv nazývaných bisfosfonáty a používá se k léčbě postmenopauzálních žen a dospělých mužů s osteoporózou nebo osteoporózou způsobenou léčbou kortikosteroidy používanými k léčbě zánětů a Pagetovou chorobou kostí u dospělých.
Osteoporóza
Osteoporóza je onemocnění, které způsobuje řídnutí a oslabení kostí a je běžné u žen po menopauze, ale může se vyskytnout i u mužů. V období menopauzy vaječníky přestávají produkovat ženský hormon estrogen, který přispívá k zachování zdravotního stavu kosti. Po menopauze dochází ke ztrátě kostní hmoty, kosti jsou slabší a snadněji se lámou.Osteoporóza se může také objevit u mužů a žen v důsledku dlouhodobého užívání steroidů, které mohou ovlivnit pevnost kostí. Mnoho pacientů s osteoporózou nemá žádné příznaky, ale stále jim hrozí zlomenina kosti, protože osteoporóza způsobila, že jejich kosti jsou křehčí. Snížení hladin cirkulujících pohlavních hormonů, zejména estrogenu přeměněného z androgenů, také hraje roli v pozvolnějším úbytku kostní hmoty pozorovaném u mužů. U žen i mužů Aclasta posiluje kosti a snižuje riziko zlomenin. Aclasta se také používá u pacientů, kteří nedávno utrpěli zlomeninu kyčle v důsledku lehkého traumatu, jako je pád, a jsou proto ohroženi zlomeninami kostí.
Pagetova choroba kosti
Je normální, že stará kost je odstraněna a nahrazena novou kostí. Tento proces se nazývá remodelace kosti. U Pagetovy choroby je remodelace kostí příliš rychlá a nové kosti se tvoří neuspořádaným způsobem, což ji činí slabší než obvykle. Pokud se nemoc neléčí, kosti se mohou deformovat a být bolestivé a mohou se zlomit. Aclasta pracuje na tom, aby se proces remodelace kostí vrátil do normálu, zajišťoval normální tvorbu kostí, a tím obnovoval pevnost kosti.
Kontraindikace Kdy by Aclasta neměla být použita
Před podáním přípravku Aclasta pečlivě dodržujte všechny pokyny, které vám dal lékař, lékárník nebo zdravotní sestra.
Aclasta vám nesmí být podána:
- jestliže jste alergický (á) na kyselinu zoledronovou, jiné bisfosfonáty nebo na kteroukoli další složku tohoto přípravku
- jestliže máte hypokalcemii (tj. pokud máte příliš nízkou hladinu vápníku v krvi)
- jestliže máte závažné problémy s ledvinami
- pokud jste těhotná.
- pokud kojíte.
Opatření pro použití Co potřebujete vědět před užitím přípravku Aclasta
Před podáním přípravku Aclasta se poraďte se svým lékařem:
- jestliže jste léčen jakýmkoli lékem obsahujícím kyselinu zoledronovou, která je rovněž účinnou látkou přípravku Aclasta (kyselina zoledronová se používá u dospělých pacientů s určitými druhy rakoviny k prevenci kostních komplikací nebo ke snížení množství vápníku)
- jestliže máte problémy s ledvinami nebo jste někdy měl
- pokud nemůžete užívat denní doplněk vápníku
- pokud vám byla chirurgicky odstraněna část nebo všechny příštítné tělíska na krku.
- pokud vám byly odstraněny části střeva.
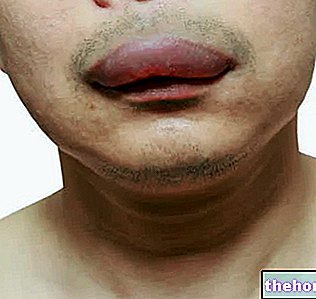
Po uvedení přípravku na trh byl u pacientů léčených přípravkem Aclasta (kyselina zoledronová) k léčbě osteoporózy hlášen nežádoucí účinek zvaný osteonekróza čelisti (poškození kosti čelisti). Osteonekróza čelisti. Může také nastat po ukončení léčby.
Je důležité pokusit se zabránit vzniku osteonekrózy čelisti, protože jde o bolestivý stav, který lze obtížně léčit. Abyste snížili riziko vzniku osteonekrózy čelisti, musíte dodržovat některá opatření.
Před zahájením léčby přípravkem Aclasta se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou, pokud:
- máte problémy s ústy nebo zuby, jako je špatné zdraví zubů, onemocnění dásní, nebo jste plánovali „extrakci zubů“
- nedostávejte běžnou péči o zuby nebo jste již delší dobu neměli zubní prohlídku
- jste kuřák (protože to může zvýšit riziko zubních problémů)
- dříve jste byli léčeni bisfosfonáty (používají se k léčbě nebo prevenci kostních poruch);
- užíváte léky nazývané kortikosteroidy (jako je prednisolon nebo dexamethason)
- má rakovinu.
Váš lékař vás může před zahájením léčby přípravkem Aclasta požádat o absolvování zubního vyšetření.
Během léčby přípravkem Aclasta musíte udržovat dobrou ústní hygienu (která zahrnuje pravidelné čištění zubů) a chodit na pravidelné zubní prohlídky. Pokud nosíte zubní protézy, musíte se ujistit, že jsou řádně zajištěny. Pokud podstupujete zubní ošetření nebo se chystáte podstoupit zubní chirurgii (např. Extrakce zubu), sdělte to prosím svému lékaři a řekněte svému zubnímu lékaři, že jste léčeni přípravkem Aclasta. Okamžitě informujte svého lékaře a zubaře, pokud se u vás vyskytnou problémy s ústy nebo zuby, jako je uvolnění, bolest, otok nebo nehojící se boláky nebo výtoky, protože to mohou být příznaky osteonekrózy čelisti.
Monitorovací test
Před každou infuzí přípravku Aclasta vám lékař musí odebrat vzorek krve, aby zkontroloval funkci ledvin (hladiny kreatininu). Je důležité, abyste vypili alespoň dvě sklenice tekutin (např. Vody) během několika hodin před ošetřením přípravkem Aclasta podle pokynů ošetřovatele.
Děti a dospívající
Aclasta se nedoporučuje do 18 let. Použití přípravku Aclasta u dětí a dospívajících nebylo studováno
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Aclasta
Informujte svého lékaře, lékárníka nebo zdravotní sestru o všech lécích, které užíváte, které jste v nedávné době užíval (a) nebo které možná budete užívat.
Je důležité, aby Váš lékař věděl o všech lécích, které užíváte, zvláště pokud již užíváte jiné léky, které jsou potenciálně škodlivé pro ledviny (např. Aminoglykosidy) nebo diuretika („léky na močení“), které mohou způsobit dehydrataci.
Varování Je důležité vědět, že:
Těhotenství a kojení
Aclasta vám nesmí být podána, pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět.
Před užitím tohoto léku se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou.
Řízení dopravních prostředků a obsluha strojů
Pokud máte při užívání přípravku Aclasta závrať, neřiďte ani neobsluhujte stroje, dokud se nebudete cítit lépe.
Aclasta obsahuje sodík
Tento léčivý přípravek obsahuje méně než 1 mmol sodíku (23 mg) na 100 ml lahvičku přípravku Aclasta, takže je v podstatě „bez sodíku“.
Dávka, způsob a doba podání Jak používat Aclasta: Dávkování
Pečlivě dodržujte všechny pokyny, které vám dal váš lékař nebo sestra.V případě pochybností se poraďte se svým lékařem nebo zdravotní sestrou.
Osteoporóza
Obvyklá dávka je 5 mg, kterou Vám lékař nebo sestra podá jednorázovou infuzí do žíly za rok Infuze bude trvat nejméně 15 minut.
V případě nedávné zlomeniny kyčle se doporučuje podat přípravek Aclasta dva nebo více týdnů po operaci zlomeniny kyčle.
Je důležité užívat doplňky vápníku a vitaminu D (např. Tablety) podle pokynů lékaře.
Na osteoporózu funguje Aclasta po dobu jednoho roku. Váš lékař vám sdělí, kdy se máte vrátit pro další dávku.
Pagetova nemoc
K léčbě Pagetovy choroby by přípravek Aclasta měli předepisovat pouze lékaři se zkušenostmi s léčbou Pagetovy choroby kostí.
Obvyklá dávka je 5 mg, kterou Vám lékař nebo sestra podá v úvodní infuzi do žíly. Infuze bude trvat nejméně 15 minut. Aclasta může působit déle než rok a váš lékař vás upozorní, pokud potřebujete další léčbu.
Váš lékař vám může doporučit užívat doplňky vápníku a vitaminu D (např. Tablety) alespoň prvních deset dní po užití přípravku Aclasta. Je důležité, abyste tuto radu pečlivě dodržovali, aby v období po infuzi nebyla hladina vápníku v krvi příliš nízká. Váš lékař vás bude informovat o možných příznacích spojených s hypokalcemií.
Přípravek Aclasta s jídlem a pitím
Před a po léčbě přípravkem Aclasta se ujistěte, že pijete dostatek tekutin (alespoň jednu nebo dvě sklenice). To pomůže zabránit dehydrataci. V den léčby přípravkem Aclasta můžete normálně jíst. To je zvláště důležité u pacientů užívajících diuretika (močicí pilulky) a u starších pacientů (ve věku 65 let nebo starších).
Jestliže jste zapomněl (a) užít dávku přípravku Aclasta
Kontaktujte svého lékaře nebo nemocnici co nejdříve a domluvte si novou schůzku.
Před ukončením léčby přípravkem Aclasta
Pokud zvažujete ukončení léčby přípravkem Aclasta, přijďte prosím na příští schůzku a prodiskutujte to se svým lékařem. Váš lékař vám může poradit a rozhodnout, jak dlouho pokračovat v léčbě.
Máte -li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Aclasta
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Nežádoucí účinky související s první infuzí jsou velmi časté (vyskytují se u více než 30% pacientů), ale po následných infuzích jsou méně časté. Většina nežádoucích účinků, jako je horečka a zimnice, bolest svalů nebo kloubů a bolest hlavy, se objevuje během prvních tří dnů po užití přípravku Aclasta. Příznaky jsou obvykle mírné až středně závažné a vymizí do tří dnů. Váš lékař může doporučit mírné zmírnění bolesti, jako je ibuprofen nebo acetaminofen, ke snížení těchto nežádoucích účinků. Šance na vedlejší účinky klesá s následnými dávkami přípravku Aclasta.
Některé nežádoucí účinky mohou být závažné
Časté (mohou postihnout až 1 z 10 lidí)
U pacientů léčených přípravkem Aclasta k léčbě postmenopauzální osteoporózy byl pozorován nepravidelný srdeční rytmus (fibrilace síní). V současné době není jasné, zda je příčinou tohoto nepravidelného srdečního rytmu Aclasta, ale měli byste o tom informovat svého lékaře, pokud po podání přípravku Aclasta vykazuje takové příznaky.
Méně časté (mohou postihnout až 1 ze 100 lidí)
Otok, zarudnutí, bolest a svědění očí nebo citlivost očí na světlo.
Velmi vzácné (mohou postihnout až 1 z 10 000 lidí)
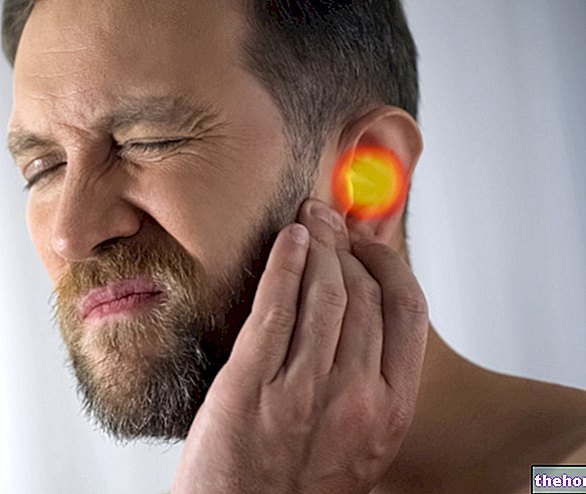
Poraďte se svým lékařem, pokud máte bolesti ucha, výtok z ucha a / nebo ušní infekci. Tyto epizody mohou být známkami poškození kostí v uchu. Není známo (frekvenci nelze z dostupných údajů určit) Bolest v ústech a / nebo čelisti, otok nebo vředy v ústech nebo čelisti, které se nehojí, výtok, necitlivost nebo pocit těžkosti v čelisti nebo uvolnění zubu ; mohou to být příznaky závažné kostní degenerace čelisti (osteonekróza). Okamžitě informujte svého lékaře a zubaře, pokud se u vás tyto příznaky objeví během léčby přípravkem Aclasta nebo po ukončení léčby.
Mohou se objevit poruchy ledvin (např. Snížené množství moči). Před každou infuzí přípravku Aclasta vám lékař bude muset odebrat krev, aby zkontroloval funkci ledvin. Je důležité, abyste vypili alespoň jednu nebo dvě sklenice tekutin (např. Vody) během několika hodin před léčbou přípravkem Aclasta, podle pokynů poskytovatele zdravotní péče.
Pokud se u vás vyskytne kterýkoli z těchto nežádoucích účinků, okamžitě to sdělte svému lékaři.
Aclasta může také způsobit další vedlejší účinky
Velmi časté (mohou postihnout více než 1 z 10 lidí)
Horečka
Časté (mohou postihnout až 1 z 10 lidí)
Bolest hlavy, závratě, malátnost, zvracení, průjem, bolesti těla, bolest kostí a / nebo kloubů, bolest zad, paží nebo nohou, příznaky podobné chřipce (např. Únava, zimnice, bolesti kloubů a svalů), zimnice, pocit únavy a nedostatek zájmu, slabost, bolest, pocit nevolnosti, otok a / nebo bolest v místě infuze.
U pacientů s Pagetovou chorobou byly hlášeny příznaky nízké hladiny vápníku v krvi, jako jsou svalové křeče nebo necitlivost nebo brnění, zejména v oblasti kolem úst.
Méně časté (mohou postihnout až 1 ze 100 lidí)
Chřipka, infekce horních cest dýchacích, snížený počet červených krvinek, ztráta chuti k jídlu, nespavost, ospalost, která může zahrnovat sníženou bdělost a vědomí, brnění nebo necitlivost, extrémní únava, třes, dočasná ztráta vědomí, infekce očí nebo podráždění nebo zánět s bolestí a zarudnutí, pocit závratě, zvýšený krevní tlak, zrudnutí, kašel, dušnost, bolest žaludku, bolest břicha, zácpa, sucho v ústech, pálení žáhy, vyrážka, nadměrné pocení, svědění, zarudnutí kůže, bolest krku, svalů, kostí a / nebo ztuhlost kloubů, otoky kloubů, svalové křeče, bolesti ramen, hrudníku a svalů hrudníku, záněty kloubů, svalová slabost, abnormální výsledky ledvinové testy, časté abnormální nutkání močit, otoky rukou, kotníků nebo chodidel, žízeň, bolest zubů, vysoká chuťový příděl.
Vzácné (mohou postihnout až 1 z 1000 lidí)
Zřídka, zvláště u pacientů dlouhodobě léčených na osteoporózu, může dojít k neobvyklé zlomenině stehenní kosti. Kontaktujte svého lékaře, pokud pociťujete bolest, slabost nebo nepříjemné pocity ve stehně, kyčli nebo tříslech, protože to může být „časná indikace možná zlomenina stehenní kosti.
Není známo (frekvenci nelze z dostupných údajů určit)
závažné alergické reakce zahrnující závratě a potíže s dýcháním, otoky hlavně obličeje a hrdla, pokles krevního tlaku, dehydrataci sekundární k příznakům po infuzi, jako je horečka, zvracení a průjem.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. To se týká i všech možných nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. poskytnout více informací o bezpečnosti tohoto léku.
Expirace a retence
Váš lékař, lékárník nebo zdravotní sestra vám poradí, jak správně uchovávat přípravek Aclasta.
- Uchovávejte tento přípravek mimo dohled a dosah dětí.
- Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a lahvičce za EXP.
- Neotevřená láhev nevyžaduje žádné zvláštní podmínky uchovávání.
- Po otevření lahve by měl být přípravek použit okamžitě, aby se zabránilo mikrobiální kontaminaci. Pokud není použit okamžitě, doba a podmínky uchovávání po otevření před použitím jsou v odpovědnosti uživatele a normálně by neměly být delší než 24 hodin při 2 ° C - 8 ° C. Před použitím počkejte, až roztok odebraný z chladničky dosáhne pokojové teploty.
Jiná informace
Co přípravek Aclasta obsahuje
Léčivou látkou je kyselina zoledronová. Jedna 100ml lahvička roztoku obsahuje 5 mg kyseliny zoledronové (jako monohydrát). Jeden ml roztoku obsahuje 0,05 mg kyseliny zoledronové (jako monohydrát).
Dalšími složkami jsou mannitol, citrát sodný a voda na injekci.
Jak přípravek Aclasta vypadá a obsah balení
Aclasta je čirý a bezbarvý roztok. Dodává se ve 100 ml plastových lahvích jako roztok připravený k infuzi.Je dodáván v krabičkách obsahujících jednu lahvičku pro jedno balení nebo ve vícedávkových kartonech obsahujících pět balení, po jedné lahvi. Na trhu nemusí být všechny velikosti balení.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
ACLASTA 5 MG ROZTOK K INFUZI
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna lahvička se 100 ml roztoku obsahuje 5 mg kyseliny zoledronové (jako monohydrát).
Jeden ml roztoku obsahuje 0,05 mg kyseliny zoledronové (jako monohydrát).
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Infuzní roztok
Čirý a bezbarvý roztok.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Léčba osteoporózy
• u postmenopauzálních žen
• u dospělých mužů
se zvýšeným rizikem zlomenin, včetně těch s nedávnou lehkou traumatickou zlomeninou kyčle.
Léčba osteoporózy spojená s dlouhodobou systémovou terapií glukokortikoidy
• u postmenopauzálních žen
• u dospělých mužů
se zvýšeným rizikem zlomenin.
Léčba Pagetovy choroby kostí u dospělých.
04.2 Dávkování a způsob podání
Dávkování
Před podáním přípravku Aclasta musí být pacienti dostatečně hydratováni. To je zvláště důležité pro starší osoby (≥65 let) a pro pacienty na diuretické léčbě.
Doporučuje se podávání přípravku Aclasta kombinovat s adekvátním doplňkem vápníku a vitaminu D.
Osteoporóza
Pro léčbu postmenopauzální osteoporózy, osteoporózy u lidí a pro léčbu osteoporózy spojené s dlouhodobou systémovou léčbou glukokortikoidy je doporučenou dávkou jedna intravenózní infuze přípravku Aclasta 5 mg podávaná jednou denně. Optimální doba léčby osteoporózy bisfosfonáty je nebyla stanovena. Potřeba pokračující léčby by měla být u každého jednotlivého pacienta pravidelně přehodnocována na základě potenciálních přínosů a rizik přípravku Aclasta, zejména po 5 a více letech používání. U pacientů s nedávnou lehkou traumatickou zlomeninou kyčle se doporučuje podávání infuzí přípravku Aclasta nejméně dva týdny po hojení zlomeniny kyčle (viz bod 5.1). U pacientů s nedávnou lehkou traumatickou zlomeninou kyčle se doporučuje nasycovací dávka 50 000 až 125 000 IU. vitamín D podávaný orálně nebo intramuskulárně před první infuzí přípravku Aclasta .
Pagetova nemoc
K léčbě Pagetovy choroby by přípravek Aclasta měli předepisovat pouze lékaři se zkušenostmi s léčbou Pagetovy choroby kostí. Doporučená dávka je jednorázová intravenózní infuze přípravku Aclasta 5 mg. Pacientům s Pagetovou chorobou se důrazně doporučuje zajistit adekvátní doplněk vápníku odpovídající alespoň 500 mg elementárního vápníku dvakrát denně po dobu nejméně 10 dnů po podání přípravku Aclasta (viz bod 4.4).
Opakovaná léčba Pagetovy choroby: U Pagetovy choroby bylo po počáteční léčbě přípravkem Aclasta u reagujících pacientů pozorováno prodloužené období remise. Opakovaná léčba u relabujících pacientů spočívá v „dodatečné intravenózní infuzi přípravku Aclasta 5 mg po intervalu jednoho roku nebo déle od počáteční léčby. O opětovné léčbě Pagetovy choroby jsou k dispozici omezené údaje (viz bod 5.1).
Zvláštní populace
Pacienti s poruchou funkce ledvin
Aclasta je kontraindikována u pacientů s clearance kreatininu
U pacientů s clearance kreatininu ≥ 35 ml / min není nutná úprava dávky.
Pacienti s poruchou funkce jater
Úprava dávky není nutná (viz bod 5.2).
Starší lidé (≥65 let)
Protože biologická dostupnost, distribuce a eliminace byly u starších a mladších subjektů podobné, není nutná úprava dávky.
Pediatrická populace
Bezpečnost a účinnost přípravku Aclasta u dětí a dospívajících mladších 18 let nebyla stanovena. Nejsou k dispozici žádné údaje.
Způsob podání
Intravenózní podání.
Aclasta se podává infuzní linkou s ventilační membránou a podává se pomalu konstantní rychlostí infuze. Doba infuze by neměla být kratší než 15 minut. Informace o tom, jak je přípravek Aclasta podáván, viz bod 6.6.
Pacienti léčení přípravkem Aclasta by měli dostat příbalovou informaci a kartu pacienta.
04.3 Kontraindikace
- Přecitlivělost na léčivou látku, na jakýkoli bisfosfonát nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
- Pacienti s hypokalcemií (viz bod 4.4).
- Těžké poškození ledvin s clearance kreatininu
- Těhotenství a kojení (viz bod 4.6).
04.4 Zvláštní upozornění a vhodná opatření pro použití
Funkce ledvin
Použití přípravku Aclasta u pacientů s těžkou poruchou funkce ledvin (renální insuficience clearance kreatininu v této populaci.
Po podání přípravku Aclasta (viz bod 4.8) bylo pozorováno poškození ledvin, zejména u pacientů s již existující renální dysfunkcí nebo s jinými rizikovými faktory včetně pokročilého věku, souběžného užívání nefrotoxických léčivých přípravků, souběžné diuretické léčby (viz bod 4.5), nebo dehydratace po podání přípravku Aclasta. Po jednorázovém podání bylo u pacientů pozorováno poškození ledvin. Renální selhání zahrnující potřebu dialýzy nebo s fatálním koncem se vzácně objevilo u pacientů se základním poškozením ledvin nebo s některým z výše popsaných rizikových faktorů. Aby se minimalizovalo riziko nežádoucích účinků na ledviny, je třeba zvážit následující opatření:
• Před každou infuzí přípravku Aclasta je třeba vypočítat clearance kreatininu z tělesné hmotnosti pomocí vzorce Cockcroft-Gault.
• Přechodné zvýšení sérového kreatininu může být výraznější u pacientů se základním poškozením ledvin.
• U rizikových pacientů by mělo být zváženo pravidelné sledování sérového kreatininu.
• Aclasta by měla být používána s opatrností, pokud je podávána současně s jinými léčivými přípravky, které mohou ovlivnit funkci ledvin (viz bod 4.5).
• Pacienti, zejména starší pacienti a ti, kteří užívají diuretika, by měli být před podáním přípravku Aclasta dostatečně hydratováni.
• Jedna infuze přípravku Aclasta by neměla překročit 5 mg a infuze by měla trvat nejméně 15 minut (viz bod 4.2).
Hypokalcémie
Již existující hypokalcemie by měla být před zahájením léčby přípravkem Aclasta léčena odpovídajícím podáním vápníku a vitaminu D (viz bod 4.3). Rovněž je třeba adekvátně léčit další změny v minerálním metabolismu (např. Snížená rezerva příštítných tělísek, malabsorpce střevního vápníku). U těchto pacientů by měli lékaři vyhodnotit možnost klinického sledování.
Vysoký obrat kostí je znakem Pagetovy choroby kostí. Vzhledem k rychlému nástupu účinku kyseliny zoledronové na kostní přeměnu se může vyvinout přechodná, někdy symptomatická hypokalcemie, která dosahuje maximálních hladin obvykle do 10 dnů po infuzi Aclasty (viz bod 4.8).
Doporučuje se podávání přípravku Aclasta kombinovat s adekvátním doplňkem vápníku a vitaminu D. Kromě toho se pacientům trpícím Pagetovou nemocí důrazně doporučuje zajistit dostatečný doplněk vápníku odpovídající alespoň 500 mg vápníku dvakrát denně alespoň v 10 dnů po podání přípravku Aclasta (viz bod 4.2). Pacienti by měli být informováni o možných příznacích způsobených hypokalcemií a během rizikového období by měli být vhodně sledováni z klinického hlediska.U pacientů s Pagetovou chorobou se doporučuje změřit sérové kalcium před infuzí Aclasta. U pacientů léčených bisfosfonáty, včetně kyseliny zoledronové, byla vzácně hlášena těžká a příležitostně invalidizující bolest kostí, kloubů a / nebo svalů (viz bod 4.8).
Osteonekróza dolní čelisti / čelisti
Osteonekróza čelisti byla po uvedení přípravku na trh hlášena u pacientů léčených Aclastou (kyselina zoledronová) na osteoporózu (viz bod 4.8). Zahájení léčby nebo nový průběh léčby by měl být odložen u pacientů s nezahojenými otevřenými lézemi měkkých tkání ústní dutiny.Před zahájením léčby přípravkem Aclasta u pacientů se souběžnými rizikovými faktory se doporučuje zubní vyšetření se souběžnými rizikovými faktory. preventivní zubní výkony a individuální posouzení prospěchu a rizika Při posuzování rizika rozvoje osteonekrózy čelisti u pacienta je třeba vzít v úvahu následující:
- Síla inhibice kostní resorpce léčiva (vyšší riziko pro velmi silné molekuly), způsob podání (vyšší riziko pro parenterální podání) a kumulativní dávka.
- Rakovina, komorbidity (např .: anémie, koaugulopatie, infekce), kouření.
- Souběžné terapie: kortikosteroidy, chemoterapie, inhibitory angiogeneze, radioterapie hlavy a krku.
- Špatná ústní hygiena, onemocnění parodontu, špatně fixované zubní protézy, anamnéza zubního onemocnění, invazivní zubní výkony, např .: extrakce zubů.
Všichni pacienti by měli být povzbuzováni k tomu, aby během léčby kyselinou zoledronovou udržovali dobrou ústní hygienu, podstupovali rutinní zubní prohlídky a okamžitě hlásili jakékoli orální příznaky, jako je pohyblivost zubů, bolest, otok nebo nehození vředů nebo výtok. V průběhu léčby by měly být invazivní zubní zákroky prováděny opatrně a nemělo by se jim vyhýbat v těsné blízkosti léčby kyselinou zoledronovou.
Program péče o pacienty, u kterých se vyvine osteonekróza čelisti, by měl být zaveden v úzké spolupráci mezi ošetřujícím lékařem a zubním lékařem nebo orálním chirurgem kompetentním v oblasti osteonekrózy čelisti. Je třeba zvážit dočasné přerušení léčby kyselinou zoledronovou, dokud se stav nevyřeší a pokud to bude možné, zmírnit souběžné rizikové faktory.
Osteonekróza zevního zvukovodu
Osteonekróza zevního zvukovodu byla hlášena v souvislosti s používáním bisfosfonátů, převážně ve spojení s dlouhodobými terapiemi.Možné rizikové faktory pro osteonekrózu zevního zvukovodu zahrnují použití steroidů a chemoterapie a / nebo lokálních rizikových faktorů, jako je jako infekce nebo trauma. Osteonekróza zevního zvukovodu by měla být zvážena u pacientů léčených bisfosfonáty, kteří mají ušní příznaky, včetně chronických ušních infekcí.
Atypické zlomeniny stehenní kosti
Byly hlášeny atypické subtrochanterické a diafyzární zlomeniny femuru, zejména u pacientů na dlouhodobé léčbě osteoporózy bisfosfonáty.Tyto krátké příčné nebo šikmé zlomeniny se mohou objevit kdekoli ve stehenní kosti od těsně pod malým trochanterem až nad suprakondylickou linii.Tyto zlomeniny se objevují spontánně nebo po minimálním traumatu a u některých pacientů se objevují bolesti stehen nebo třísel, často spojené se zobrazovacími známkami stresových zlomenin, týdny nebo měsíce před úplnou zlomeninou stehenní kosti. Zlomeniny jsou často oboustranné; proto u pacientů léčených bisfosfonáty Pokud utrpíte zlomeninu stehenní kosti, měl by být vyšetřen kontralaterální femur. Bylo také hlášeno omezené hojení těchto zlomenin. U pacientů s podezřením na atypickou zlomeninu stehenní kosti je třeba zvážit přerušení léčby bisfosfonáty až do zhodnocení pacienta na základě individuálního rizika prospěchu.
Během léčby bisfosfonáty by pacienti měli být poučeni, aby hlásili jakoukoli bolest stehna, kyčle nebo třísla a každý pacient, který vykazuje tyto příznaky, by měl být vyšetřen na přítomnost neúplné zlomeniny stehenní kosti.
Všeobecné
Výskyt symptomů po infuzi vyskytujících se během prvních tří dnů po podání přípravku Aclasta lze snížit podáním paracetamolu nebo ibuprofenu bezprostředně po podání přípravku Aclasta.
K dispozici jsou další přípravky obsahující kyselinu zoledronovou jako účinnou látku pro onkologické indikace. Pacienti léčení přípravkem Aclasta by neměli být současně léčeni těmito přípravky nebo jinými bisfosfonáty, protože kombinované účinky těchto látek nejsou známy. Tento léčivý přípravek obsahuje méně než 1 mmol sodíku (23 mg) na 100 ml lahvičku přípravku Aclasta, takže je v podstatě „bez sodíku“.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Nebyly provedeny žádné studie interakcí s jinými léčivými přípravky. Kyselina zoledronová není systémově metabolizována a neovlivňuje in vitro aktivita lidských enzymů cytochromu P450 (viz bod 5.2) Kyselina zoledronová se neváže extenzivně na plazmatické proteiny (váže se přibližně 43–55% léčiva), a proto dochází k interakcím vyplývajícím z vytlačení léčivých přípravků s vysokou vazbou na bílkoviny.
Kyselina zoledronová se eliminuje renální exkrecí.Pokud je kyselina zoledronová podávána v kombinaci s léčivými přípravky, které mohou mít významný vliv na funkci ledvin (např. Aminoglykosidy nebo diuretika, která mohou způsobit dehydrataci), postupujte opatrně (viz bod 4.4).
U pacientů s poruchou funkce ledvin může být zvýšena systémová expozice souběžně podávaným léčivým přípravkům vylučovaným primárně ledvinami.
04.6 Těhotenství a kojení
Ženy ve fertilním věku
Přípravek Aclasta se nedoporučuje u žen ve fertilním věku.
Těhotenství
Aclasta je během těhotenství kontraindikována (viz bod 4.3). Adekvátní údaje o podávání kyseliny zoledronové těhotným ženám nejsou k dispozici. Studie na zvířatech s kyselinou zoledronovou prokázaly reprodukční toxicitu včetně malformací (viz bod 5.3). Potenciální riziko pro člověka není známo.
Čas krmení
Aclasta je kontraindikována během laktace (viz bod 4.3) Není známo, zda se kyselina zoledronová vylučuje do lidského mléka.
Plodnost
Kyselina zoledronová byla hodnocena na potkanech z hlediska potenciálních nežádoucích účinků na plodnost rodičů a generaci F1. Výsledkem byly výrazné farmakologické účinky, které jsou považovány za související s inhibicí mobilizace kosterního vápníku sloučeninou, což má za následek hypokalcemii během periparta, bisfosfonátu třídní efekt, dystokie a předčasné ukončení studie. Tyto výsledky proto neumožňují určit konečný účinek přípravku Aclasta na plodnost u lidí.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Nežádoucí účinky, jako například závratě, mohou ovlivnit schopnost řídit nebo obsluhovat stroje.
04.8 Nežádoucí účinky
Shrnutí bezpečnostního profilu
Celkové procento pacientů s nežádoucími účinky bylo 44,7%, 16,7% a 10,2% po první, druhé a třetí infuzi. Incidence jednotlivých nežádoucích účinků po první infuzi byla: pyrexie (17,1%), myalgie (7,8%), onemocnění podobné chřipce (6,7%), artralgie (4,8%) a bolest hlavy (5,1%) Incidence těchto reakcí se snížila výrazně s postupnými ročními dávkami přípravku Aclasta. Většina těchto reakcí se vyskytla během prvních tří dnů po podání přípravku Aclasta. Většina těchto reakcí byla mírná až středně závažná a odezněla do tří dnů od výskytu příhody. V menší studii, kde byla profylaxe nežádoucích účinků prováděna níže popsaným způsobem, bylo procento pacientů, u nichž se vyskytly nežádoucí účinky, nižší (19,5%, 10,4 %, 10,7% po první, druhé a třetí infuzi).
Tabulka nežádoucích účinků
Nežádoucí účinky v tabulce 1 jsou uvedeny podle třídy orgánových systémů MedDRA a kategorie četnosti. Kategorie frekvencí jsou definovány pomocí následující konvence: velmi časté (≥ 1/10); časté (≥ 1/100,
stůl 1
# Pozorováno u pacientů užívajících současně glukokortikoidy.
* Běžné pouze u Pagetovy choroby.
** Na základě postmarketingových hlášení. Četnost nelze z dostupných údajů určit.
† Identifikováno během postmarketingového sledování.
Popis vybraných nežádoucích účinků
Fibrilace síní
Ve studii HORIZON - Pivotal Fracture Trial [PFT] (viz bod 5.1) byl celkový výskyt fibrilace síní u léčených pacientů 2,5% (96 z 3862) a 1,9% (75 z 3852). Míra závažných nežádoucích účinků fibrilace síní se zvýšila u pacientů užívajících přípravek Aclasta (1,3%) (51 z 3 862) ve srovnání s pacienty, kteří dostávali placebo (0,6%) (22 z 3 852). Mechanismus zvýšeného výskytu fibrilace síní je neznámý. Ve studiích osteoporózy (PFT, HORIZON - Recurrent Fracture Trial [RFT]) byl kombinovaný výskyt fibrilace síní srovnatelný mezi Aclastou (2,6%) a placebem (2,1%). U závažných nežádoucích účinků fibrilace síní byla kombinovaná incidence 1,3% u přípravku Aclasta a 0,8% u placeba.
Efekty třídy:
Porucha funkce ledvin
Kyselina zoledronová je spojována s poruchou funkce ledvin, což se projevuje zhoršením funkce ledvin (tj. Zvýšeným sérovým kreatininem) a ve vzácných případech akutním selháním ledvin.Po podání kyseliny zoledronové hlavně pacientům s již existující poruchou funkce ledvin nebo s dalšími rizikovými faktory ( např. vyšší věk, onkologičtí pacienti podstupující chemoterapii, souběžné užívání nefrotoxických léčivých přípravků, souběžná diuretická terapie, těžká dehydratace) bylo pozorováno poškození ledvin.Ve většině případů byli tito pacienti léčeni dávkou 4 mg každé 3-4 týdny, ale změna byla také detekována po jediném podání.
V klinických studiích s osteoporózou byly změny clearance kreatininu (měřeno každoročně před podáním dávky) a výskyt renální insuficience a poškození srovnatelné ve skupinách léčených Aclastou i placebem po dobu tří let. Během prvních 10 dnů bylo pozorováno přechodné zvýšení sérového kreatininu u 1,8% pacientů léčených přípravkem Aclasta ve srovnání s 0,8% pacientů léčených placebem.
Hypokalcémie
V klinických studiích osteoporózy přibližně 0,2% pacientů vykazovalo po podání přípravku Aclasta značný pokles hladin vápníku v séru (méně než 1,87 mmol / l). Nebyly pozorovány žádné symptomatické případy hypokalcemie.
Ve studiích Pagetovy choroby byla symptomatická hypokalcemie pozorována přibližně u 1% pacientů, přičemž ve všech případech ustupovala.
Na základě laboratorních hodnot se asymptomatické přechodné hladiny vápníku pod normálním referenčním rozsahem (méně než 2,10 mmol / l) vyskytly u 2,3% pacientů léčených přípravkem Aclasta ve velké klinické studii ve srovnání s 21% pacientů léčených přípravkem Aclasta ve studiích Pagetovy choroby. frekvence hypokalcemie byla po následných infuzích mnohem nižší.
Všem pacientům zařazeným do studie postmenopauzální osteoporózy, studie prevence klinické zlomeniny po zlomenině kyčle a studií Pagetovy choroby (viz také bod 4.2) bylo podáno dostatečné množství vitaminu D a vápníku ve studii prevence zlomenin po nedávné zlomenině kyčle, hladiny vitaminu D nebyly běžně měřeny, ale většina pacientů dostala před podáním přípravku Aclasta nasycovací dávku vitaminu D (viz bod 4.2).
Místní reakce
Ve velké klinické studii byly po podání kyseliny zoledronové hlášeny lokální reakce v místě infuze (0,7%), jako je zarudnutí, otok a / nebo bolest.
Osteonekróza dolní čelisti / čelisti
Případy osteonekrózy (čelisti) byly hlášeny hlavně u pacientů s rakovinou léčených přípravky, které inhibují resorpci kosti, včetně kyseliny zoledronové (viz bod 4.4) .V rozsáhlé klinické studii u 7 736 pacientů se jednalo o osteonekrózu čelisti jeden pacient léčený přípravkem Aclasta a jeden léčený placebem Po uvedení přípravku Aclasta na trh byly hlášeny případy osteonekrózy čelisti.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky, ke kterým dochází po registraci léčivého přípravku, je důležité, protože umožňuje průběžné sledování poměru přínosů a rizik léčivého přípravku.Zdravotničtí pracovníci jsou požádáni, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků.
04.9 Předávkování
Klinické zkušenosti s akutním předávkováním jsou omezené.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Léčiva k léčbě onemocnění kostí, bisfosfonáty, ATC kód: M05BA08
Mechanismus účinku
Kyselina zoledronová patří do třídy bisfosfonátů obsahujících dusík a působí především na kostní tkáň a je inhibitorem procesu kostní resorpce zprostředkované osteoklasty.
Farmakodynamické účinky
Selektivní působení bisfosfonátů na kost je dáno jejich vysokou afinitou k mineralizované kosti.Hlavním molekulárním cílem kyseliny zoledronové je enzym farnesylpyrofosfátsyntetáza v osteoklastech. Dlouhé působení kyseliny zoledronové lze přičíst její vysoké vazebné afinitě k aktivnímu místu syntetázy farnesylpyrofosfátu (FPP) a silné afinitě vůči mineralizované kosti .
Léčba přípravkem Aclasta rychle snížila rychlost kostního obratu z vysokých postmenopauzálních hladin s nejnižším počtem resorpčních markerů pozorovaných 7. den a markery tvorby ve 12. týdnu. Poté se kostní markery stabilizovaly v premenopauzálních rozsazích. Při opakovaném ročním dávkování nedošlo k progresivnímu snížení markerů kostního obratu.
Klinická účinnost při léčbě postmenopauzální osteoporózy (PFT)
Účinnost a bezpečnost přípravku Aclasta 5 mg jednou ročně po dobu 3 po sobě jdoucích let byla prokázána u postmenopauzálních žen (7 736 žen ve věku 65–89 let) s: kostní minerální hustotou (BMD), T-skóre krčku stehenní kosti ≤ -1,5 a alespoň dvěma pre -existující mírné nebo středně těžké zlomeniny obratlů; nebo skóre BMD krčku stehenní kosti ≤ -2,5 s nebo bez známek již existujících zlomenin obratlů. 85% pacientů bylo na první léčbě bisfosfonáty.Ženy hodnocené na výskyt zlomenin obratlů nedostávaly souběžnou léčbu osteoporózy, která byla podávána ženám hodnoceným na zlomeniny kyčle a všechny zlomeniny. Kliniky. Souběžná léčba osteoporózy zahrnovala: kalcitonin, raloxifen, tamoxifen, hormonální substituční terapii, tibolon; ale vyloučeny další bisfosfonáty. Všechny ženy dostaly 1 000 až 1 500 mg elementárního vápníku a 400 až 1 200 IU doplňku denně. Vitaminu D.
Účinek na morfometrické zlomeniny obratlů
Aclasta významně snížil výskyt jedné nebo více nových zlomenin obratlů během tří let a již v prvním roce průzkumu (viz tabulka 2).
Tabulka 2 Souhrn účinnosti u zlomenin obratlů po 12, 24 a 36 měsících
U pacientů ve věku 75 let a starších léčených přípravkem Aclasta došlo k 60% snížení rizika zlomenin obratlů ve srovnání s pacienty léčenými placebem (p
Účinek na zlomeniny kyčle
Aclasta prokázala konzistentní účinek po dobu 3 let, což vedlo ke snížení rizika zlomenin kyčle o 41% (95% CI, 17% až 58%). Míra epizody fraktury kyčle byla 1,44% ve skupině s Aclastou ve srovnání s 2,49% v skupina s placebem. Snížení rizika bylo 51% u pacientů na první léčbě bisfosfonáty a 42% u pacientů, kterým byla souběžně podávána léčba osteoporózy.
Účinek na všechny klinické zlomeniny
Všechny klinické zlomeniny byly vyšetřeny na základě radiografických a / nebo klinických důkazů. Souhrn výsledků je uveden v tabulce 3.
Tabulka 3 Srovnání léčby ve výskytu hlavních proměnných klinických zlomenin po dobu 3 let
Účinek na kostní minerální denzitu (BMD)
Aclasta významně zvýšil BMD bederní páteře, kyčle a distálního poloměru ve srovnání s léčbou placebem ve všech časových bodech (6, 12, 24 a 36 měsíců). Léčba přípravkem Aclasta vykázala ve srovnání s placebem za 3 roky léčby 6,7% nárůst BMD bederní páteře, 6,0% celkového kyčle, 5,1% krčku femuru a 3,2% distálního poloměru.
Histologie kostí
U 152 postmenopauzálních pacientů s osteoporózou léčených přípravkem Aclasta (N = 82) a placebem (N = 70) byly kostní biopsie získány z hřebene iliaca 1 rok po třetí roční dávce. Histomorfometrická analýza ukázala snížení obratu kostí o 63%. Osteomalácia, cystická fibróza a tvorba tkaná kost. S výjimkou jednoho případu byl marker tetracyklinů nalezen ve všech 82 biopsiích provedených u pacientů léčených přípravkem Aclasta. Mikropočítačová tomografie (µCT) prokázala zvýšení objemu trabekulární kosti a zachování architektury trabekulární kosti. „Trabeculární kost u pacientů léčeni přípravkem Aclasta ve srovnání se skupinou s placebem.
Značka obratu kostí
Hodnocení kostně specifické alkalické fosfatázy (BALP), sérového N-terminálního kolagenu typu I propeptidu (P1NP) a sérových beta-C telopeptidů (b-CTx) v podskupinách 517 až 1 246 pacientů v pravidelných intervalech po celou dobu studie. Léčba roční dávkou 5 mg Aclasty významně snížila BALP o 30% oproti výchozímu stavu po 12 měsících, což bylo udržováno na 28% pod výchozím stavem po 36 měsících. P1NP významně poklesl o 61% pod 12měsíční výchozí úroveň a zůstal 52% pod 36měsíční výchozí úrovní. B-CTx byl ve 12 měsících významně snížen o 61% oproti výchozím hodnotám a po 36 měsících zůstal 55% pod výchozími hodnotami. Po celé sledované časové období zůstávaly ukazatele kostního obratu na konci každého roku v rozmezí před menopauzou. Opakované dávkování nevedlo k dalšímu snížení ukazatelů kostního obratu.
Vliv na výšku
Ve tříleté studii osteoporózy byla výška postavení každoročně měřena pomocí stadiometru. Skupina léčená přípravkem Aclasta vykazovala přibližně o 2,5 mm menší zmenšení postavy než skupina s placebem (95% CI: 1,6 mm, 3,5 mm) [p = 0,0001].
Dny invalidity
Ve srovnání s placebem Aclasta významně snížil průměrné dny snížené aktivity a dny klidu na lůžku v důsledku bolestí dolní části zad o 17,9 dne, respektive o 11,3 dne, a současně také snížil průměrné dny snížené aktivity. A dny odpočinku v důsledku zlomenin 2,9 dne, respektive 0,5 dne, ve srovnání s placebem (p = 0,01).
Klinická účinnost při léčbě osteoporózy u pacientů se zvýšeným rizikem zlomenin po nedávné zlomenině kyčle (RFT)
Incidence zahrnutých klinických, vertebrálních, nevertebrálních zlomenin a zlomenin kyčle byla hodnocena u 2 127 mužů a žen ve věku 50–95 let (průměrný věk 74,5 let) s nedávnou (do 90 dnů) zlomeninou kyčle v důsledku mírného traumatu, které bylo následovala studijní léčba (Aclasta) v průměru 2 roky U přibližně 42% pacientů bylo T -skóre krčku stehenní kosti nižší než -2,5 a přibližně u 45% pacientů mělo T -skóre krčku stehenní kosti vyšší než -2,5. Aclasta byla podávána každoročně, dokud nebyly potvrzeny klinické zlomeniny alespoň u 211 pacientů sledované populace. Hladiny vitaminu D nebyly běžně měřeny, ale 2 týdny před infuzí byla většině pacientů podána nasycovací dávka vitaminu D (50 000 až 125 000 IU orálně nebo intramuskulárně). Všichni účastníci užívali 1 000 až 1 500 mg elementárního vápníku plus 800 až 1 200 IU doplňku vitaminu D denně. 95% pacientů dostalo infuzi dva nebo více týdnů po reparaci zlomeniny kyčle a medián doby do infuze byl přibližně šest týdnů po reparaci zlomeniny kyčle. Primární proměnnou účinnosti byl výskyt klinických zlomenin v průběhu studie.
Účinek na všechny klinické zlomeniny
Míra výskytu hlavních proměnných klinické zlomeniny je uvedena v tabulce 4.
Tabulka 4 Srovnání mezi léčbami ve výskytu hlavních proměnných klinické zlomeniny
Studie nebyla navržena tak, aby měřila významné rozdíly ve zlomenině kyčle, ale byl pozorován trend ve prospěch snížení nových zlomenin kyčle. Ve skupině léčené přípravkem Aclasta byla úmrtnost ze všech příčin 10% (101 pacientů) ve srovnání s 13% (141 pacientů) ve skupině s placebem. To odpovídá snížení rizika úmrtnosti ze všech příčin o 28% (p = 0,01).
Incidence opožděného hojení zlomeniny kyčle byla srovnatelná mezi Aclastou (34 [3,2%]) a placebem (29 [2,7%]).
Účinek na kostní minerální denzitu (BMD)
Ve studii HORIZON-RFT léčba Aclastou významně zvýšila celkovou BMD kyčelního a stehenního krku v porovnání s léčbou placebem ve všech časových bodech. Léčba Aclastou vykázala nárůst o 5,4%. Celková BMD kyčelního kloubu a 4,3% krčku femuru za 24 měsíců léčby ve srovnání s placebem .
Klinická účinnost u lidí
Ve studii HORIZON-RFT bylo randomizováno 508 mužů a 185 pacientů bylo hodnoceno na BMD ve 24. měsíci. Podobný významný 3,6% nárůst srovnatelné celkové BMD kyčle byl pozorován ve 24. měsíci u pacientů léčených přípravkem Aclasta. Účinky pozorované u postmenopauzálních žen ve studii HORIZON-PFT. Studie nebyla taková, aby prokázala snížení klinických zlomenin u lidí; výskyt klinických zlomenin byl 7,5% u mužů léčených přípravkem Aclasta ve srovnání s 8,7% u placeba. V jiné studii s placebem. "Muž (studie CZOL446M & SUP2; 308 ) procentuální změna BMD páteře ve 24. měsíci ve srovnání s výchozím stavem nebyla nižší po roční „infuzi Aclasty ve srovnání s alendronátem podávaným týdně.
Klinická účinnost při osteoporóze vyvolané dlouhodobou systémovou terapií glukokortikoidy Účinnost a bezpečnost přípravku Aclasta při léčbě a prevenci osteoporózy vyvolané dlouhodobou systémovou terapií glukokortikoidy byla hodnocena v randomizované, multicentrické studii. Dvojitě zaslepená, stratifikovaná aktivní kontrola na 833 mužích a ženách ve věku 18-85 let (průměrný věk u mužů 56,4 let; u žen 53,5 let) léčených> 7,5 mg / den prednisonu perorálně (nebo ekvivalentně). Pacienti byli stratifikováni podle délky léčby glukokortikoidy před randomizace (≤ 3 měsíce versus> 3 měsíce). Trvání studie bylo jeden rok. Pacienti byli randomizováni k jednorázové infuzi Aclasta 5 mg jednou denně nebo k perorálnímu risedronátu 5 mg denně po dobu jednoho roku. Všichni dostávali 1 000 mg elementárního vápníku denně plus 400 až 1 000 IU. doplnění vitaminu D. cia byla demonstrována v designu non-inferiority k risedronátu sekvenčním zobrazením procentní změny BMD páteře ve 12. měsíci od výchozí hodnoty v subpopulacích léčby a prevence. Většina pacientů pokračovala v užívání glukokortikoidů po dobu jednoho roku studie.
Účinek na kostní minerální denzitu (BMD)
Zvýšení BMD v páteři a krčku stehenní kosti ve 12. měsíci bylo ve skupině léčené přípravkem Aclasta významně větší ve srovnání s risedronátem (p
Klinická účinnost při léčbě Pagetovy choroby kostí Aclasta byla studována u pacientů mužského a ženského pohlaví starších 30 let s převážně mírnou až středně závažnou Pagetovou chorobou kostí (průměrná hladina alkalické fosfatázy v séru 2, 6–3,0násobek horní hranice specifické pro věk limit normálu při zápisu do studia) potvrzeno radiologickým vyšetřením.
Účinnost 5mg infuze kyseliny zoledronové proti risedronátu 30 mg denně podávaná po dobu 2 měsíců byla prokázána ve dvou srovnávacích studiích trvajících 6 měsíců. Po 6 měsících vykazoval Aclasta 96% (169/176) a 89% (156/176) terapeutické odpovědi a normalizaci sérových alkalických fosfatáz (SAP) ve srovnání se 74% (127/171) a 58% (99/ 171) získané risedronátem (vždy str
Při souhrnných výsledcích byl u přípravku Aclasta a risedronátu pozorován podobný pokles intenzity bolesti a skóre interference bolesti po dobu 6 měsíců od výchozího stavu.
Pacienti, kteří byli klasifikováni jako reagující na léčbu na konci 6měsíční základní studie, byli považováni za způsobilé pro zařazení do prodlouženého hodnotícího období. Ze 153 pacientů léčených přípravkem Aclasta a 115 pacientů léčených risedronátem, kteří vstoupili do prodlouženého období sledování studie, po průměrném období sledování 3,8 let po podání prodloužil podíl pacientů, kteří studii dokončili, pozorování potřeba opakované léčby (klinický úsudek) byla větší u risedronátu (48 pacientů, 41,7%) než u kyseliny zoledronové (11 pacientů, 7,2%). Průměrná doba do ukončení prodlouženého období pozorování z důvodu potřeby přepracování Pagetu z počáteční dávky byla delší u kyseliny zoledronové (7,7 let) než u risedronátu (5,1 roku).
Šest pacientů, kteří dosáhli terapeutické odpovědi 6 měsíců po léčbě přípravkem Aclasta a u nichž poté došlo k recidivě onemocnění během prodlouženého období hodnocení, bylo léčeno přípravkem Aclasta po průměrné době 6,5 roku mezi počátečním a přepracováním. Pět ze 6 pacientů mělo v 6. měsíci sérové hladiny alkalické fosfatázy v normálním rozmezí (Last Observation Carried Forward, LOCF).
Histologie kostí byla hodnocena u 7 pacientů s Pagetovou nemocí 6 měsíců po léčbě 5 mg kyseliny zoledronové Výsledky kostní biopsie ukázaly normální kvalitu kosti bez známek zhoršené remodelace kosti a bez známek mineralizačních defektů. Tyto výsledky byly v souladu s biochemickým ukazatelem důkazů normalizace kostního obratu.
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s přípravkem Aclasta ve všech podskupinách pediatrické populace pro Pagetovu kostní chorobu, osteoporózu u postmenopauzálních žen se zvýšeným rizikem zlomenin, osteoporózu u mužů se zvýšeným rizikem zlomenin a prevence klinických zlomenin po zlomenině kyčle u mužů a žen (informace o použití u dětí viz bod 4.2).
05.2 Farmakokinetické vlastnosti
Jednorázové a opakované 5 a 15minutové infuze 2, 4, 8 a 16 mg kyseliny zoledronové u 64 pacientů ukázaly následující farmakokinetické údaje bez ohledu na dávku.
Rozdělení
Po zahájení infuze kyseliny zoledronové se plazmatické koncentrace účinné látky rychle zvyšovaly, vrcholily na konci infuzní periody, následované rychlým poklesem.
Odstranění
Po intravenózním podání je kyselina zoledronová eliminována třístupňovým procesem: rychlé vymizení s dvoufázovým průběhem ze systémového oběhu s poločasy t½a 0,24 a t½b 1,87 hodiny, po kterém následuje dlouhá eliminační fáze s terminálním eliminačním poločasem t½g 146 hodin. Nebyla pozorována žádná akumulace účinné látky v plazmě po opakovaných dávkách podávaných každých 28 dní. vychytávání kostí a vylučování ledvinami. Kyselina zoledronová se nemetabolizuje a vylučuje se v nezměněné formě ledvinami.Počas prvních 24 hodin se v moči zachytí 39 ± 16% podané dávky, zatímco zbytek se váže hlavně na kostní tkáň. Tato absorpce do kosti je společná pro všechny bisfosfonáty a je pravděpodobně důsledkem strukturální analogie pyrofosfátu. Stejně jako u jiných bisfosfonátů je retenční čas kyseliny zoledronové v kosti velmi dlouhý. Z kosti se léčivo velmi pomalu uvolňuje do systémového oběhu a poté se eliminuje ledvinami. Celková tělesná clearance je 5,04 ± 2,5 l / h, bez ohledu na dávka, a není ovlivněna pohlavím, věkem, rasou nebo tělesnou hmotností. Variace v plazmatické clearance kyseliny zoledronové mezi jednotlivci a mezi jednotlivci byla 36%, respektive 34%. Prodloužení doby infuze z 5 na 15 minut mělo za následek 30% pokles koncentrace kyseliny zoledronové na konci infuze, ale nemělo to žádný vliv na oblast pod křivkou závislosti plazmatické koncentrace na čase.
Farmakokinetické / farmakodynamické vztahy
Nebyly provedeny žádné interakční studie s jinými léčivými přípravky a kyselinou zoledronovou. Jelikož kyselina zoledronová není u lidí metabolizována a bylo zjištěno, že látka má malou nebo žádnou kapacitu jako přímo působící a / nebo nevratný inhibitor metabolismu, v závislosti na enzymech P450 „Kyselina zoledronová pravděpodobně nesníží metabolickou clearance látek metabolizovaných prostřednictvím enzymatických systémů cytochromu P450. Kyselina zoledronová se ve velké míře neváže na plazmatické proteiny (váže se přibližně 43–55%) a vazba je nezávislá na koncentraci. Interakce vyplývající z vytlačení léčivých přípravků s vysokou vazbou na bílkoviny jsou proto nepravděpodobné.
Zvláštní populace (viz bod 4.2)
Porucha funkce ledvin
Renální clearance kyseliny zoledronové korelovala s clearance kreatininu, protože renální clearance představuje 75 ± 33% clearance kreatininu, což bylo v průměru 84 ± 29 ml / min u 64 studovaných pacientů. (Rozmezí 22 až 143 ml / min). zvýšení pozorované v AUC (0-24 hodin), mezi přibližně 30% a 40% u mírné až středně závažné poruchy funkce ledvin, ve srovnání s pacienty s normální funkcí ledvin, a absence akumulace léčiva po opakovaných dávkách bez ohledu na funkci ledvin naznačují, že žádná dávka úpravy kyseliny zoledronové jsou nutné u mírných (Clcr = 50-80 ml / min) a středně těžkého poškození ledvin až do clearance kreatininu 35 ml / min. Použití přípravku Aclasta u pacientů s těžkou poruchou funkce ledvin (clearance kreatininu
05.3 Předklinické údaje vztahující se k bezpečnosti
Akutní toxicita
Maximální neletální dávka pro jednorázové intravenózní podání byla 10 mg / kg tělesné hmotnosti u myší a 0,6 mg / kg u potkanů. Ve studiích s jednorázovou infuzí u psů bylo dobře tolerováno 1,0 mg / kg (6násobek doporučené terapeutické expozice u člověka na základě AUC) po dobu 15 minut bez renálních účinků.
Subchronická a chronická toxicita
Ve studiích intravenózní infuze byla u potkanů stanovena renální snášenlivost kyseliny zoledronové s podáváním 0,6 mg / kg jako 15minutové infuze ve 3denních intervalech, celkem šest infuzí (pro kumulativní dávku, která odpovídá hladinám AUC přibližně 6násobek terapeutické expozice u člověka), zatímco pět 15minutových infuzí 0,25 mg / kg podávaných ve 2–3 týdenních intervalech (kumulativní dávka odpovídající 7násobku terapeutické expozice pro člověka) byla u psů dobře snášena. V intravenózních bolusových studiích dávky, které byly dobře tolerovány, se s rostoucí délkou studie snižovaly: dávky 0,2 a 0,02 mg / kg denně byly dobře tolerovány po dobu 4 týdnů u potkanů a psů, ale pouze dávky 0,01 mg / kg a 0,005 mg / kg byly dobré tolerovány u potkanů a psů, v tomto pořadí, pokud jsou podávány po dobu 52 týdnů.
Dlouhodobé opakované podávání při kumulativních expozicích dostatečně překračujících maximální očekávanou expozici u člověka mělo toxikologické účinky v jiných orgánech, včetně gastrointestinálního traktu a jater, a v místě intravenózního podání. Klinický význam těchto nálezů není znám. Nejčastějším zjištěním ve studiích s opakovanými dávkami je nárůst houbovité kostní tkáně v metafýzách dlouhých kostí u vyvíjejících se zvířat téměř ve všech dávkách, což odráží antiresorpční farmakologickou aktivitu přípravku.
Toxicita pro reprodukci
Teratologické studie byly provedeny na dvou druzích, oba využívající subkutánní podání. Teratogenita byla pozorována u potkanů v dávkách ≥ 0,2 mg / kg a měla za následek vnější, viscerální a skeletální malformace. Dystocia byla pozorována při nejnižší testované dávce u potkanů (0,01 mg / kg tělesné hmotnosti). U králíků nebyly pozorovány žádné teratogenní ani embryo / fetální účinky, přestože toxicita pro matku byla pozorována při dávce 0,1 mg / kg kvůli nízkým hladinám vápníku v séru.
Mutagenita a karcinogenní potenciál
Kyselina zoledronová nebyla v provedených testech mutagenity mutagenní a testy karcinogenity neposkytly důkaz o karcinogenním potenciálu.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Mannitol
Citrát sodný
Voda na injekci
06.2 Neslučitelnost
Tento léčivý přípravek by neměl přijít do styku s roztoky obsahujícími vápník. Aclasta nesmí být mísena ani podávána intravenózně s jinými léčivými přípravky.
06.3 Doba platnosti
Neotevřená láhev: 3 roky
Po otevření: 24 hodin při 2 ° C - 8 ° C
Z mikrobiologického hlediska by měl být přípravek použit okamžitě. Není -li použit okamžitě, doba a podmínky uchovávání přípravku po otevření před použitím jsou v odpovědnosti uživatele a normálně by doba neměla být delší než 24 hodin při 2 ° C - 8 ° C.
06.4 Zvláštní opatření pro skladování
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Podmínky uchovávání léčivého přípravku po prvním otevření viz bod 6.3.
06.5 Charakter vnitřního obalu a obsah balení
100 ml roztoku v čiré plastové lahvičce (cykloolefinový polymer) uzavřené bromobutylovou gumovou zátkou potaženou fluoropolymerem a hliníkovým / polypropylenovým víčkem s odklápěcím prvkem.
Aclasta se dodává v jednotlivých baleních obsahujících jednu láhev nebo ve více baleních po pěti baleních, z nichž každé obsahuje jednu lahev.
Na trhu nemusí být všechny velikosti balení.
06.6 Návod k použití a zacházení
Pouze pro jednorázové použití.
Roztok by měl být použit pouze tehdy, je -li čirý, bez částic nebo bez barvy.
Pokud je roztok uchováván v chladničce, nechte jej před podáním dosáhnout pokojové teploty. Při přípravě infuze je nutné dodržovat aseptické postupy.Nepoužitý léčivý přípravek a odpad z tohoto léčivého přípravku musí být zlikvidován v souladu s místními předpisy.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Novartis Europharm Limited
Business park Frimley
Camberley GU16 7SR
Spojené království
08.0 REGISTRAČNÍ ČÍSLO
EU/1/05/308/001
EU/1/05/308/002
037105018
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Datum první registrace: 15. dubna 2005
Datum posledního obnovení: 19. dubna 2015