Aktivní složky: Bromelain
ANANASE 40 mg potahované tablety
Indikace Proč se používá Ananase? K čemu to je?
FARMAKOTERAPEUTICKÁ KATEGORIE
Ananase patří do třídy proteolytických enzymů
TERAPEUTICKÉ INDIKACE
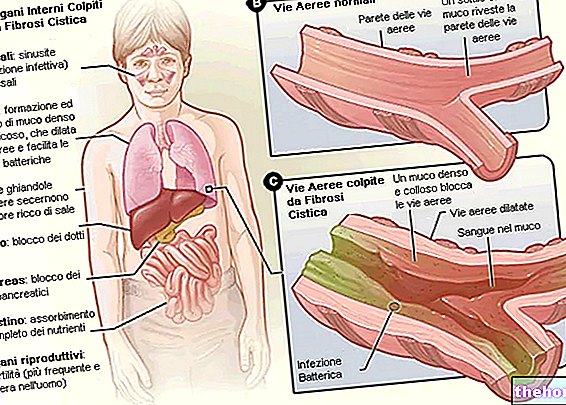
Procesy zánětlivého edému v lékařských a chirurgických oborech.
Kontraindikace Kdy by Ananase neměl být používán
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku tohoto přípravku.
Přípravek je kontraindikován u pacientů s hemofilií a s hemoragickou diatézou, v případě závažných hepatopatií a nefropatií; peptický vřed.
Pokud vám lékař řekl, že trpíte „nesnášenlivostí některých cukrů, kontaktujte svého lékaře před užitím tohoto léku (viz Zvláštní upozornění).
Opatření pro použití Co potřebujete vědět před užitím přípravku Ananase
Zkušenosti s používáním přípravku Ananase u dětí jsou omezené; dokud nebudou získány dostatečné údaje o bezpečnosti a účinnosti, mělo by být používání léčivého přípravku vyhrazeno pro dospělé.
U pacientů s hemofilií a hemoragickou diatézou je vhodné zkontrolovat koagulační indexy. Bromelain by měl být používán se zvláštní opatrností u pacientů se závažným onemocněním jater a renální insuficiencí.
Možný výskyt projevů přecitlivělosti různých typů a lokalizací naznačuje přerušení léčby a zavedení vhodné terapie.
Interakce Které léky nebo potraviny mohou ovlivnit účinek Ananase
Informujte svého lékaře nebo lékárníka o všech lécích, které jste v nedávné době užíval (a), a to i bez lékařského předpisu.
Spojení přípravku ANANASE s antikoagulancii často vyžaduje adekvátní úpravu dávkování.
Varování Je důležité vědět, že:
Těhotenství a kojení
Před užitím jakéhokoli léku se poraďte se svým lékařem nebo lékárníkem. Ananase lze používat během těhotenství nebo kojení pouze po konzultaci s lékařem a zhodnocení poměru rizika a přínosu ve vašem případě.
Pokud máte podezření, že jste těhotná nebo chcete naplánovat mateřskou dovolenou, poraďte se se svým lékařem.
Řízení dopravních prostředků a obsluha strojů
Ananase neovlivňuje schopnost řídit nebo obsluhovat stroje.
Důležité informace o některých složkách přípravku Ananase
Výrobek obsahuje laktózu a sacharózu; Pokud vám lékař řekl, že nesnášíte některé cukry, kontaktujte svého lékaře před užitím tohoto léku (viz Kontraindikace.
Dávka, způsob a doba podání Jak používat Ananase: Dávkování
Dospělí
Optimální počáteční dávkování je 1 potahovaná tableta čtyřikrát denně. 1 potahovaná tableta 2–3krát denně jako udržovací terapie.
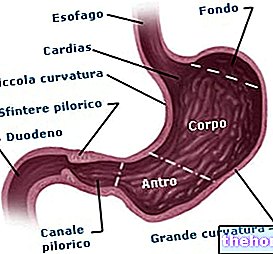
Potahované tablety se polykají celé, nejlépe na prázdný žaludek.
Děti
Zkušenosti s používáním přípravku Ananase u dětí jsou omezené; dokud nebudou získány dostatečné údaje o bezpečnosti a účinnosti, mělo by být používání léčivého přípravku vyhrazeno pro dospělé.
Předávkování Co dělat, když jste užil příliš mnoho přípravku Ananase
V případě náhodného požití / požití předávkování Ananase okamžitě informujte svého lékaře nebo jděte do nejbližší nemocnice.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Ananase
Podobně jako všechny léky, může mít i Ananase nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Byly hlášeny případy nevolnosti, zvracení, průjmu a vzácně případy menoragie a metrorhagie. Občas se mohou objevit alergické kožní reakce, erytém, svědění a ve vzácných případech astmatické záchvaty.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Expirace a retence
Expirace: Viz datum spotřeby vytištěné na obalu
Datum exspirace se vztahuje na produkt v neporušeném obalu, správně skladovaný.
UPOZORNĚNÍ: Nepoužívejte lék po uplynutí doby použitelnosti uvedené na obalu
Léčivé přípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
UCHOVÁVEJTE LÉČIVÝ MIMO DOSAH A DOHLED DĚTÍ
SLOŽENÍ
Jedna potahovaná tableta ANANASE obsahuje:
AKTIVNÍ ZÁSADA
Bromelain 40 000 mg (odpovídá 40 U.P.F.U.)
EXCIPIENTS
Bezvodý hydrogenfosforečnan vápenatý, monohydrát laktózy, dihydrát hydrogenfosforečnanu vápenatého, Macrogol 4000, kukuřičný škrob, koloidní oxid křemičitý, mastek, stearan hořečnatý, kyselina stearová, Eudragit L30 D-55, triethylcitrát, simethikon, želatina, Opalux AS-23014 (sacharóza, Chinolinová žluť, oxid titaničitý, oranžová žlutá S, povidon, benzoát sodný) voskový prášek, sacharóza.
LÉKOVÁ FORMA
Potahované tablety.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
TABLETY S ANALÝZOU 40 MG
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna potahovaná tableta ANANASE obsahuje:
AKTIVNÍ ZÁSADA
Bromelain mg 40 000 (odpovídá 40 U.P.F.U.).
EXCIPIENTS
Laktóza;
sacharóza.
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Potahované tablety.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Procesy zánětlivého edému v lékařských a chirurgických oborech.
04.2 Dávkování a způsob podání
Dospělí
Optimální počáteční dávkování je 1 potahovaná tableta čtyřikrát denně.
1 potahovaná tableta 2–3krát denně jako udržovací terapie.
Potahované tablety se polykají celé, nejlépe na prázdný žaludek.
Děti
Zkušenosti s používáním přípravku Ananase u dětí jsou omezené; dokud nebudou získány dostatečné údaje o bezpečnosti a účinnosti, je použití léčivého přípravku vyhrazeno pro dospělé (viz bod 4.4).
04.3 Kontraindikace
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku tohoto přípravku.
Přípravek je kontraindikován u pacientů s hemofilií a hemoragickou diatézou, jako v případě závažných jater a nefropatií; peptický vřed.
Vzhledem k přítomnosti laktózy mezi pomocnými látkami přípravku Ananase by tento přípravek neměli užívat pacienti se vzácnými dědičnými problémy s intolerancí galaktózy, vrozeným nedostatkem laktázy nebo malabsorpcí glukózy a galaktózy (viz bod 4.4).
Vzhledem k přítomnosti sacharózy mezi pomocnými látkami přípravku Ananase by pacienti se vzácnými dědičnými problémy s intolerancí fruktózy, malabsorpcí glukózy / galaktózy nebo insuficiencí sacharázy a izolátu nesměli tento léčivý přípravek užívat (viz bod 4.4).
04.4 Zvláštní upozornění a vhodná opatření pro použití
U těhotných žen a kojenců používejte pouze tehdy, je -li to nezbytně nutné, a pod přímým lékařským dohledem. Zkušenosti s používáním přípravku Ananase u dětí jsou omezené; dokud nebudou získány dostatečné údaje o bezpečnosti a účinnosti, je použití léčivého přípravku vyhrazeno pro dospělé.
U pacientů s hemofilií a hemoragickou diatézou je vhodné zkontrolovat koagulační indexy. Bromelain by měl být používán se zvláštní opatrností u pacientů s těžkým onemocněním jater nebo renální insuficiencí, která naznačuje přerušení léčby a zahájení vhodné terapie. Pacienti se vzácnými dědičnými problémy s intolerancí galaktózy, nedostatkem
Lapp laktáza nebo malabsorpce glukózy a galaktózy by tento léčivý přípravek neměly užívat (viz bod 4.3)
Pacienti se vzácnými dědičnými problémy s intolerancí fruktózy, malabsorpcí glukózo-galaktosy nebo insuficiencí sacharázy a izomatázy by tento léčivý přípravek neměli užívat (viz bod 4.3).
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Spojení přípravku ANANASE s antikoagulancii často vyžaduje adekvátní úpravu dávkování.
04.6 Těhotenství a kojení
Pro bromelain nejsou k dispozici žádné klinické údaje o těhotenství během těhotenství. Studie na zvířatech (krysy a králíci) neprokázaly embryotoxické ani teratogenní účinky. Proto by měl být Ananase podáván během těhotenství a kojení pouze tehdy, pokud je to zjevně nutné, a pod přímým lékařským dohledem.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Ananase neovlivňuje schopnost řídit nebo obsluhovat stroje.
04.8 Nežádoucí účinky
Byly hlášeny případy nevolnosti, zvracení, průjmu a vzácně případy menoragie a metroragie. Občas se mohou vyskytnout kožní alergické situace, erytém, svědění a ve vzácných případech astmatické záchvaty.
* jejichž četnost nelze z dostupných údajů odhadnout.
04.9 Předávkování
Nejsou známy žádné případy náhodného a úmyslného předávkování u lidí s nástupem toxických příznaků.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: jiná hematologická činidla - enzymy.
ATC: B06AA.
Bromelain podávaný i.p. a orálně v dávkách 5-10 mg / kg snižuje otoky a záněty způsobené histaminem, formalinem, dextranem, karagenanem a vaječným albuminem u zvířete. Na úrovni zánětlivé tkáně snižuje vazodilataci, zvýšení kapilární permeability, migraci leukocytů a lokální bolest tím, že inhibuje tvorbu bradykininu a serotoninu.
05.2 Farmakokinetické vlastnosti
Absorpce bromelainu po perorálním podání představuje velkou individuální variabilitu. Plazmatický poločas je mezi 6 a 9 hodinami.
05.3 Předklinické údaje vztahující se k bezpečnosti
LD50 pro orální podání: žádná toxicita při dávkách nad 10 mg / kg pro všechna testovaná zvířata.
Pro jiné způsoby podání (i.p. a i.v.): LD50 se liší podle zvířat od 20 do 85 mg / kg.
Při dlouhodobém orálním podávání u hlodavců a nehlodavců nebyla ve srovnání s kontrolami zaznamenána žádná změna ve fyzikálně biologických parametrech.
Fetální toxicita: chybí.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Bezvodý hydrogenfosforečnan vápenatý, monohydrát laktózy, dihydrát hydrogenfosforečnanu vápenatého, makrogol 4000, kukuřičný škrob, koloidní oxid křemičitý, mastek, stearan hořečnatý, kyselina stearová, eudragit l30 d-55, triethylcitrát, simethikon, želatina, sacharóza, voskový prášek, opalux jako -23014 (sacharóza, chinolinová žluť, oxid titaničitý, oranžově žlutá s, polyvinylpyrrolidon, benzoát sodný).
06.2 Neslučitelnost
Irelevantní.
06.3 Doba platnosti
5 let.
Uvedené datum použitelnosti se vztahuje na produkt v neporušeném obalu, správně skladovaný.
06.4 Zvláštní opatření pro skladování
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
06.5 Charakter vnitřního obalu a obsah balení
Krabička s 20 potahovanými tabletami
06.6 Návod k použití a zacházení
Žádné zvláštní pokyny
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
ROTTAPHARM S.p.A. - Galleria Unione, 5 - 20122 Milán
08.0 REGISTRAČNÍ ČÍSLO
AIC: 020501021
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Datum první registrace: 20. listopadu 1971
Obnovení autorizace: květen 2010
10.0 DATUM REVIZE TEXTU
Březen 2011