Účinné látky: Deferasirox
EXJADE 90 mg potahované tablety
EXJADE 180 mg potahované tablety
EXJADE 360 mg potahované tablety
Vložky do balení Exjade jsou k dispozici pro velikosti balení: - EXJADE 125 mg dispergovatelné tablety, EXJADE 250 mg dispergovatelné tablety, EXJADE 500 mg dispergovatelné tablety
- EXJADE 90 mg potahované tablety, EXJADE 180 mg potahované tablety, EXJADE 360 mg potahované tablety
Proč se Exjade používá? K čemu to je?
Co je EXJADE
EXJADE obsahuje léčivou látku zvanou deferasirox. Jedná se o chelátor železa, což je lék používaný k odstranění přebytečného železa z těla (přetížení železem) .Deferasirox se na přebytečné železo váže a odstraňuje ho tak, že ho eliminuje hlavně ve stolici.
K čemu je EXJADE
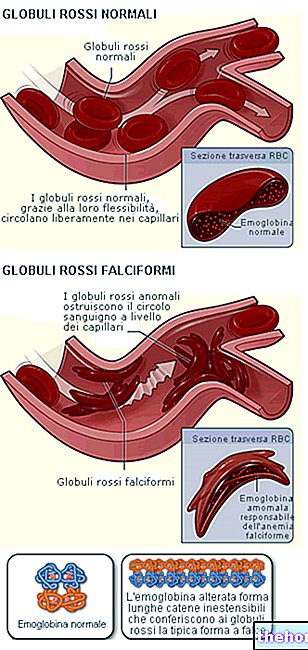
U pacientů s různými formami anémie (například talasémie, srpkovitá anémie nebo myelodysplastické syndromy (MDS)) mohou být nutné opakované krevní transfuze. Ty však mohou v těle způsobit nadbytek železa. Důvodem je, že krev obsahuje železo v těle. nemá žádný přirozený způsob, jak odstranit přebytečné železo zavedené transfuzí krve. U pacientů s thalassemickými syndromy, kteří nedostávají krevní transfuze, se může časem vyvinout také přetížení železem, zejména v důsledku zvýšeného krevního tlaku. Dietní absorpce železa v reakci na nízký počet krvinek. Časem může přebytečné železo poškodit důležité orgány, jako jsou játra a srdce. K odstranění železa se používají léky zvané chelátory železa. přebytek železa a snížení rizika, že to může poškodit některé orgány.
EXJADE se používá k léčbě přetížení železa v důsledku častých krevních transfuzí u pacientů s beta thalassemií major ve věku 6 let a starší.
EXJADE se také používá k léčbě přetížení železem, pokud je léčba deferoxaminem kontraindikována nebo neadekvátní u pacientů s beta thalassemií major s přetížením železem v důsledku vzácných krevních transfuzí, u pacientů s jinými formami anémie a u dětí. Ve věku od 2 do 5 let .
EXJADE se také používá, pokud je léčba deferoxaminem kontraindikována nebo neadekvátní k léčbě pacientů ve věku 10 let a starších, kteří mají přetížení železem související se syndromy thalasemie, ale nevyžadují transfuzi krve.
Kontraindikace Kdy by neměl být přípravek Exjade používán
Neužívejte EXJADE
- jestliže jste alergický (á) na deferasirox nebo na kteroukoli další složku tohoto přípravku. Pokud se vás to týká, řekněte to svému lékaři dříve, než začnete užívat EXJADE.Pokud si myslíte, že byste mohli být alergičtí, poraďte se se svým lékařem.
- jestliže máte středně závažné nebo závažné onemocnění ledvin.
- jestliže v současné době užíváte jiné léky na chelaci železa.
EXJADE se nedoporučuje
- jestliže jste v pokročilém stádiu myelodysplastického syndromu (MDS: snížená tvorba krevních buněk v kostní dřeni) nebo máte pokročilé nádorové onemocnění.
Opatření pro použití Co potřebujete vědět před užitím přípravku Exjade
Před užitím přípravku EXJADE se poraďte se svým lékařem nebo lékárníkem:
- jestliže máte problémy s ledvinami nebo játry.
- pokud máte srdeční potíže kvůli přetížení železem.
- pokud zaznamenáte výrazné snížení výdeje moči (známka problému s ledvinami).
- jestliže máte závažnou kožní vyrážku nebo potíže s dýcháním a závratě nebo otoky zejména obličeje a krku (příznaky závažné alergické reakce).
- pokud máte vyrážku, zarudlou kůži, puchýře na rtech, očích nebo ústech, olupování kůže, horečku (příznaky závažné kožní reakce)
- pokud se u vás objeví kombinace ospalosti, bolesti v pravé horní části břicha, zežloutnutí nebo zvýšené žloutnutí kůže nebo očí a tmavá moč (příznaky problémů s játry).
- pokud zvracíte krev a / nebo máte černou stolici.
- pokud pociťujete časté bolesti břicha, zejména po jídle nebo po užití přípravku EXJADE.
- pokud trpíte častým pálením žáhy.
- jestliže máte v krevních testech nízké hladiny krevních destiček nebo bílých krvinek.
- pokud máte rozmazané vidění.
- jestliže máte průjem nebo zvracení.
Pokud se vás cokoli z výše uvedeného týká, okamžitě to sdělte svému lékaři.
Monitorování léčby přípravkem EXJADE
Během léčby budete pravidelně testovat krev a moč. Zkontrolují množství železa ve vašem těle (hladina feritinu v krvi), aby zjistili, jak přípravek EXJADE funguje. Testy také zkontrolují funkci ledvin (hladina kreatininu v krvi, přítomnost bílkovin v moči) a funkci jater (hladina transaminázy v krvi). Váš lékař vás může požádat o provedení biopsie ledvin, pokud má podezření na závažné poškození ledvin. Játra mohou být také podrobena testům zobrazování magnetickou rezonancí (MRI) ke stanovení množství železa v játrech. Váš lékař vyhodnotí tyto testy, aby rozhodl, která dávka přípravku EXJADE je pro vás nejvhodnější, a také tyto testy použije k rozhodnutí, kdy ukončit užívání přípravku EXJADE.
Jako preventivní opatření bude každý rok během léčby vyšetřen váš zrak a sluch.
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Exjade
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval (a) nebo které možná budete užívat. To platí zejména pro:
- jiné chelátory železa, které by neměly být užívány s EXJADE,
- antacida (léky používané k léčbě pálení žáhy) obsahující hliník, které se nesmí užívat ve stejnou denní dobu jako EXJADE,
- cyklosporin (používá se k prevenci odmítnutí transplantovaného orgánu nebo k jiným stavům, jako je revmatoidní artritida nebo atopická dermatitida),
- simvastatin (používaný ke snížení cholesterolu),
- některé léky proti bolesti nebo protizánětlivé léky (např. aspirin, ibuprofen, kortikosteroidy),
- perorální bisfosfonáty (používané k léčbě osteoporózy),
- antikoagulační léky (používané k prevenci nebo léčbě srážení krve),
- hormonální antikoncepce (antikoncepční léky),
- bepridil, ergotamin (používá se při srdečních problémech a migréně),
- repaglinid (používaný k léčbě cukrovky),
- rifampicin (používá se k léčbě tuberkulózy),
- fenytoin, fenobarbital, karbamazepin (používané k léčbě epilepsie),
- ritonavir (používaný k léčbě infekce HIV),
- paklitaxel (používá se k léčbě rakoviny),
- teofylin (používá se k léčbě respiračních onemocnění, jako je astma),
- klozapin (používá se k léčbě psychiatrických poruch, jako je schizofrenie)
- tizanidin (používá se jako svalový relaxant),
- cholestyramin (používá se ke snížení hladiny cholesterolu v krvi).
Ke sledování hladin některých těchto léků v krvi mohou být zapotřebí další testy.
Varování Je důležité vědět, že:
Starší lidé (65 let nebo starší)
Přípravek EXJADE mohou používat lidé ve věku 65 let a starší ve stejné dávce jako dospělí. Starší pacienti mohou mít více nežádoucích účinků (zejména průjem) než mladší pacienti. Lékař by je měl pečlivě sledovat kvůli nežádoucím účinkům, které mohou vyžadovat úpravu dávky.
Děti a dospívající
EXJADE lze použít u dětí a dospívajících, kteří dostávají pravidelné krevní transfuze ve věku 2 let a starší, a u dětí a dospívajících, kteří nedostávají pravidelné krevní transfuze ve věku 10 let a starší. Lékař upraví dávku na základě růstu pacienta
EXJADE se nedoporučuje u dětí mladších 2 let.
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat.
EXJADE se během těhotenství nedoporučuje, pokud to není nezbytně nutné.
Pokud v současné době používáte perorální antikoncepci nebo antikoncepční náplast k zabránění otěhotnění, musíte použít další nebo jiný typ antikoncepce (např. Kondomy), protože EXJADE může snížit účinnost orální a náplasti.
Kojení se během léčby přípravkem EXJADE nedoporučuje.
Řízení dopravních prostředků a obsluha strojů
Pokud se vám po užití přípravku EXJADE zatočí hlava, neřiďte dopravní prostředky ani neobsluhujte žádné stroje nebo stroje, dokud už nebudete pociťovat závrať.
EXJADE obsahuje laktózu
Pokud vám lékař řekl, že nesnášíte některé cukry, kontaktujte svého lékaře před užitím tohoto léčivého přípravku.
Dávka, způsob a doba podání Jak používat Exjade: Dávkování
Léčba přípravkem EXJADE bude pod dohledem lékaře, který má zkušenosti s léčbou přetížení železem způsobeného transfuzí krve.
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře. Pokud máte pochybnosti, poraďte se se svým lékařem nebo lékárníkem.
Kolik EXJADE vzít
- Obvyklá denní dávka potahovaných tablet EXJADE na začátku léčby u pacientů, kteří dostávají pravidelné krevní transfuze, je 14 mg na kilogram tělesné hmotnosti. Lékař vám může doporučit vyšší nebo nižší počáteční dávku podle potřeby individuální léčby.
- Obvyklá denní dávka potahovaných tablet EXJADE na začátku léčby u pacientů, kteří nedostávají pravidelné krevní transfuze, 7 mg na kilogram tělesné hmotnosti e.
- V závislosti na tom, jak reagujete na léčbu, může lékař následně změnit vaši léčbu zvýšením nebo snížením dávky.
- Maximální doporučená denní dávka potahovaných tablet EXJADE je:
- 28 mg na kilogram tělesné hmotnosti u pacientů, kteří dostávají pravidelné krevní transfuze,
- 14 mg na kilogram tělesné hmotnosti u dospělých pacientů, kteří nedostávají pravidelné krevní transfuze,
- 7 mg na kilogram tělesné hmotnosti u dětí a dospívajících, kteří nedostávají pravidelné krevní transfuze.
Deferasirox je také k dispozici ve formě „dispergovatelných“ tablet. Pokud přecházíte z dispergovatelných tablet na tyto potahované tablety, bude nutná úprava dávky.
Kdy užívat EXJADE
- Užívejte EXJADE jednou denně, každý den, přibližně ve stejnou dobu každý den s trochou vody.
- Užívejte potahované tablety EXJADE na prázdný žaludek nebo s lehkým jídlem. Užívání EXJADE každý den ve stejnou dobu vám také pomůže zapamatovat si, kdy máte tablety užít.
U pacientů, kteří nemohou polykat tablety celé, mohou být potahované tablety EXJADE rozdrceny a podány rozetřením celé dávky na měkké jídlo, jako je jogurt nebo jablečné pyré (čisté jablko). Jídlo je nutné konzumovat okamžitě a úplně. Nenechávejte si jej pro budoucí použití.
Jak dlouho přípravek EXJADE užívat
Užívejte EXJADE každý den tak dlouho, jak vám řekne lékař. Jedná se o dlouhodobou léčbu, která může trvat měsíce nebo roky. Váš lékař bude Váš lékař pravidelně kontrolovat, aby zkontroloval, zda je léčba účinná (viz také bod 2: „Sledování léčby přípravkem EXJADE“).
Máte -li jakékoli dotazy, jak dlouho přípravek EXJADE užívat, promluvte si se svým lékařem.
Jestliže jste zapomněl (a) užít EXJADE
Pokud zapomenete užít dávku, vezměte si ji hned, jak si během toho dne vzpomenete. Užijte další dávku podle plánu. Následující den neužívejte dvojnásobnou dávku, abyste nahradili zapomenutou tabletu (tablety).
Jestliže jste přestal (a) užívat EXJADE
Nepřestávejte užívat EXJADE, pokud vám to lékař neřekne. Pokud přestanete užívat, přebytečné železo již nebude z vašeho těla odstraněno (viz také výše v části „Jak dlouho užívat EXJADE“).
Předávkování Co dělat, když jste užil příliš mnoho přípravku Exjade
Pokud jste užil příliš mnoho EXJADE nebo pokud někdo jiný omylem užil Vaše tablety, okamžitě kontaktujte svého lékaře nebo nemocnici o radu. Ukažte jim balení tablet. Možná budete potřebovat lékařské ošetření.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Exjade
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Většina nežádoucích účinků je mírná až středně závažná a obvykle odezní po léčebném období mezi několika dny a několika týdny.
Některé nežádoucí účinky mohou být závažné a vyžadují okamžitou lékařskou pomoc.
Tyto nežádoucí účinky jsou méně časté (mohou postihnout až 1 z 100 lidí) nebo vzácné (mohou postihnout až 1 z 1000 lidí).
- Jestliže máte závažnou kožní vyrážku nebo potíže s dýcháním a závratě nebo otoky hlavně obličeje a krku (příznaky závažné alergické reakce),
- Pokud máte závažnou vyrážku, zarudlou kůži, puchýře na rtech, v očích nebo v ústech, olupování kůže, horečku (příznaky závažné kožní reakce),
- Pokud zaznamenáte výrazné snížení výdeje moči (známka problému s ledvinami),
- Pokud se u vás objeví kombinace ospalosti, bolesti v pravé horní části břicha, zežloutnutí nebo zvýšené žloutnutí kůže nebo očí a tmavá moč (příznaky problémů s játry),
- Pokud zvracíte krev a / nebo máte černou stolici,
- Pokud pociťujete častou bolest břicha, zejména po jídle nebo po užití přípravku EXJADE,
- Pokud máte časté pálení žáhy,
- Pokud pocítíte částečnou ztrátu zraku,
- Pokud pocítíte silnou bolest v horní části břicha (pankreatitida), přestaňte tento přípravek užívat a ihned to sdělte svému lékaři.
Některé nežádoucí účinky mohou být závažné.
Tyto nežádoucí účinky jsou neobvyklé.
- Pokud máte rozmazané nebo rozmazané vidění,
- Pokud máte snížený sluch,
řekněte to svému lékaři co nejdříve.
Jiné nežádoucí účinky
Velmi časté (mohou postihnout více než 1 z 10 lidí)
- Změny ve funkčních testech ledvin.
Časté (mohou postihnout až 1 z 10 lidí)
- Gastrointestinální poruchy, jako je nevolnost, zvracení, průjem, bolest břicha, nadýmání, zácpa, poruchy trávení
- Vyrážka
- Bolest hlavy
- Abnormální testy jaterních funkcí
- Svědění
- Abnormální test moči (bílkovina v moči)
Pokud vás některý z těchto stavů závažně postihne, sdělte to svému lékaři.
Méně časté (mohou postihnout až 1 ze 100 lidí)
- Závrať
- Horečka
- Bolest krku
- Otoky paží nebo nohou
- Změna barvy kůže
- Úzkost
- Poruchy spánku
- Únava
Pokud se některý z těchto účinků vyskytne závažně, sdělte to svému lékaři.
Frekvence není známa (frekvenci nelze z dostupných údajů určit).
- Snížení počtu buněk podílejících se na srážení krve (trombocytopenie), počtu červených krvinek (zhoršení „anémie), počtu bílých krvinek (neutropenie) nebo počtu všech typů krvinek ( pancytopenie)
- Ztráta vlasů
- Ledvinové kameny
- Nízký výdej moči
- Slza ve stěně žaludku nebo střev, která může být bolestivá a způsobit nevolnost
- Silná bolest v horní části břicha (pankreatitida)
- Zvýšená kyselost krve (metabolická acidóza).
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
Expirace a retence
- Uchovávejte tento přípravek mimo dohled a dosah dětí.
- Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na blistru za EXP a na krabičce za EXP. Datum exspirace se vztahuje k poslednímu dni uvedeného měsíce.
- Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
- Nepoužívejte poškozené obaly nebo známky poškození.
- Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Jiná informace
Co EXJADE obsahuje
Léčivou látkou je deferasirox.
Jedna potahovaná tableta EXJADE 90 mg obsahuje deferasirox 90 mg.
Jedna potahovaná tableta EXJADE 180 mg obsahuje deferasiroxum 180 mg.
Jedna potahovaná tableta EXJADE 360 mg obsahuje deferasirox 360 mg.
Dalšími složkami jsou mikrokrystalická celulóza; krospovidon; povidon (K30); stearát hořečnatý; koloidní bezvodý oxid křemičitý a poloxamer 188.Potah tablety obsahuje: hypromelózu; oxid titaničitý (E171); makrogol; mastek; hlinitý lak indigokarmínu (E132).
Popis, jak vypadá EXJADE a obsah balíčku
EXJADE je dodáván ve formě potahovaných tablet. Potahované tablety jsou oválné a bikonvexní.
EXJADE 90 mg potahované tablety jsou světle modré a na jedné straně mají označení „90“ a na druhé „NVR“.
EXJADE 180 mg potahované tablety jsou středně modré a označené „180“ na jedné straně a „NVR“ na druhé straně.
EXJADE 360 mg potahované tablety jsou tmavě modré s označením „360“ na jedné straně a „NVR“ na druhé straně.
Jedno balení obsahuje 30 nebo 90 potahovaných tablet v blistrech. Více balení obsahuje 300 (10 balení po 30) potahovaných tablet.
Ve vaší zemi nemusí být uvedeny na trh všechny velikosti nebo síly balení.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
EXJADE
▼ Léčivý přípravek podléhá dalšímu sledování. To umožní rychlou identifikaci nových bezpečnostních informací. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky. Informace o hlášení nežádoucích účinků viz bod 4.8.
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
EXJADE 90 mg potahované tablety
Jedna potahovaná tableta obsahuje 90 mg deferasiroxu.
EXJADE 180 mg potahované tablety
Jedna potahovaná tableta obsahuje deferasiroxum 180 mg.
EXJADE 360 mg potahované tablety
Jedna potahovaná tableta obsahuje deferasiroxum 360 mg.
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Potahovaná tableta
EXJADE 90 mg potahované tablety
Světle modrá, oválná, bikonvexní potahovaná tableta se zkosenými hranami a s potiskem NVR na jedné straně a 90 na druhé. Přibližná velikost tablety 10,7 mm x 4,2 mm.
EXJADE 180 mg potahované tablety
Středně modré, oválné, bikonvexní potahované tablety se zkosenými hranami a s potiskem NVR na jedné straně a 180 na druhé. Přibližná velikost tablety 14 mm x 5,5 mm.
EXJADE 360 mg potahované tablety
Tmavě modrá, oválná, bikonvexní potahovaná tableta se zkosenými hranami a s potiskem NVR na jedné straně a 360 na druhé. Přibližná velikost tablety 17 mm x 6,7 mm.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
EXJADE je indikován k léčbě chronického přetížení železa v důsledku častých krevních transfuzí (≥ 7 ml / kg / měsíc koncentrovaných červených krvinek) u pacientů s beta thalassemia major ve věku 6 let a starší.
EXJADE je také indikován k léčbě chronického přetížení železa v důsledku krevních transfuzí, pokud je léčba deferoxaminem kontraindikována nebo nedostatečná u následujících skupin pacientů:
- u pediatrických pacientů s beta thalassemií major s přetížením železem v důsledku častých krevních transfuzí (≥7 ml / kg / měsíc koncentrovaných červených krvinek) ve věku od 2 do 5 let,
- u dospělých a pediatrických pacientů s beta thalassemia major s přetížením železem v důsledku vzácných krevních transfuzí (
- u dospělých a dětských pacientů s jinou anémií ve věku 2 let a starších.
EXJADE je také indikován k léčbě chronického přetížení železem vyžadujícího chelatační terapii, pokud je léčba deferoxaminem kontraindikována nebo neadekvátní u pacientů s thalassemickými syndromy nezávislými na transfuzi ve věku 10 let a starší.
04.2 Dávkování a způsob podání
Léčbu přípravkem EXJADE by měli zahájit a udržovat lékaři se zkušenostmi s léčbou chronického přetížení železem.
Dávkování
Přetížení železa v důsledku transfuze krve
Doporučuje se zahájit léčbu po transfuzi přibližně 20 jednotek (přibližně 100 ml / kg) koncentrovaných červených krvinek (RBC) nebo pokud klinické sledování prokazuje přítomnost chronického přetížení železem (např. Sérový feritin> 1 000 mcg / l). Dávky (v mg / kg) by měly být vypočítány a zaokrouhleny na nejbližší celou tabletu.
Cílem terapie chelatací železa je eliminovat množství železa podávaného při transfuzích a podle potřeby snížit stávající zatížení železem.
Potahované tablety EXJADE vykazují vyšší biologickou dostupnost než formulace dispergovatelných tablet EXJADE (viz bod 5.2). V případě přechodu z dispergovatelných tablet na potahované tablety by měla být dávka potahovaných tablet o 30% nižší než dávka dispergovatelných tablet zaokrouhlená na nejbližší celou tabletu.
Odpovídající dávky pro obě formulace jsou uvedeny v tabulce níže.
Tabulka 1 Doporučené dávky při přetížení železem v důsledku transfuzí krve
Počáteční dávka
Doporučená počáteční denní dávka potahovaných tablet EXJADE je 14 mg / kg tělesné hmotnosti.
Počáteční denní dávku 21 mg / kg lze zvážit u pacientů, kteří potřebují snížit vysoké hladiny železa v těle a kteří také dostávají GRC více než 14 ml / kg / měsíc (přibližně> 4 jednotky / měsíc u dospělého).
Počáteční denní dávku 7 mg / kg lze zvážit u pacientů, kteří nepotřebují snižovat hladinu železa v těle a kteří také dostávají GRC méně než 7 ml / kg / měsíc (přibližně
U pacientů, kteří jsou již dostatečně léčeni deferoxaminem, lze zvážit počáteční dávku potahovaných tablet EXJADE, která je číselně jedna třetina dávky deferoxaminu (např. Pacient, který dostává 40 mg / kg / den deferoxaminu po dobu 5 dnů v týdnu (nebo ekvivalent) může přejít na počáteční denní dávku 14 mg / kg / den potahovaných tablet EXJADE). Pokud to vede k denní dávce nižší než 14 mg / kg tělesné hmotnosti, je třeba sledovat odpověď pacienta a pokud není dosaženo dostatečné účinnosti, je třeba zvážit zvýšení dávky (viz bod 5.1).
Úprava dávky
Doporučuje se monitorovat sérový feritin každý měsíc a v případě potřeby upravit dávku přípravku EXJADE každých 3-6 měsíců na základě trendu hodnot sérového feritinu. Úpravu dávky lze provádět v intervalech mezi 3, 5 a 7 mg / kg a měly by být přizpůsobeny individuální odpovědi pacienta a terapeutickým cílům (udržení nebo snížení zátěže železem) .U pacientů nedostatečně kontrolovaných dávkami 21 mg / kg (např. sérové hladiny feritinu trvale nad 2500 mcg / l a nevykazující klesající trend lze považovat za dávky až do 28 mg / kg. Dostupnost dlouhodobých údajů o účinnosti a bezpečnosti s dispergovatelnými tabletami EXJADE používanými v dávkách nad 30 mg / kg je v současné době omezená (264 pacientů sledovalo v průměru 1 rok po eskalace dávky). Pokud je při dávkách až 21 mg / kg dosaženo jen velmi špatné kontroly hemosiderózy, další zvýšení (maximálně na 28 mg / kg) nemusí dosáhnout uspokojivé kontroly a lze zvážit alternativní možnosti léčby. Pokud není dosažena uspokojivá kontrola při dávkách vyšších než 21 mg / kg, léčba těmito dávkami by neměla pokračovat a pokud je to možné, měly by být zváženy alternativní možnosti léčby. Dávky nad 28 mg / kg se nedoporučují, protože s dávkami nad tuto úroveň jsou pouze omezené zkušenosti.
U pacientů léčených dávkami vyššími než 21 mg / kg by mělo být zváženo snížení dávky v rozmezí 3,5 až 7 mg / kg, pokud bylo dosaženo kontroly (např. Sérové hladiny feritinu trvale pod 2 500 mcg / le, které v průběhu času vykazují klesající trend). U pacientů, jejichž hladina feritinu v séru dosáhla referenční hodnoty (obvykle mezi 500 a 1 000 mcg / l), by mělo být zváženo snížení dávky v rozmezí 3,5 až 7 mg / kg, aby se udržely hladiny v krvi. Feritin v séru v referenčním rozmezí. feritin trvale klesá pod 500 mcg / l, je třeba zvážit přerušení léčby (viz bod 4.4).
Syndrom talasemie nezávislý na transfuzi
Chelatační terapie by měla být zahájena pouze tehdy, pokud existují známky přetížení železem (koncentrace železa v játrech (LIC) ≥ 5 mg Fe / g / dw nebo sérový feritin konzistentně> 800 mcg / l). LIC je preferovanou metodou pro stanovení přetížení železem a měl by být používán všude tam, kde je k dispozici. Při chelatační terapii je u všech pacientů nutná opatrnost, aby se minimalizovalo riziko nadměrné chelace.
Potahované tablety EXJADE vykazují vyšší biologickou dostupnost než formulace dispergovatelných tablet EXJADE (viz bod 5.2). V případě přechodu z dispergovatelných tablet na potahované tablety by měla být dávka potahovaných tablet o 30% nižší než dávka dispergovatelných tablet zaokrouhlená na nejbližší celou tabletu.
Odpovídající dávky pro obě formulace jsou uvedeny v tabulce níže.
Tabulka 2 Doporučené dávky pro syndromy talasemie nezávislé na transfuzi
* LIC je preferovanou metodou pro stanovení přetížení železem.
Počáteční dávka
U pacientů se syndromy talasemie nezávislými na transfuzi je doporučená počáteční denní dávka potahovaných tablet EXJADE 7 mg / kg tělesné hmotnosti.
Úprava dávky
Doporučuje se monitorovat sérový feritin měsíčně. Po každých 3–6 měsících léčby je třeba zvážit zvyšování dávky v přírůstcích 3,5 až 7 mg / kg, pokud je LIC pacienta ≥ 7 mg Fe / g dw, nebo pokud je sérový feritin trvale> 2000 mcg / l a není vykazují klesající trend a pokud pacient lék dobře snáší. Dávky vyšší než 14 mg / kg se nedoporučují, protože nejsou žádné zkušenosti s dávkami nad touto úrovní u pacientů se syndromy talasemie nezávislými na transfuzi.
U pacientů, u kterých nebyl hodnocen LIC a sérový feritin je ≤2000 mcg / l, by dávka neměla překročit 7 mg / kg.
U pacientů, jejichž dávka byla zvýšena nad 7 mg / kg, se při snížení LIC doporučuje snížení dávky na 7 mg / kg nebo méně
Přerušení léčby
Léčba by měla být ukončena, jakmile bude dosaženo uspokojivé hladiny železa v těle (LIC
Zvláštní kategorie pacientů
Starší pacienti (≥65 let)
Doporučené dávkování pro starší pacienty je stejné jako výše popsané. V klinických studiích zaznamenali starší pacienti vyšší frekvenci nežádoucích účinků než mladší pacienti (zejména průjem) a měli by být pečlivě sledováni z hlediska nežádoucích účinků, které mohou vyžadovat úpravu dávky.
Pediatrická populace
Přetížení železa v důsledku transfuze krve:
Doporučené dávkování u pediatrických pacientů ve věku 2-17 let s přetížením železem v důsledku krevních transfuzí je stejné jako u dospělých pacientů. Výpočet dávky by měl vzít v úvahu změny hmotnosti dětských pacientů v průběhu času.
U dětí s přetížením železem v důsledku krevních transfuzí ve věku 2 až 5 let je expozice nižší než u dospělých (viz bod 5.2). V důsledku toho mohou pacienti v této věkové skupině vyžadovat vyšší dávky, než je požadováno. U dospělých by však počáteční dávka měla být stejné jako u dospělých, s následnou individuální titrací.
Syndrom talasemie nezávislý na transfuzi:
U pediatrických pacientů se syndromy talasemie nezávislými na transfuzi by dávka neměla překročit 7 mg / kg. U těchto pacientů je přísnější kontrola LIC a sérového feritinu nezbytná k zamezení nadměrné chelace: kromě měsíčního hodnocení sérového feritinu by měl být LIC kontrolován každé 3 měsíce, pokud je sérový feritin ≤ 800 mcg / l.
Děti od narození do 23 měsíců:
Bezpečnost a účinnost EXJADE u kojenců od narození do 23 měsíců věku nebyla stanovena. Nejsou k dispozici žádné údaje.
Pacienti s poruchou funkce ledvin
EXJADE nebyl studován u pacientů s poruchou funkce ledvin a je kontraindikován u pacientů s odhadovanou clearance kreatininu.
Pacienti s poruchou funkce jater
EXJADE se nedoporučuje u pacientů s těžkou poruchou funkce jater (Child-Pugh třída C). U pacientů se středně těžkou poruchou funkce jater (Child-Pugh třída B) by měla být dávka výrazně snížena a následně postupným zvyšováním až na hranici 50% (viz body 4.4 a 5.2) a EXJADE by měl být používán s opatrností. takoví pacienti. Jaterní funkce by měla být zkontrolována u všech pacientů před léčbou, každé 2 týdny během prvního měsíce a poté každý měsíc (viz bod 4.4).
Způsob podání
K perorálnímu podání.
Potahované tablety se polykají celé s trochou vody. U pacientů, kteří nemohou polykat celé tablety, mohou být potahované tablety rozdrceny a podány rozetřením celé dávky na měkké jídlo, jako je jogurt nebo jablečné pyré (jablečné pyré) Porce by měla být spotřebována okamžitě a úplně a neměla by být skladována pro budoucí použití.
Potahované tablety se užívají jednou denně, nejlépe každý den ve stejnou dobu, a lze je užít na prázdný žaludek nebo s lehkým jídlem (viz body 4.5 a 5.2).
04.3 Kontraindikace
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Kombinace s jinými terapiemi chelatujícími železo, protože bezpečnost těchto kombinací nebyla stanovena (viz bod 4.5).
Pacienti s odhadovanou clearance kreatininu
04.4 Zvláštní upozornění a vhodná opatření pro použití
Funkce ledvin
Deferasirox byl studován pouze u pacientů s výchozím sérovým kreatininem v normálním rozmezí odpovídajícím věku.
Během klinických studií došlo u přibližně 36% pacientů ke zvýšení sérového kreatininu o> 33% při ≥ 2 po sobě jdoucích příležitostech, někdy nad horní hranici normálního rozmezí. Toto zvýšení bylo závislé na dávce. Přibližně ve dvou třetinách u pacientů, u nichž došlo ke zvýšení sérového kreatininu, se hladina vrátila na hodnoty pod 33% bez úpravy dávky. U zbývajících pacientů zvýšení sérového kreatininu ne vždy odpovídalo na snížení dávky nebo „Přerušení léčby. V některých případech po snížení dávky byla pozorována pouze stabilizace hodnot kreatininu v séru.Po uvedení deferasiroxu na trh bylo hlášeno akutní selhání ledvin (viz bod 4.8) .V některých z těchto případů vedlo postmarketingové zhoršení funkce ledvin k selhání ledvin vyžadujícímu dočasné nebo permanentní dialýza.
Příčiny zvýšení sérového kreatininu nebyly objasněny.Proto je třeba věnovat zvláštní pozornost monitorování sérového kreatininu u pacientů, kteří současně užívají léčivé přípravky tlumící ledviny, a u pacientů, kteří dostávají vysoké dávky deferasiroxu a / nebo nízkou frekvenci krevních transfuzí (
Před zahájením léčby se doporučuje dvakrát vyhodnotit sérový kreatinin. Sérový kreatinin, clearance kreatininu (odhadováno pomocí Cockcroft-Gaultova vzorce nebo MDRD u dospělých a Schwartzova vzorce u dětí) a / nebo plazmatické hladiny cystatinu C by měly být monitorovány před zahájením léčby, jednou týdně v prvním měsíci po zahájení nebo úpravě terapie EXJADE (včetně změna formulace) a poté jednou za měsíc.U pacientů s anamnézou problémů s ledvinami a pacientů užívajících léky snižující funkci ledvin může být zvýšené riziko komplikací.U pacientů s průjmem nebo zvracením je třeba dbát na dostatečnou hydrataci.
Během postmarketingové léčby deferasiroxem byly hlášeny případy metabolické acidózy. Většina těchto pacientů měla poškození ledvin, renální tubulopatii (Fanconiho syndrom) nebo průjem nebo stavy, při nichž je acidobazická nerovnováha známou komplikací. V těchto populacích by měla být acidobazická rovnováha monitorována, jak je klinicky indikováno. U pacientů s metabolickou acidózou by mělo být zváženo ukončení léčby přípravkem EXJADE.
Tabulka 3 Úprava dávky a přerušení léčby pro sledování ledvin
Léčbu lze obnovit v závislosti na individuálních klinických okolnostech.
Snížení dávky nebo přerušení léčby lze také zvážit, pokud dojde k abnormálním hladinám markerů tubulární funkce a / nebo pokud je to klinicky indikováno:
• Proteinurie (test musí být proveden před zahájením terapie a poté jednou za měsíc).
• Glykosurie u nediabetických pacientů a nízké sérové hladiny draslíku, fosfátu, hořčíku nebo urátu, fosfaturie, aminoacidurie (monitorujte podle potřeby).
Renální tubulopatie byla hlášena hlavně u dětí a dospívajících s beta-talasemií léčených přípravkem EXJADE.
Pacienti by měli být odesláni k nefrologovi a mohou být zvážena další specializovaná vyšetření (jako je renální biopsie), pokud dojde ke snížení dávky nebo přerušení léčby:
• Kreatinin v séru, který zůstává výrazně zvýšený, např
• Trvalá abnormalita v jiném markeru funkce ledvin (např. Proteinurie, Fanconiho syndrom).
Jaterní funkce
U pacientů léčených deferasiroxem bylo pozorováno zvýšení jaterních testů. U pacientů léčených deferasiroxem byly po uvedení přípravku na trh hlášeny případy selhání jater, některé s fatálním koncem. Většina případů jaterního selhání se týkala pacientů s významnou morbiditou, včetně již existující jaterní cirhózy. Roli deferasiroxu jako přispívajícího nebo přitěžujícího faktoru však nelze vyloučit (viz bod 4.8).
Doporučuje se před zahájením léčby, každé 2 týdny během prvního měsíce a poté měsíčně, zkontrolovat sérové transaminázy, bilirubin a alkalickou fosfatázu. Pokud dochází k trvalému a progresivnímu zvyšování hladin sérových transamináz, které nelze přičíst jiným příčinám, měl by přípravek EXJADE Jakmile bude objasněna příčina abnormalit funkce jaterních testů nebo po návratu k normálním hodnotám, je možné zvážit opatrné obnovení léčby nižší dávkou a následně postupné zvyšování dávky.
EXJADE se nedoporučuje u pacientů s těžkou poruchou funkce jater (Child-Pugh třída C) (viz bod 5.2).
Tabulka 4 Souhrn doporučení pro monitorování bezpečnosti
U pacientů s krátkou délkou života (např. Vysoce rizikové myolodysplastické syndromy), zejména pokud souběžná morbidita může zvýšit riziko nežádoucích účinků, může být přínos přípravku EXJADE omezený a menší než rizika. V důsledku toho se léčba přípravkem EXJADE u těchto pacientů nedoporučuje.
U starších pacientů je nutná opatrnost kvůli vyšší frekvenci nežádoucích účinků (zejména průjmu).
Údaje u dětí s talasemií nezávislou na transfuzi jsou velmi omezené (viz bod 5.1). V důsledku toho by u pediatrické populace měla být léčba EXJADE velmi pečlivě sledována z hlediska nežádoucích účinků a monitorována zátěž železem. Kromě toho by si lékaři před léčbou dětí s talasemií nezávislou na transfuzích a nadměrným přetížením železem přípravkem EXJADE měli uvědomit, že důsledky dlouhodobé expozice u těchto pacientů nejsou v současné době známy.
Gastrointestinální poruchy
U pacientů užívajících deferasirox, včetně dětí a dospívajících, byly hlášeny vředy v horní části gastrointestinálního traktu a krvácení. U některých pacientů bylo pozorováno mnohočetné vředy (viz bod 4.8). Byly hlášeny komplikované vředy s perforací trávicího systému.Byly také hlášeny smrtelné gastrointestinální krvácení, zejména u starších pacientů, kteří měli hematologické malignity a / nebo nízký počet krevních destiček.Lékaři a pacienti by měli být během léčby přípravkem EXJADE poučeni. věnujte pozornost vzniku známek a příznaků gastrointestinálních ulcerací a krvácení a v případě podezření na závažnou gastrointestinální nežádoucí reakci okamžitě zahajte hodnocení a souběžnou léčbu. Opatrnosti je třeba u pacientů užívajících přípravek EXJADE v kombinaci s látkami, které mají rozpoznatelný ulcerogenní potenciál, jako jsou nesteroidní protizánětlivé léky, kortikosteroidy nebo perorální bisfosfonáty, u pacientů užívajících antikoagulancia a u pacientů s počtem krevních destiček pod 50 000. / Mm3 (50 x 109 / l) (viz bod 4.5).
Kožní poruchy
Během léčby přípravkem EXJADE se mohou objevit kožní vyrážky. Ve většině případů vyrážky spontánně odezní. Pokud je nutné přerušení léčby, lze léčbu obnovit poté, co erupce odezní, nižší dávkou, kterou je možné postupně zvyšovat. V závažných případech lze obnovení léčby provést ve spojení s orálním podáním steroidů na krátkou dobu. Po uvedení přípravku na trh byly hlášeny případy Stevens-Johnsonova syndromu (SJS) a toxické epidermální nekrolýzy (TEN). Nelze vyloučit riziko dalších závažnějších kožních reakcí včetně DRESS (léková reakce s eozinofilií a systémovými příznaky). Pokud je podezření na SJS nebo jakoukoli jinou závažnou kožní reakci, přípravek EXJADE musí být okamžitě vysazen a nesmí být znovu zaveden.
Reakce přecitlivělosti
U pacientů léčených deferasiroxem byly hlášeny případy závažných reakcí z přecitlivělosti (jako je anafylaxe a angioedém), které se ve většině případů objevily během prvního měsíce léčby (viz bod 4.8). Pokud k takovým reakcím dojde, je třeba léčbu přípravkem EXJADE přerušit a zahájit příslušnou lékařskou intervenci. Vzhledem k riziku anafylaktického šoku by deferasirox neměl být znovu podáván pacientům, u kterých se vyskytla reakce z přecitlivělosti (viz bod 4.3).
Zrak a sluch
Byly hlášeny poruchy sluchu (ztráta sluchu) a zraku (zakalení čočky) (viz bod 4.8). Doporučuje se provést sluchová a oční vyšetření (včetně fundoskopie) před zahájením léčby a poté v pravidelných intervalech (každých 12 měsíců) .Pokud jsou během léčby zaznamenány poruchy, lze zvážit snížení dávky nebo přerušení léčby.
Krevní poruchy
U pacientů léčených deferasiroxem byly po uvedení na trh hlášeny případy leukopenie, trombocytopenie nebo pancytopenie (nebo zhoršení těchto cytopenií) a zhoršení anémie.Většina z těchto pacientů měla již existující hematologické poruchy, které jsou často spojeny s nedostatečným krevním tlakem. Nelze však vyloučit přispívající nebo přitěžující úlohu léčby.U pacientů, u nichž se rozvine cytopenie, kterou nelze přičíst žádné příčině, by mělo být zváženo ukončení léčby.
Další úvahy
Doporučuje se monitorovat sérové hladiny feritinu měsíčně, aby se vyhodnotila reakce pacienta na léčbu (viz bod 4.2). Pokud sérový feritin trvale klesá pod 500 mcg / l (při přetížení železa v důsledku krevních transfuzí) nebo pod 300 mcg / l (u syndromů talasemie nezávislých na transfuzi), měla by být zvážena možnost „přerušení léčby“.
Výsledky sérového kreatininu, sérového feritinu a sérových transamináz by měly být zaznamenávány a pravidelně vyhodnocovány, aby se sledoval jejich postup.
Ve dvou klinických studiích neměla léčba deferasiroxem po dobu až 5 let vliv na růst a sexuální vývoj pediatrických pacientů (viz bod 4.8). Jako obecné preventivní opatření pro léčbu dětských pacientů s přetížením železem v důsledku transfuzí krve by však měla být před zahájením léčby a v pravidelných intervalech (každých 12 měsíců) sledována tělesná hmotnost, růst a sexuální vývoj.
Srdeční dysfunkce je známou komplikací závažného přetížení železem. U pacientů s těžkým přetížením železem by měly být během dlouhodobé léčby přípravkem EXJADE monitorovány srdeční funkce.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Bezpečnost deferasiroxu v kombinaci s jinými chelátory železa nebyla stanovena. Proto by neměl být kombinován s jinými terapiemi chelatujícími železo (viz bod 4.3).
Interakce s jídlem
C deferasirox potahovaných tablet byl zvýšen (o 29%), pokud byl podáván s jídlem s vysokým obsahem tuku. Potahované tablety EXJADE lze užívat buď na prázdný žaludek nebo s lehkým obědem, nejlépe každý den ve stejnou dobu (viz body 4.2 a 5.2).
Látky, které mohou snížit systémovou expozici přípravku EXJADE
Deferasirox je metabolizován enzymy UGT. Ve studii na zdravých dobrovolnících vedlo současné podávání deferasiroxu (jednorázová dávka 30 mg / kg, dispergovatelná tabletová forma) a rifampicinu, silného induktoru UGT enzymů (opakovaná dávka 600 mg / den) ke snížení o 44%. expozice deferasiroxu (90% CI: 37% - 51%). Proto může současné užívání přípravku EXJADE se silnými induktory UGT enzymů (např. Rifampicin, karbamazepin, fenytoin, fenobarbital, ritonavir) vést ke snížení účinnosti přípravku EXJADE. dávku EXJADE.
V mechanické studii ke stanovení stupně enterohepatální recirkulace cholestyramin významně snížil expozici deferasiroxu (viz bod 5.2).
Interakce s midazolamem a jinými látkami metabolizovanými CYP3A4
Ve studii na zdravých dobrovolnících vedlo současné podávání deferasiroxových dispergovatelných tablet a midazolamu (substrátu cytochromu CYP3A4) ke snížení expozice midazolamu o 17% (90% CI: 8% - 26%). V klinické praxi může tento účinek být výraznější Proto je třeba opatrnosti, pokud je deferasirox kombinován s léky metabolizovanými prostřednictvím CYP3A4 (např. cyklosporin, simvastatin, hormonální antikoncepce, bepridil, ergotamin) vzhledem k možnému snížení jejich účinnosti.
Interakce s repaglinidem a jinými látkami metabolizovanými CYP2C8
Ve studii se zdravými dobrovolníky souběžné podávání deferasiroxu jako středně silného inhibitoru CYP2C8 (30 mg / kg / den, dispergovatelná tabletová formulace) s repaglinidem substrátu CYP2C8, podávané jako jednorázová dávka 0,5 mg, zvýšilo AUC a Cmax repaglinid přibližně 2,3krát (90% CI [2,03-2,63]) respektive 1,6krát (90% CI [1,42-1,84]). "Interakce s dávkami repaglinidu vyššími než 0,5 mg nebyla stanovena," současné užívání je třeba se vyvarovat deferasiroxu s repaglinidem.Pokud se tato kombinace jeví jako nezbytná, mělo by být provedeno pečlivé klinické sledování a monitorování hladiny glukózy v krvi (viz bod 4.4). Interakci mezi deferasiroxem a jinými substráty CYP2C8, jako je paklitaxel, nelze vyloučit.
Interakce s theofylinem a jinými látkami metabolizovanými CYP1A2
Ve studii na zdravých dobrovolnících vedlo souběžné podávání deferasiroxu jako inhibitoru CYP1A2 (opakovaná dávka 30 mg / kg / den ve formě dispergovatelných tablet) a theofylinu, substrátu CYP1A2 (jednorázová dávka 120 mg) k 84% nárůst AUC teofylinu (90% CI: 73% -95%). Jednorázová Cmax nebyla ovlivněna, ale při chronickém podávání se očekává zvýšení Cmax theofylinu. Souběžné užívání deferasiroxu a theofylinu se proto nedoporučuje.Pokud se deferasirox a theofylin používají současně, je třeba zvážit monitorování koncentrace theofylinu a snížení dávky teofylinu. Interakce mezi deferasiroxem a jinými substráty CYP1A2 by neměla být zvažována. vyloučeno. Stejná doporučení týkající se theofylinu platí pro látky, které jsou převážně metabolizovány cytochromem CYP1A2 a které mají úzký terapeutický index (např. Klozapin, tizanidin).
Jiná informace
Souběžné podávání deferasiroxu a antacidových přípravků obsahujících hliník nebylo formálně studováno. Ačkoli má deferasirox nižší afinitu k hliníku než k železu, užívání tablet deferasiroxu s antacidovými přípravky obsahujícími hliník se nedoporučuje.
Souběžné podávání deferasiroxu s látkami, které mají rozpoznaný ulcerogenní potenciál, jako jsou nesteroidní protizánětlivé léky (včetně vysokých dávek kyseliny acetylsalicylové), perorální kortikosteroidy nebo bisfosfonáty, může zvýšit riziko gastrointestinální toxicity (viz bod 4.4). deferasirox s antikoagulancii může také zvýšit riziko gastrointestinálního krvácení. Pokud je deferasirox kombinován s těmito látkami, je nutné pečlivé klinické sledování.
04.6 Těhotenství a kojení
Těhotenství
Pro deferasirox nejsou k dispozici žádné klinické údaje o těhotenství po expozici. Studie na zvířatech prokázaly reprodukční toxicitu při dávkách, které byly shledány toxickými pro matku (viz bod 5.3). Potenciální riziko pro člověka není známo.
Jako preventivní opatření se doporučuje nepoužívat EXJADE během těhotenství, pokud to není nezbytně nutné.
EXJADE může snížit účinnost hormonální antikoncepce (viz bod 4.5) .Ženám ve fertilním věku se doporučuje při používání EXJADE používat doplňkové nebo alternativní nehormonální metody antikoncepce.
Čas krmení
Ve studiích na zvířatech bylo zjištěno, že deferasirox se rychle a extenzivně vylučuje do lidského mléka. Nebyly pozorovány žádné účinky na potomstvo. Není známo, zda se deferasirox vylučuje do lidského mléka. Při užívání přípravku EXJADE se kojení nedoporučuje.
Plodnost
Údaje o fertilitě pro člověka nejsou k dispozici.U zvířat nebyly zjištěny žádné nežádoucí účinky na mužskou nebo ženskou plodnost (viz bod 5.3).
04.7 Účinky na schopnost řídit a obsluhovat stroje
EXJADE má malý vliv na schopnost řídit nebo obsluhovat stroje. Pacienti, kteří zaznamenají závratě, méně časté nežádoucí účinky, by měli být opatrní při řízení nebo obsluze strojů (viz bod 4.8).
04.8 Nežádoucí účinky
Shrnutí bezpečnostního profilu
Mezi nejčastější reakce hlášené během chronické léčby deferasiroxem dispergovatelnými tabletami u dospělých a pediatrických pacientů patří gastrointestinální poruchy (hlavně nauzea, zvracení, průjem nebo bolest břicha) a vyrážka. Průjem byl nejčastěji hlášen u pediatrických pacientů ve věku 2 až 5 let a u starších osob. Tyto reakce jsou závislé na dávce, většinou mírné až střední intenzity, obvykle přechodné a odezní ve většině případů i při pokračující léčbě.
Během klinických studií došlo ke zvýšení dávky kreatininu v séru v závislosti na dávce přibližně u 36% pacientů, i když ve většině případů zůstalo v normálním rozmezí.V prvním roce léčby bylo pozorováno snížení průměrné clearance kreatininu u pediatrických i dospělých pacientů s beta-talasemie a přetížení železem, ale existují důkazy, že se to v dalších letech léčby dále nesnižuje. Bylo hlášeno zvýšení jaterních transamináz. Doporučují se programy monitorování bezpečnosti. pro ledvinové a jaterní parametry Sluchové (snížený sluch) a oční ( poruchy zákalu čočky) jsou neobvyklé a doporučuje se každoroční vyšetření (viz bod 4.4).
Tabulka nežádoucích účinků
Nežádoucí účinky jsou seřazeny níže podle následující konvence: velmi časté (≥ 1/10); časté (≥ 1/100,
Tabulka 5
1 Nežádoucí účinky hlášené ze zkušeností po uvedení na trh Vycházejí ze spontánních hlášení, u nichž není vždy možné spolehlivě stanovit frekvenci nebo příčinný vztah k expozici drogám.
Popis vybraných nežádoucích účinků
Žlučové kameny a související poruchy žlučových cest byly hlášeny přibližně u 2% pacientů. Zvýšení transamináz bylo hlášeno jako nežádoucí účinek u 2% pacientů. Zvýšení transamináz více než 10násobek horní hranice normálního rozmezí, což svědčí pro hepatitidu, bylo neobvyklé (0,3%). Během postmarketingového sledování byla hlášena nedostatečnost přípravku deferasirox ve formě dispergovatelných tablet. Jaterní, někdy fatální, zvláště u pacientů s již existující cirhózou jater (viz bod 4.4). Po uvedení přípravku na trh byly hlášeny případy metabolické acidózy. Většina těchto pacientů měla poškození ledvin, renální tubulopatii (Fanconiho syndrom) nebo průjem nebo stavy, při nichž je acidobazická nerovnováha známou komplikací (viz bod 4.4). Byly pozorovány případy závažné akutní pankreatitidy při absenci dokumentovaných podkladových změn žlučových cest. Stejně jako u jiných léčebných postupů chelatujících železo byla u pacientů léčených deferasiroxem neobvykle pozorována vysokofrekvenční ztráta sluchu a zakalení čočky (časná katarakta) (viz bod 4.4).
Clearance kreatininu při přetížení železem transfuzí
V retrospektivní metaanalýze 2 102 dospělých a pediatrických pacientů s beta-thalassemií s přetížením transfuzí železa léčených deferasiroxem dispergovatelnými tabletami ve dvou randomizovaných klinických studiích a čtyřech otevřených studiích trvajících až pět let byl pozorován pokles hodnoty. clearance kreatininu 13,2% u dospělých pacientů (95% CI: -14,4%, -12,1%; n = 935) a 9,9% u pediatrických pacientů (95% CI: -11, 1%, -8,6%; n = 1142) během prvního roku léčby. U 250 pacientů sledovaných po dobu až pěti let nebyl pozorován žádný další pokles průměrných hladin clearance kreatininu.
Klinické studie u pacientů se syndromy talasemie nezávislými na transfuzi
V roční studii u pacientů se syndromy talasemie nezávislými na transfuzích a přetížením železem (dispergovatelné tablety v dávce 10 mg / kg / den) byly nejčastějšími nežádoucími účinky souvisejícími se studovaným léčivem průjem (9,1%) , vyrážka (9,1%) a nevolnost (7,3%).Změny sérového kreatininu a clearance kreatininu byly hlášeny u 5,5% respektive 1,8% pacientů. Zvýšení hodnot jaterních transamináz větší než 2násobek výchozí hodnoty a 5násobek horní hranice normálu bylo hlášeno u 1,8% pacientů.
Pediatrická populace
Ve dvou klinických studiích neměla léčba deferasiroxem po dobu až 5 let vliv na růst a sexuální vývoj pediatrických pacientů (viz bod 4.4).
Průjem byl hlášen častěji u pediatrických pacientů ve věku 2 až 5 let než u starších pacientů.
Renální tubulopatie byla hlášena hlavně u dětí a dospívajících s beta-talasemií léčených deferasiroxem. V postmarketingových zprávách se „vysoké procento případů metabolické acidózy vyskytlo u dětí v kontextu Fanconiho syndromu“.
Byla hlášena akutní pankreatitida, zejména u dětí a dospívajících.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky, které se vyskytnou po registraci léčivého přípravku, je důležité, protože umožňuje průběžné sledování poměru přínosu a rizika léčivého přípravku. Zdravotničtí pracovníci jsou požádáni, aby hlásili jakékoli podezření na nežádoucí účinky prostřednictvím italské agentury pro léčivé přípravky. , webové stránky: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Předávkování
Byly hlášeny případy předávkování (2–3násobek předepsané dávky po dobu několika týdnů). V jednom případě to vedlo k subklinické hepatitidě, která odezněla po „přerušení léčby. U pacientů s talasemií přetíženou železem jednotlivé dávky 80 mg / kg dispergovatelné tabletové formulace deferasiroxu (což odpovídá dávce 56 mg / kg kg filmové potahované tablety) způsobily mírnou nevolnost a průjem.
Akutní příznaky předávkování mohou zahrnovat nevolnost, zvracení, bolesti hlavy a průjem. Předávkování lze léčit vyvoláním zvracení nebo výplachem žaludku a symptomatickou léčbou.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: chelatační činidla na bázi železa.
ATC kód: V03AC03.
Mechanismus účinku
Deferasirox je orální aktivní chelátor, vysoce selektivní pro železo (III). Jedná se o tridentátní ligand, který váže železo s vysokou afinitou v poměru 2: 1. Deferasirox podporuje vylučování železa hlavně stolicí.Deferasirox má nízkou afinitu k zinku a mědi a nezpůsobuje stálý pokles hladin těchto kovů v séru.
Farmakodynamické účinky
V metabolické studii bilance železa u dospělých pacientů s talasemií s přetížením železem vedl deferasirox v denních dávkách 10, 20 a 40 mg / kg (formulace ve formě dispergovatelných tablet) k průměrnému čistému vylučování 0,119, 0,329 a 0,445 mg. kg tělesné hmotnosti / den.
Klinická účinnost a bezpečnost
Studie klinické účinnosti byly provedeny s dispergovatelnými tabletami deferasiroxu.
Přípravek Deferasirox byl zkoumán u 411 dospělých pacientů (věk ≥ 16 let) a 292 pediatrických pacientů (věk 2 až srpkovitá anémie a jiné vrozené a získané anémie (myelodysplastické syndromy, Diamond-Blackfanův syndrom, aplastická anémie a další velmi vzácné anémie)).
Denní léčba často transfuzovaných dospělých a pediatrických pacientů s beta-talasemií v dávkách 20 a 30 mg / kg formou dispergovatelné tablety deferasiroxu po dobu jednoho roku vedla ke snížení indikátorů celkového tělesného železa; koncentrace železa v játrech byla v průměru snížena přibližně o -0,4 a -8,9 mg Fe / g jater (suchá hmotnost z biopsie) a sérový feritin byl snížen v průměru o -36, respektive -926 mcg / l. Při těchto stejných dávkách byly poměry vylučování železa k příjmu železa 1,02 (indikující čistou bilanci železa) respektive 1,67 (indikující „čistou eliminaci železa“). Deferasirox vyvolal podobné reakce u pacientů s přetížením železem ovlivněným jinými anémiemi. Denní dávky 10 mg / kg (přípravek ve formě dispergovatelných tablet) po dobu jednoho roku může udržovat hladiny železa a sérového feritinu v játrech a indukovat čistou rovnováhu železa u pacientů, kteří dostávají vzácné transfuze nebo erytrocytoferézu. trend v sérovém feritinu lze použít k monitorování odpovědi na terapii. Omezené klinické údaje (29 pacientů s normální srdeční funkcí na počátku) s použitím MRI ukazují, že léčba deferasiroxem 10-30 mg / kg / den (dispergovatelná tabletová formulace) po dobu 1 roku může také snížit hladinu železa v srdci (na průměrně byl nárůst MRI T2 * 18,3 až 23,0 milisekund).
Hlavní analýza klíčové srovnávací studie provedené na 586 pacientech s beta thalasemií a přetížením železem v důsledku krevních transfuzí neprokázala, že v analýze celkové populace pacientů nebyla inferiorita tablet dispergovatelných deferasiroxem vůči deferoxaminu. Post-hoc analýza této studie ukazuje, že v podskupině pacientů s jaterní koncentrací železa ≥ 7 mg Fe / g suché hmotnosti léčených deferasiroxem dispergovatelnými tabletami (20 a 30 mg / kg) nebo deferoxaminem (35 až ≥ 50 mg / kg ), byla splněna kritéria non-méněcennosti.
Nicméně u pacientů s jaterní koncentrací železa
Předklinické a klinické studie ukázaly, že dispergovatelné tablety deferasiroxu mohou být účinné jako deferoxamin, pokud jsou použity v dávkovém poměru 2: 1 (např. Dávka dispergovatelných tablet deferasiroxu je číselně poloviční než dávka deferoxaminu). U potahovaných tablet deferasiroxu lze uvažovat s dávkovým poměrem 3: 1 (např. Dávka potahovaných tablet deferasiroxu je číselně jedna třetina dávky deferoxaminu). Toto doporučení pro dávkování však nebylo prospektivně hodnoceno v klinických studiích.
Rovněž u pacientů s koncentrací železa v játrech ≥ 7 mg Fe / g / suchou hmotnost, kteří trpí různými vzácnými anémiemi nebo srpkovitou anémií, způsobují deferasiroxové dispergovatelné tablety až do 20 a 30 mg / kg snížení koncentrace jaterního železa a sérového feritinu. Srovnatelné s získané u pacientů s beta talasemií.
V 5leté observační studii, ve které 267 dětí ve věku 2 až 33% sérového kreatininu a nad horní hranicí normálu při> 2 po sobě jdoucích příležitostech (3,1%) a alanin zvyšuje aminotransferázu (ALT) více než 5násobek horní hranice normálních (4,3%). Jednotlivé příhody zvýšení ALT a aspartátaminotransferázy byly hlášeny u 20,0% respektive 8,3% ze 145 pacientů. kteří studii dokončili
173 dospělých a pediatrických pacientů s talasemií nebo myelodysplastickými syndromy závislými na transfuzi bylo léčeno po dobu 24 týdnů ve studii hodnotící bezpečnost deferasiroxu potahovaných tablet a dispergovatelných tablet. Srovnatelný bezpečnostní profil byl pozorován u potahovaných tablet a dispergovatelných tablet.
U pacientů se syndromy talasemie nezávislými na transfuzi a přetížením železem byla léčba dispergovatelnými tabletami deferasiroxu hodnocena v roční, randomizované, dvojitě zaslepené, placebem kontrolované studii. Studie porovnávala účinnost dvou různých režimů dispergovatelných tablet deferasiroxu (počáteční dávky 5 a 10 mg / kg / den, 55 pacientů v každém rameni) a odpovídajícího placeba (56 pacientů). Do studie bylo zařazeno 145 pacientů. Dospělí a 21 dětských pacientů.Primárním parametrem účinnosti byla změna koncentrace železa v játrech (LIC) oproti výchozímu stavu po 12 měsících léčby.Jedním ze sekundárních parametrů účinnosti byla změna sérového feritinu mezi výchozím a čtvrtým trimestrem Při počáteční dávce 10 mg / kg / den, dispergovatelné tablety deferasiroxu vedly ke snížení indikátorů celkového tělesného železa. U léčených pacientů s dispergovatelnými tabletami deferasirox v průměru klesla koncentrace železa v játrech o 3,80 mg Fe / g / suchou hmotnost (počáteční dávka 10 mg / kg / den) a zvýšil o 0,38 mg Fe / g / suchou hmotnost u pacientů léčených placebem (str
Evropská agentura pro léčivé přípravky udělila odklad povinnosti předložit výsledky studií s přípravkem EXJADE u jedné nebo více podskupin pediatrické populace pro léčbu chronického přetížení železem vyžadujícího chelatační terapii (informace o použití u dětí viz bod 4.2).
05.2 Farmakokinetické vlastnosti
Potahované tablety EXJADE vykazují vyšší biologickou dostupnost než formulace dispergovatelných tablet EXJADE. Po úpravě dávky byla formulace potahovaných tablet (síla 360 mg) ekvivalentní dispergovatelným tabletám EXJADE (síla 500 mg) ve srovnání s průměrem plochy pod křivkou závislosti plazmatické koncentrace na čase (AUC) za podmínek nalačno. Cmax byla zvýšena o 30% (90% CI: 20,3% - 40,0%); Analýza klinické expozice / reakce však neodhalila žádné důkazy o klinicky relevantních účincích tohoto zvýšení.
Vstřebávání
Deferasirox (přípravek ve formě dispergovatelných tablet) je po perorálním podání absorbován se střední dobou do dosažení maximální plazmatické koncentrace (Tmax) přibližně 1,5 až 4 hodiny. Absolutní biologická dostupnost (AUC) deferasiroxu (přípravek ve formě dispergovatelných tablet) je přibližně 70% intravenózní dávky. Absolutní biologická dostupnost přípravku ve formě potahovaných tablet nebyla stanovena. Biologická dostupnost potahovaných tablet deferasiroxu byla o 36% vyšší než u dispergovatelných tablet.
Studie účinků jídla na podávání potahovaných tablet zdravým dobrovolníkům nalačno a s nízkotučným (kalorickým) tukem nebo s vysokým obsahem tuku (obsah tuku> 50% kalorií) má AUC a C byly po nízkotučném jídle (11%, respektive 16%). Po jídle s vysokým obsahem tuku byly AUC a Cmax zvýšeny (o 18%, respektive 29%). Jsou aditivní, a proto se doporučuje užívat potahované tablety buď na prázdný žaludek nebo s lehkým jídlem .
Rozdělení
Deferasirox se silně (99%) váže na plazmatické bílkoviny, téměř výhradně na sérový albumin, a má malý distribuční objem přibližně 14 litrů u dospělých.
Biotransformace
Glukuronidace je hlavní metabolickou cestou deferasiroxu s následným vylučováním žlučí. Pravděpodobně dojde k dekonjugaci glukuronidů ve střevě a následné reabsorpci (enterohepatická recirkulace): Ve studii u zdravých dobrovolníků vedlo podávání cholestyraminu po jedné dávce deferasiroxu k 45% snížení AUC deferasiroxu.
Deferasirox je převážně glukuronidován prostřednictvím UGT1A1 a v menší míře UGT1A3. Zdá se, že metabolismus deferasiroxu katalyzovaný (oxidační) CYP450 je u lidí malý (přibližně 8%). In vitro nebyla pozorována žádná inhibice metabolismu deferasiroxu hydroxymočovinou.
Odstranění
Deferasirox a jeho metabolity se vylučují převážně stolicí (84% dávky). Renální exkrece deferasiroxu a jeho metabolitů je minimální (8% dávky). Průměrný eliminační poločas (t1 / 2) se pohybuje od 8 do 16 hodin. Na biliárním vylučování deferasiroxu se podílejí transportéry MRP2 a MXR (BCRP).
Linearita / nelinearita
Za podmínek ustáleného stavu se Cmax a AUC0-24h deferasiroxu zvyšují přibližně lineárně s dávkou. Při vícenásobném dávkování se expozice zvyšuje o akumulační faktor 1,3 až 2,3.
Charakteristika pacientů
Dětští pacienti
Celková expozice dospívajících (12 až ≤17 let) a dětí (2 až
Sex
Samice mají mírně nižší (17,5%) zjevnou clearance pro deferasirox než muži. Vzhledem k tomu, že se dávka upravuje individuálně podle odpovědi, neočekává se, že by to mělo klinické důsledky.
Starší pacienti
Farmakokinetika deferasiroxu nebyla studována u starších pacientů (ve věku 65 let a starších).
Renální nebo jaterní insuficience
Farmakokinetika deferasiroxu nebyla studována u pacientů s renální insuficiencí. Farmakokinetika deferasiroxu není ovlivněna hladinami jaterních transamináz až do 5násobku horní hranice normálního rozmezí.
V klinické studii s jednorázovými dávkami dispergovatelných tablet deferasiroxu 20 mg / kg se průměrná expozice zvýšila o 16% u subjektů s lehkou poruchou funkce jater (Child-Pugh třída A) a o 76% u subjektů se středně těžkou poruchou funkce jater ( Child-Pugh třída B) ve srovnání s subjekty s normální funkcí jater. U subjektů s mírnou až středně těžkou poruchou funkce jater byla průměrná C deferasiroxu zvýšena o 22%. U subjektů s těžkou poruchou funkce jater (třída C podle Child-Pugha) se expozice zvýšila o 2,8- složit (viz body 4.2 a 4.4).
05.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje na základě konvenčních studií neodhalily žádné zvláštní riziko pro člověka farmakologie bezpečnosti, toxicita po opakovaných dávkách, genotoxicita nebo karcinogenní potenciál. Hlavními nálezy byla renální toxicita a zakalení čočky (katarakta). Podobné důkazy byly pozorovány u novorozenců a mladistvých zvířat. Předpokládá se, že renální toxicita je primárně způsobena ztrátou železa u zvířat, která neměla předchozí přetížení železem.
Testy genotoxicity in vitro byly negativní (Amesův test, test chromozomální aberace), zatímco deferasirox způsobil tvorbu mikrojader in vivo v kostní dřeni, ale ne v játrech, u potkanů, kterým nebyla podána dávka železa v smrtelných dávkách. Nebyly pozorovány žádné takové účinky u potkanů při zatížení železem. Deferasirox nebyl karcinogenní, když byl podáván potkanům ve 2leté studii a p53 +/- transgenním heterozygotním myším v 6měsíční studii.
Potenciál reprodukční toxicity byl hodnocen u potkanů a králíků. Deferasirox nebyl teratogenní, ale způsoboval zvýšenou frekvenci změn skeletu a mrtvě narozených potkanů při vysokých dávkách, které byly pro matku přetíženou železem silně toxické. Deferasirox nezpůsobil jiné účinky na plodnost nebo reprodukci.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Jádro tabletu:
Mikrokrystalická celulóza
Krospovidon
Povidon (K30)
Stearát hořečnatý
Koloidní bezvodý oxid křemičitý
Poloxamer 188
Složky nátěru:
Hypromelóza
Oxid titaničitý (E171)
Macrogol
Mastek
Hlinitý lak indigokarmínu (E132)
06.2 Neslučitelnost
Irelevantní.
06.3 Doba platnosti
3 roky
06.4 Zvláštní opatření pro skladování
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
06.5 Charakter vnitřního obalu a obsah balení
PVC / PVDC / hliníkové blistry.
Jednotlivá balení obsahující 30 nebo 90 potahovaných tablet nebo vícečetná balení obsahující 300 (10 balení po 30) potahovaných tablet.
Na trhu nemusí být všechny velikosti balení.
06.6 Návod k použití a zacházení
Žádné zvláštní pokyny.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Novartis Europharm Limited
Business park Frimley
Camberley GU16 7SR
Spojené království
08.0 REGISTRAČNÍ ČÍSLO
EXJADE 90 mg potahované tablety
EU/1/06/356/011
037421118
EU/1/06/356/012
037421120
EU/1/06/356/013
037421132
EXJADE 180 mg potahované tablety
EU/1/06/356/014
037421144
EU/1/06/356/015
037421157
EU/1/06/356/016
037421169
EXJADE 360 mg potahované tablety
EU/1/06/356/017
037421171
EU/1/06/356/018
037421183
EU/1/06/356/019
037421195
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Datum první registrace: 28. srpna 2006
Datum posledního obnovení: 18. dubna 2016
10.0 DATUM REVIZE TEXTU
26. ledna 2017

























-perch-e-quando-si-misura.jpg)

