Účinné látky: raloxifen
Raloxifene Sandoz 60 mg potahované tablety
Proč se používá raloxifen - generický lék? K čemu to je?
Raloxifene Sandoz obsahuje léčivou látku raloxifen hydrochlorid.
Raloxifene Sandoz se používá k léčbě a prevenci osteoporózy u postmenopauzálních žen.
Raloxifene Sandoz snižuje riziko zlomenin obratlů u žen s postmenopauzální osteoporózou. Snížení rizika zlomeniny kyčle nebylo prokázáno.
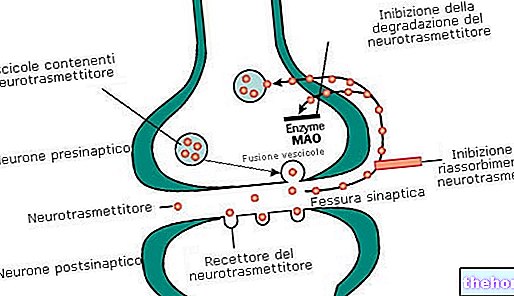
Jak přípravek Raloxifene Sandoz působí
Raloxifene Sandoz patří do skupiny nehormonálních léčiv nazývaných selektivní modulátory estrogenových receptorů (MSRE). Když žena dosáhne menopauzy, hladina estrogenu, ženských pohlavních hormonů, klesá. Raloxifene Sandoz reprodukuje některé pozitivní účinky estrogenu po menopauze.
Osteoporóza je onemocnění, které způsobuje, že jsou vaše kosti tenké a křehké - toto onemocnění je zvláště časté u postmenopauzálních žen. Ačkoli zpočátku nemusí mít žádné příznaky, osteoporóza je náchylnější k lámání kostí, zejména páteře. Zad, boků a zápěstí a může způsobit bolesti zad, sníženou výšku a shrbená záda.
Kontraindikace Kdy by neměl být používán Raloxifene - generikum
Neužívejte Raloxifene Sandoz:
- Jestliže se léčíte nebo jste se léčil (a) pro krevní sraženiny v nohou (hluboká žilní trombóza), plicích (plicní embolie) nebo očí (trombóza sítnicových žil).
- Jestliže jste alergický / á (přecitlivělý / á) na raloxifen nebo na kteroukoli další složku tohoto přípravku.
- Pokud je stále možné, abyste otěhotněla, mohl by Raloxifene Sandoz poškodit nenarozené dítě.
- Pokud máte onemocnění jater (příklady onemocnění jater jsou cirhóza, mírné selhání jater nebo cholestatická žloutenka).
- Pokud máte závažné problémy s ledvinami.
- Pokud máte nevysvětlitelné vaginální krvácení. Tuto situaci musí vyhodnotit lékař.
- Pokud máte aktivní rakovinu dělohy, protože s použitím přípravku Raloxifene Sandoz u žen s tímto onemocněním nejsou dostatečné zkušenosti.
Opatření pro použití Co potřebujete vědět před užitím generického léku Raloxifene
Před užitím přípravku Raloxifene Sandoz se poraďte se svým lékařem nebo lékárníkem.
- Pokud jste již nějakou dobu imobilizováni, například pokud jste upoutáni na invalidní vozík, potřebujete hospitalizaci nebo potřebujete zůstat na lůžku, abyste se zotavili z úrazu nebo neočekávaného onemocnění, protože tyto stavy mohou zvýšit riziko trombózy (hluboká žilní trombóza) plicní embolie nebo trombóza sítnicových žil).
- Pokud jste prodělal (a) mozkovou cévní příhodu (např. Cévní mozkovou příhodu) nebo vám lékař řekl, že máte vysoké riziko, že ji budete mít.
- Pokud máte onemocnění jater.
- Pokud trpíte rakovinou prsu, protože s použitím přípravku Raloxifene Sandoz u žen s tímto onemocněním nejsou dostatečné zkušenosti.
- Pokud užíváte orální estrogenovou terapii.
Je nepravděpodobné, že by Raloxifene Sandoz způsoboval vaginální krvácení. Při užívání přípravku Raloxifene Sandoz se proto neočekává žádné vaginální krvácení. Tuto situaci by měl zhodnotit váš lékař.
Raloxifene Sandoz neléčí postmenopauzální příznaky, jako jsou návaly horka.
Raloxifene Sandoz snižuje hladinu celkového cholesterolu a LDL („špatného“) cholesterolu. Obecně se hladina triglyceridů a HDL („dobrého“) cholesterolu nemění. Pokud jste však v minulosti užívali estrogen a došlo k přehnanému nárůstu triglyceridů, měli byste se před užitím přípravku Raloxifene Sandoz poradit se svým lékařem.
Raloxifene Sandoz obsahuje laktózu
Pokud vám lékař řekl, že trpíte „nesnášenlivostí laktózy, druh cukru, kontaktujte svého lékaře před užitím tohoto léku.
Interakce Které léky nebo potraviny mohou ovlivnit účinek přípravku Raloxifene - generikum
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte nebo jste v nedávné době užíval, a to i o lécích, které jsou dostupné bez lékařského předpisu.
Pokud užíváte léky na srdce digitalis nebo léky na ředění krve, jako je warfarin, na ředění krve, lékař může potřebovat změnit dávku těchto léků.
Informujte svého lékaře, pokud užíváte cholestyramin, který se používá hlavně jako lék snižující lipidy, protože Raloxifene Sandoz nemusí fungovat optimálně.
Varování Je důležité vědět, že:
Těhotenství, kojení a plodnost
Raloxifene Sandoz mohou užívat pouze ženy po menopauze a nesmí jej užívat ženy, které mohou mít ještě dítě. Raloxifene Sandoz by mohl poškodit nenarozené dítě.
Neužívejte Raloxifene Sandoz, pokud kojíte, protože se může mísit s mateřským mlékem.
Řízení dopravních prostředků a obsluha strojů
Raloxifene Sandoz nemá žádné známé nebo zanedbatelné účinky na řízení nebo obsluhu strojů.
Dávka, způsob a doba podání Jak používat raloxifen - generikum: dávkování
Vždy užívejte přípravek Raloxifene Sandoz přesně podle pokynů svého lékaře. Pokud máte pochybnosti, poraďte se se svým lékařem nebo lékárníkem.
Doporučená dávka je jedna tableta denně. Nezáleží na tom, v jakou denní dobu si ji dáte, ale vždy, když ji vezmete ve stejnou dobu, pomůže vám to zapamatovat si ji. Můžete ji užívat s jídlem i bez jídla.
Tablety jsou určeny k perorálnímu podání.
Tabletu spolkněte celou. Pokud si přejete, můžete s ním pít vodu. Tabletu nerozbijte ani nerozdrťte, než ji užijete. Rozbitá nebo rozdrcená tableta může mít špatnou chuť a existuje možnost, že můžete užít nesprávnou dávku.
Váš lékař vám řekne, jak dlouho pokračovat v užívání přípravku Raloxifene Sandoz. Váš lékař vám může také doporučit užívat doplňky vápníku a vitaminu D.
Jestliže jste zapomněl (a) užít přípravek Raloxifene Sandoz
Užijte tabletu, jakmile si vzpomenete, a poté pokračujte jako obvykle. Nezdvojnásobujte následující dávku, abyste nahradil (a) zapomenutou tabletu.
Jestliže jste přestal (a) užívat přípravek Raloxifene Sandoz
Nejprve si promluvte se svým lékařem.
Je důležité, abyste pokračoval v užívání přípravku Raloxifene Sandoz tak dlouho, jak vám řekne lékař.
Raloxifene Sandoz může léčit nebo předcházet osteoporóze, pouze pokud budete tablety nadále užívat.
Předávkování Co dělat, pokud jste předávkovali přípravkem Raloxifene - generikum
Jestliže jste užil (a) více přípravku Raloxifene Sandoz, než jste měl (a)
Promluvte si se svým lékařem nebo lékárníkem. Pokud užijete více přípravku Raloxifene Sandoz, než byste měli, můžete pociťovat křeče v nohou a závratě.
Nežádoucí účinky Jaké jsou vedlejší účinky generického léku Raloxifene
Podobně jako všechny léky, může mít i Raloxifene Sandoz nežádoucí účinky, které se ale nemusí vyskytnout u každého. Většina vedlejších účinků pozorovaných u raloxifenu byla mírná.
Velmi časté nežádoucí účinky (mohou postihnout více než 1 z 10 pacientů) jsou:
- Návaly horka (vazodilatace)
- Chřipkový syndrom
- Gastrointestinální příznaky, jako je malátnost (nauzea), zvracení, bolest břicha a poruchy trávení (dyspepsie)
- Zvýšený krevní tlak
Časté nežádoucí účinky (mohou postihnout až 1 z 10 lidí) jsou:
- Bolest hlavy, včetně migrény
- Křeče v nohou
- Otok rukou, nohou a nohou (periferní edém)
- Žlučové kameny
- Vyrážka
- Mírné příznaky prsu, jako je bolest, zvětšení a citlivost
Méně časté nežádoucí účinky (mohou postihnout až 1 ze 100 lidí) jsou:
- Zvýšené riziko krevních sraženin v nohou (hluboká žilní trombóza)
- Zvýšené riziko vzniku krevních sraženin v plicích (plicní embolie)
- Zvýšené riziko vzniku krevních sraženin v oku (trombóza sítnicových žil)
- Kůže kolem žíly je červená a bolestivá (tromboflebitida povrchové žíly)
- Tvorba krevní sraženiny v tepně (například mrtvice, včetně zvýšeného rizika úmrtí na mrtvici)
- Snížení počtu krevních destiček, což zvyšuje riziko krvácení nebo tvorby modřin.
Ve vzácných případech (mohou postihnout až 1 z 1000 pacientů) se během léčby přípravkem Raloxifene Sandoz mohou zvýšit hladiny jaterních enzymů v krvi.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48100 41 Praha 10 Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
Expirace a retence
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Raloxifene Sandoz nepoužívejte po uplynutí doby použitelnosti, uvedené na obalu.
Uchovávejte blistr v krabičce, aby byl chráněn před světlem a vlhkostí. Chraňte před mrazem.
Léčivé přípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Jiná informace
Co přípravek Raloxifene Sandoz obsahuje
- Léčivou látkou je raloxifen hydrochlorid. Jedna tableta obsahuje raloxifen hydrochlorid 60 mg, což odpovídá raloxifenum 56 mg.
- Dalšími složkami tablet Raloxifene Sandoz jsou:
- Jádro tablety: sodná sůl karboxymetylškrobu, monohydrát kyseliny citronové, mikrokrystalická celulóza, hydrogenfosforečnan vápenatý, poloxamer 407, magnesium -stearát
- Potah tablety: hypromelosa, monohydrát laktózy, oxid titaničitý (E171) a makrogol / PEG 4000.
Jak Raloxifene Sandoz vypadá a obsah balení
Raloxifene Sandoz jsou bílé, eliptické, potahované tablety. Tablety jsou baleny v blistrech. Krabice obsahují blistry se 14, 28, 30, 84 nebo 90 tabletami.
Na trhu nemusí být všechny velikosti balení.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
RALOXIFENE SANDOZ 60 MG TABLETY NAPLNENÉ FILMEM
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna potahovaná tableta obsahuje raloxifen hydrochlorid 60 mg, což odpovídá 56 mg volného raloxifenu.
Pomocné látky se známými účinky:
Jedna tableta obsahuje monohydrát laktosy (1,5 mg).
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Potahovaná tableta. Bílé eliptické tablety.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Raloxifene Sandoz je indikován k léčbě a prevenci osteoporózy u postmenopauzálních žen.Ukázalo se, že významně snižuje riziko osteoporotických zlomenin obratlů, nikoli však zlomenin kyčle.
Při určování volby přípravku Raloxifene Sandoz nebo jiných terapií, včetně estrogenu, pro jednotlivou ženu po menopauze je třeba vzít v úvahu symptomy menopauzy, účinky na děložní a prsní tkáň, kardiovaskulární rizika a přínosy (viz bod 5.1)
04.2 Dávkování a způsob podání
Dávkování
Doporučená dávka je jedna tableta denně pro orální podání, kterou lze užít kdykoli během dne a bez ohledu na jídlo. Vzhledem k povaze této patologie je přípravek Raloxifene Sandoz určen k dlouhodobému užívání.
Doplňky vápníku a vitaminu D jsou obecně doporučovány ženám se sníženým dietním příjmem vápníku.
Senioři
U starších pacientů není nutná úprava dávky.
Poškození ledvin:
Raloxifene Sandoz nesmí užívat pacienti s těžkou poruchou funkce ledvin (viz bod 4.3). U pacientů s lehkou nebo středně těžkou poruchou funkce ledvin by měl být přípravek Raloxifene Sandoz používán s opatrností.
Porucha funkce jater:
Raloxifene Sandoz nesmí být podáván pacientům s poruchou funkce jater (viz body 4.3 a 4.4).
Pediatrická populace
Raloxifene Sandoz by neměly používat děti jakéhokoli věku. Použití přípravku Raloxifene Sandoz u pediatrické populace není relevantní.
04.3 Kontraindikace
• Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
• Nesmí být podáván ženám ve fertilním věku (viz bod 4.6).
• Předchozí nebo současné žilní tromboembolické epizody (VTE), včetně hluboké žilní trombózy, plicní embolie a trombózy sítnicových žil.
• Porucha funkce jater, včetně cholestázy.
• Vážné poškození ledvin.
• Děložní krvácení neurčené povahy.
Raloxifene Sandoz by neměly používat pacientky s příznaky nebo příznaky rakoviny endometria, protože bezpečnost u této skupiny pacientek nebyla dostatečně studována.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Raloxifen je spojen se zvýšeným rizikem žilních tromboembolických příhod, což je podobné riziku, jaké je spojeno se stávající hormonální substituční terapií. U pacientů s rizikem žilních tromboembolických příhod jakékoli etiologie je třeba zvážit poměr přínosů a rizik. Raloxifene Sandoz by měl být vysazen v případě jakéhokoli onemocnění nebo situace zahrnující delší dobu imobilizace. Pozastavení by mělo proběhnout co nejdříve v případě nemoci nebo tři dny před začátkem imobilizačního období. Léčba by neměla být obnovena, dokud nebude vyřešena příčina přerušení a pacient znovu nezačne mít úplnou pohyblivost.
Ve studii postmenopauzálních žen s dokumentovanou ischemickou chorobou srdeční nebo se zvýšeným rizikem koronárních příhod raloxifen ve srovnání s placebem neovlivnil ani výskyt infarktu myokardu, hospitalizace kvůli akutnímu koronárnímu syndromu, ani celkovou úmrtnost, včetně celkového kardiovaskulárního úmrtnost, ani počet mozkových mrtvic. U žen, které dostaly raloxifen c “, však došlo ke zvýšení úmrtnosti na mozkové mrtvice. Incidence úmrtí na cévní mozkovou příhodu byla 2,2 na 1 000 žen ročně s raloxifenem ve srovnání s 1,5 na 1 000 žen za rok s placebem (viz bod 4.8) .Tyto údaje je třeba vzít v úvahu při předepisování raloxifenu postmenopauzálním ženám s cévní mozkovou příhodou v anamnéze nebo jinými významnými rizikové faktory cévní mozkové příhody, jako je přechodný ischemický záchvat nebo fibrilace síní.
Proliferace endometria nebyla prokázána. Jakékoli děložní krvácení, ke kterému dojde během léčby přípravkem Raloxifene Sandoz, je neočekávané a musí být plně vyšetřeno odborníkem. Dvě nejčastější diagnózy spojené s děložním krvácením, ke kterým došlo během léčby raloxifenem, byly atrofie endometria a benigní polypy endometria. U postmenopauzálních žen, které dostaly léčbu raloxifenem po dobu 4 let, byly benigní polypy endometria hlášeny s incidencí 0,9% ve srovnání s 0,3% ženy, které byly léčeny placebem.
Raloxifen je metabolizován hlavně v játrech. Jednorázové dávky raloxifenu podávané pacientům s cirhózou a středně těžkou poruchou funkce jater (Child-Pugh třída A) vedly k plazmatickým koncentracím raloxifenu přibližně 2,5krát vyšším než u kontrol. Nárůst koreluje s celkovými koncentracemi bilirubinu. Raloxifene Sandoz se navíc nedoporučuje u pacientů s jaterní insuficiencí. Pokud jsou zjištěny zvýšené hodnoty, je třeba během léčby pečlivě sledovat celkovou bilirubinémii, gammaglutamyltransferázu, alkalickou fosfatázu, alanin transferázu a aspartát transferázu.
Omezená klinická data naznačují, že u pacientů s předchozími epizodami hypertriglyceridemie (> 5,6 mmol / l) způsobenými perorálním estrogenem může být raloxifen spojen s výrazně zvýšenou triglyceridemií.U pacientů s touto anamnézou je třeba sledovat hodnoty triglyceridů v séru raloxifenu.
Bezpečnost raloxifenu u pacientek s rakovinou prsu nebyla dostatečně studována. Nejsou k dispozici žádné údaje o souběžném užívání raloxifenu s látkami používanými k léčbě časného nebo pokročilého karcinomu prsu.Proto by měl být Raloxifene Sandoz používán k léčbě a prevenci osteoporózy až po léčbě rakoviny prsu.Včetně adjuvantní terapie dokončeno.
Vzhledem k omezeným bezpečnostním informacím týkajícím se současného podávání raloxifenu a systémového estrogenu se takové použití nedoporučuje.
Raloxifene Sandoz není účinný při snižování vazodilatace (návaly horka) nebo jiných menopauzálních symptomů spojených s nedostatkem estrogenu.
Raloxifene Sandoz obsahuje laktózu. Pacienti se vzácnými dědičnými problémy s intolerancí galaktózy, vrozeným nedostatkem laktázy nebo malabsorpcí glukózy a galaktózy by tento přípravek neměli užívat.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Souběžné podávání uhličitanu vápenatého a antacid obsahujících hydroxid hořečnatý a hlinitý neovlivňuje biologickou dostupnost raloxifenu.
Současné podávání raloxifenu a warfarinu nezměnilo jejich příslušnou farmakokinetiku. Bylo však pozorováno mírné zkrácení protrombinového času, takže pokud je raloxifen podáván současně s warfarinem nebo jinými deriváty kumarinu, měl by být protrombinový čas monitorován. Účinky na protrombinový čas se mohou objevit po několika týdnech, pokud je léčba raloxifenem zahájena u pacientů, kteří již užívají kumarinová antikoagulancia.
Raloxifen nemá žádný vliv na farmakokinetiku methylprednisolonu podávaného v jedné dávce. Raloxifen neruší oblast ustáleného stavu pod digoxinovou křivkou.Maximální koncentrace digoxinu se zvyšuje o méně než 5%.
Vliv souběžného podávání léčiva na plazmatické koncentrace raloxifenu byl hodnocen v klinických studiích prevence a léčby. Mezi často podávaná léčiva patřily: paracetamol, nesteroidní protizánětlivá léčiva (jako je kyselina acetylsalicylová, ibuprofen a naproxen).), orální antibiotika, antagonisté H1 a H2 a benzodiazepiny. Nebyl zjištěn žádný klinicky relevantní účinek současného podávání výše uvedených léčiv na plazmatické koncentrace raloxifenu.
V plánu klinické studie bylo povoleno současné použití vaginálních estrogenních přípravků, pokud to bylo považováno za vhodné k léčbě atrofických projevů pochvy. Ve srovnání s placebem nedošlo k zvýšenému použití u pacientů léčených raloxifenem.
In vitroraloxifen nereaguje s vazbou warfarinu, fenytoinu nebo tamoxifenu.
Raloxifen by neměl být podáván současně s cholestyraminem (nebo jinými anexovými pryskyřicemi), což významně snižuje absorpci a entero-hepatální cirkulaci raloxifenu.
Současné podávání ampicilinu vede ke snížení vrcholů plazmatické koncentrace raloxifenu. Protože se však celkové absorbované množství a rychlost eliminace raloxifenu nemění, lze raloxifen podávat současně s ampicilinem.
Raloxifen mírně zvyšuje koncentrace globulinů vázajících hormony, včetně globulinů vážících pohlavní steroidy (SHBG), globulinu vázajícího tyroxin (TBG) a globulinu vázajícího kortikosteroidy (CBG), s odpovídajícím zvýšením koncentrací celkových hormonů. Tyto změny neovlivňují koncentrace volných hormonů.
04.6 Těhotenství a kojení
Těhotenství
Raloxifene Sandoz je určen k použití pouze u postmenopauzálních žen.
Raloxifene Sandoz nesmí užívat ženy, které ještě mohou mít děti. Raloxifen může způsobit poškození plodu při podávání těhotným ženám. Pokud je tento léčivý přípravek omylem podáván během těhotenství nebo pacientka otěhotní během jeho užívání, měla by být pacientka informována o potenciálním riziku pro plod (viz bod 5.3).
Čas krmení
Není známo, zda se raloxifen nebo jeho metabolity vylučují do lidského mléka. Nelze vyloučit riziko pro novorozence / kojence. Jeho klinické použití u kojících žen proto nelze doporučit. Raloxifene Sandoz může ovlivnit vývoj dítěte.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Raloxifene nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje.
04.8 Nežádoucí účinky
a.) Shrnutí bezpečnostního profilu
Klinicky nejvýznamnějšími nežádoucími účinky hlášenými u postmenopauzálních žen léčených přípravkem Raloxifene Sandoz jsou žilní tromboembolické příhody (viz bod 4.4), které se vyskytují u méně než 1% léčených pacientů.
b.) Souhrnná tabulka nežádoucích účinků
Níže uvedená tabulka ukazuje nežádoucí účinky a četnosti pozorované ve studiích prevence a léčby zahrnujících více než 13 000 postmenopauzálních žen spolu s nežádoucími účinky z postmarketingových údajů. Délka léčby v těchto studiích se pohybovala od 6 do 60 měsíců. Většina nežádoucích účinků rutinně nevyžadovala přerušení léčby.
Frekvence postmarketingových údajů byly vypočteny z placebem kontrolovaných klinických studií (zahrnujících celkem 15 234 pacientů, 7 601 pacientů s raloxifenem 60 mg a 7633 pacientů s placebem) u postmenopauzálních žen s osteoporózou nebo ischemickou chorobou srdeční, ICHS), u nichž se projevilo nebo zvýšilo riziko ICHS, bez srovnání s četností nežádoucích účinků ve skupinách s placebem.
Ve studiích prevence došlo k přerušení léčby jakýchkoli nežádoucích účinků u 10,7% z 581 pacientů léčených raloxifenem ve srovnání s 11,1% z 584 pacientů léčených placebem.Ve studiích léčby došlo k přerušení léčby pro jakýkoli nežádoucí účinek u 12,8% z 2557 pacientů léčených raloxifenem ve srovnání s 11,1% z 2576 pacientů léčených placebem. Pro klasifikaci nežádoucích účinků se používá následující konvence: velmi časté (≥ 1/10), časté (≥ 1/100,
termín zahrnutý na základě zkušeností po uvedení na trh
c.) Popis vybraných nežádoucích účinků
Frekvence vazodilatace (návaly horka) byla u pacientů léčených raloxifenem mírně zvýšena ve srovnání s pacienty léčenými placebem (v klinických studiích prevence osteoporózy, 2 až 8 let po menopauze, 24,3% s raloxifenem ve srovnání s 18,2% s placebem; v klinických studiích pro léčbu osteoporózy, s průměrným věkem 66 let, 10,6% s raloxifenem oproti 7,1% s placebem). Tato nežádoucí reakce byla častější v prvních 6 měsících léčby a zřídka se objevila poprvé po ten čas.
Ve studii s 10 101 postmenopauzálními ženami s prokázanou ischemickou chorobou srdeční nebo se zvýšeným rizikem koronárních příhod (RUTH) došlo k nástupu vazodilatace (návaly horka) u 7,8% pacientů léčených raloxifenem a u 4, 7% pacientů léčených placebo.
Ve všech klinických studiích s raloxifenem při léčbě osteoporózy a placebem kontrolovaných se vyskytly žilní tromboembolické příhody, včetně hluboké žilní trombózy, plicní embolie a trombózy sítnicových žil, s přibližnou frekvencí 0,8% nebo 3,22 případů na 1 000 pacientů ročně. U pacientů léčených raloxifenem bylo ve srovnání s placebem zjištěno relativní riziko 1,60 (interval spolehlivosti 0,95, 2,71). Riziko tromboembolické příhody bylo vyšší v prvních čtyřech měsících léčby. Tromboflebitida povrchové žíly se vyskytovala s frekvencí méně než 1%.
Ve studii RUTH se žilní tromboembolické příhody vyskytovaly s frekvencí přibližně 2,0% nebo 3,88 případů na 1 000 pacientů ročně ve skupině s raloxifenem a s frekvencí 1,4% nebo 2, 70 případů na 1 000 pacientů ročně ve skupině s placebem. Míra rizika pro všechny žilní tromboembolické příhody ve studii RUTH byla HR = 1,44 (1,06 - 1,95). Tromboflebitida povrchových žil se vyskytovala s frekvencí 1% ve skupině s raloxifenem a 0,6% ve skupině s placebem.
Ve studii RUTH raloxifen neovlivnil výskyt cévní mozkové příhody ve srovnání s placebem. U žen, které užívaly raloxifen, však došlo k nárůstu úmrtí na mrtvici. Incidence mortality na cévní mozkové příhody byla 2,2 na 1 000 žen ročně ve skupině s raloxifenem oproti 1,5 na 1 000 žen za rok ve skupině s placebem (viz bod 4.4) .Během průměrného sledování 5,6 roku léčilo 59 (1,2%) žen s raloxifenem zemřelo na cévní mozkovou příhodu, ve srovnání s 39 (0,8%) ženami léčenými placebem.
Další pozorovanou nežádoucí reakcí byl výskyt křečí v nohou (5,5% u raloxifenu, 1,9% u placeba v preventivních studiích a 9,2% u raloxifenu, 6,0% u placeba ve studiích léčby).
Ve studii RUTH byly křeče v nohou pozorovány u 12,1% pacientů léčených raloxifenem a 8,3% pacientů léčených placebem.
Chřipkový syndrom byl nalezen u 16,2% pacientů léčených raloxifenem ve srovnání se 14,0% pacientů léčených placebem.
„Další statisticky nevýznamný rozdíl (p> 0,05), ale s evidentní korelací s použitou dávkou, byl výskyt periferního edému, který se vyskytoval s„ 3,1% incidencí u raloxifenu ve srovnání s “1,9% u placeba v prevenci ve studiích s incidencí 7,1% u raloxifenu oproti 6,1% u placeba ve studiích léčby.
Ve studii RUTH došlo k nástupu periferního edému u 14,1% pacientů léčených raloxifenem a u 11,7% pacientů léčených placebem, což představuje statisticky významný nález.
Mírné snížení počtu krevních destiček (6–10%) bylo pozorováno během léčby raloxifenem v placebem kontrolovaných klinických studiích léčby osteoporózy.
Byly vzácně hlášeny mírné zvýšení aspartát transferázy a / nebo alanin transferázy, u nichž nelze vyloučit příčinnou souvislost s raloxifenem. Zvýšení s podobnou frekvencí bylo pozorováno u pacientů léčených placebem.
Ve studii (RUTH) provedené u postmenopauzálních žen s dokumentovanou ischemickou chorobou srdeční nebo se zvýšeným rizikem koronárních příhod došlo k další nežádoucí reakci cholelitiázy u 3,3% pacientů léčených raloxifenem a u 2,6% pacientů léčených raloxifenem. s placebem. Četnosti cholecystektomie u pacientů léčených raloxifenem (2,3%) se statisticky významně nelišily od pacientů léčených placebem (2,0%).
V některých klinických studiích byla léčba raloxifenem (n = 317) srovnávána s kombinovanou kontinuální (n = 110) nebo cyklickou (n = 205) hormonální substituční terapií (HRT). Výskyt symptomů prsu a děložního krvácení byl významně nižší u žen léčených raloxifenem než u žen léčených oběma typy HRT.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky, ke kterým dochází po registraci léčivého přípravku, je důležité, protože umožňuje průběžné sledování poměru přínosů a rizik léčivého přípravku. Zdravotničtí pracovníci jsou požádáni, aby hlásili jakékoli podezření na nežádoucí účinky prostřednictvím národního systému hlášení. "Adresa www. agenziafarmaco.gov.it/it/responsabili.
04.9 Předávkování
V některých klinických studiích byly podávány denní dávky až 600 mg po dobu 8 týdnů a 120 mg po dobu 3 let. Během klinických studií nebyly hlášeny žádné případy předávkování raloxifenem.
U dospělých pacientů, kteří užili dávky vyšší než 120 mg při jednorázovém podání, byly hlášeny příznaky jako křeče v nohou a závratě.
Při náhodném předávkování u dětí mladších 2 let byla maximální hlášená dávka 180 mg. U dětí příznaky náhodného předávkování zahrnovaly ataxii, závratě, zvracení, vyrážku, průjem, třes a návaly horka, stejně jako zvýšení alkalické fosfatázy.
Nejvyšší předávkování bylo přibližně 1,5 gramu. Nebyla hlášena žádná úmrtí spojená s předávkováním.
Pro raloxifen hydrochlorid neexistuje žádné specifické antidotum.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Selektivní modulátor estrogenových receptorů. ATC kód: G03XC01.
Mechanismus účinku a farmakodynamický účinek
Jako selektivní modulátor estrogenových receptorů (MSRE), raloxifen vykonává selektivní agonisty nebo antagonistické aktivity na tkáně citlivé na estrogen. Působí jako agonista na kost a částečně na metabolismus cholesterolu (snížení celkového cholesterolu a LDL cholesterolu).), Ale ne na hypotalamu nebo na tkáních prsu nebo dělohy.
Biologické účinky raloxifenu, jako estrogenové, jsou zprostředkovány vysokou afinitní vazbou na estrogenové receptory a regulací genové exprese. V různých tkáních tato vazba zahrnuje diferencované exprese více genů regulovaných estrogenem. Data naznačují, že estrogenový receptor může regulovat genovou expresi alespoň dvěma odlišnými cestami, které jsou specifické pro vazbu, tkáň a / nebo gen.
a) Účinky na kosterní systém
Snížená dostupnost estrogenu, ke které dochází v menopauze, vede k výraznému zvýšení resorpce kosti, úbytku kostní hmoty a riziku zlomenin. Ztráta kostí je obzvláště rychlá v prvních 10 letech po menopauze, kdy kompenzační nárůst tvorby nových kostí není dostatečný k vyrovnání ztrát způsobených resorpcí. Mezi další rizikové faktory, které mohou vést k rozvoji osteoporózy, patří: časná menopauza; přítomnost osteopenie (alespoň jedna standardní odchylka pod špičkovými hodnotami kostní hmoty); štíhlá konstituce; Bělošská nebo asijská rasa; obeznámenost s osteoporózou Obecně platí, že náhradní terapie zabraňují nadměrné resorpci kosti. U postmenopauzálních žen s osteoporózou raloxifen snižuje výskyt zlomenin obratlů, udržuje kostní hmotu a zvyšuje kostní minerální denzitu (BMD).
Na základě těchto rizikových faktorů je prevence osteoporózy pomocí raloxifenu indikována u žen do 10 let po menopauze, přičemž BMD páteře je mezi 1,0 a 2,5 SD pod průměrnou hodnotou normální mladé populace, s ohledem na vysoké riziko osteoporotických zlomenin nad Podobně je raloxifen indikován k léčbě osteoporózy nebo stabilizované osteoporózy u žen s BMD páteře s 2,5 standardní odchylkou pod hodnotou průměrné hodnoty normální mladé populace normální a / nebo se zlomeninami obratlů, bez ohledu na BMD.
i) Výskyt zlomenin. Ve studii 7 705 postmenopauzálních žen s průměrným věkem 66 let a s osteoporózou nebo osteoporózou spojenou s přítomností zlomeniny snížila léčba raloxifenem po dobu 3 let výskyt zlomenin obratlů o 47%(relativní riziko 0,53, spolehlivost Interval 0,35, 0,79, p zlomenina obratle 39% (relativní riziko 0,61, interval spolehlivosti 0,43, 0,88). Nebyl prokázán žádný účinek na nevertebrální zlomeniny. Od 4. do 8. roku byli pacienti registrováni k souběžnému užívání bisfosfonátů, kalcitoninu a fluoridy a v této studii všichni pacienti dostali doplněk vápníku a vitaminu D.
Ve studii RUTH byly všechny klinické zlomeniny zaznamenány jako sekundární cílový parametr. Raloxifen snížil výskyt klinických zlomenin obratlů o 35% ve srovnání s placebem (HR 0,65, interval spolehlivosti 0,47, 0,89). Tyto výsledky mohly být ovlivněny výchozími rozdíly v BMD a zlomeninách obratlů. Mezi léčenými skupinami nebyl žádný rozdíl ve výskytu nových nevertebrálních zlomenin. Současné použití jiných kostně aktivních ošetření bylo povoleno po celou dobu studie.
ii) Minerální hustota kostí (BMD). Účinnost raloxifenu podávaného jednou denně postmenopauzálním ženám do 60 let a s dělohou nebo bez dělohy byla prokázána po dobu dvou let léčby. Ženy byly po menopauze po dobu v rozmezí od 2 do 8 let.
Tři klinické studie zahrnovaly 1764 postmenopauzálních žen, které byly léčeny raloxifenem a placebem doplněným vápníkem nebo vápníkem. V jedné z těchto studií ženy dříve podstoupily hysterektomii. raloxifen vedl k významnému zvýšení minerální denzity kostí v proximálním femuru a páteři a také k významnému zvýšení kostní hmoty celé kostry ve srovnání s placebem. Toto zvýšení BMD bylo obecně 2% ve srovnání s placebem. Podobný nárůst BMD byl pozorován u léčené populace, která dostávala raloxifen po dobu až 7 let. Ve studiích prevence bylo procento subjektů, které během léčby raloxifenem prokázaly zvýšení nebo snížení BMD: v páteři 37% s poklesem a 63% se zvýšením; na úrovni celkového proximálního femuru 29% s poklesem a 71% s nárůstem.
iii) Údaje o kinetice vápníku. Raloxifen a estrogen působí na remodelaci kostí a metabolismus vápníku podobným způsobem. Raloxifen byl spojen se sníženou resorpcí kostí a pozitivní změnou rovnováhy vápníku rovnající se 60 mg denně, v podstatě v důsledku snížení ztrát vápníku močí.
iv) Histomorfometrie (kvalita kosti): Ve srovnávací studii mezi raloxifenem a estrogeny byla kostní tkáň pacientů léčených "jedním nebo druhým léčivým přípravkem histologicky normální, bez známek poruch mineralizace. ne lamelární nebo medulární fibrózy."
Raloxifen snižuje kostní resorpci. Tento účinek na kost se projevuje snížením hladin markerů kostního obratu v séru a moči, snížením kostní resorpce hodnoceným radioaktivními kinetickými studiemi vápníku, zvýšením BMD a snížením výskytu zlomenin.
b) Účinky na metabolismus lipidů a kardiovaskulární riziko
Klinické studie ukázaly, že denní dávka 60 mg raloxifenu významně snižuje celkový cholesterol (3 až 6%) a LDL cholesterol (4 až 10%). U pacientů s nejvyššími výchozími hladinami cholesterolu došlo k největšímu snížení. Koncentrace HDL cholesterolu a triglyceridů se významně nezměnily.Po 3 letech léčby raloxifen redukoval fibrinogen (6,71%). Ve studii léčby osteoporózy vyžadovalo zahájení léčby snižující hladinu lipidů významně méně pacientů léčených raloxifenem než pacientů léčených placebem.
Osmiletá léčba raloxifenem významně neovlivnila riziko kardiovaskulárních příhod u pacientů zařazených do studie léčby osteoporózy. Podobně ve studii RUTH neovlivnil raloxifen výskyt infarktu myokardu, hospitalizace. Kvůli akutnímu koronárnímu syndromu, cévní mozkové příhodě nebo celková úmrtnost, včetně celkové kardiovaskulární úmrtnosti, ve srovnání s placebem (zvýšené riziko smrtelné cévní mozkové příhody viz bod 4.4).
Relativní riziko žilních tromboembolických příhod pozorované během léčby raloxifenem bylo 1,60 (interval spolehlivosti 0,95, 2,71) ve srovnání s placebem a 1,0 (interval spolehlivosti 0,3, 6,2) ve srovnání s estrogenovou nebo hormonální substituční terapií. Riziko tromboembolické příhody bylo největší v prvních čtyřech měsících léčby.
c) Účinky na endometrium a pánevní dno
V klinických studiích raloxifen nestimuloval postmenopauzální endometrium dělohy. Ve srovnání s placebem nebyl raloxifen spojen s výtokem z endometria, krvácením nebo hyperplazií. Bylo zváženo téměř 3 000 transvaginálních ultrazvukových skenů (TVU) u 831 žen ve všech dávkových skupinách. Ženy léčené raloxifenem měly trvale tloušťku endometria nerozlišitelnou od tloušťky zjištěné u žen léčených placebem. Po 3 letech léčby bylo pozorováno zvýšení tloušťky endometria nejméně o 5 mm, zjištěné transvaginálním ultrazvukem, u 1,9% z 211 žen léčených raloxifenem 60 mg denně ve srovnání s 1,8% u 219 žen, které dostávaly placebo. Mezi incidencí hlášeného děložního krvácení nebyly mezi oběma skupinami s raloxifenem a placebem žádné rozdíly.
Endometriální biopsie provedené po šesti měsících léčby raloxifenem 60 mg denně prokázaly u všech pacientů neproliferativní endometrium. Kromě toho ve studii využívající dávky raloxifenu 2,5násobku doporučené denní dávky nebyly žádné důkazy o proliferaci endometria a zvýšení objemu dělohy.
Ve studii léčby osteoporózy byla tloušťka endometria hodnocena každoročně po dobu 4 let v podskupině populační studie (1 644 pacientek). Po 4 letech léčby se měření tloušťky endometria u žen léčených raloxifenem nelišilo od výchozí hodnoty. Mezi ženami léčenými raloxifenem a ženami léčenými placebem nebyl žádný rozdíl ve výskytu vaginálního krvácení (špinění) nebo vaginálního výtoku. Méně žen léčených raloxifenem než těch, které dostaly placebo, se muselo uchýlit k "operaci prolapsu dělohy. Po 3 letech léčby raloxifenem bezpečnostní profil přípravku naznačuje, že léčba raloxifenem nezvyšuje relaxaci pánevního dna nebo" operaci pánevního dna.
Po 4 letech raloxifen nezvyšoval riziko rakoviny endometria nebo vaječníků. U postmenopauzálních žen, které užívaly raloxifen po dobu 4 let, byly benigní polypy endometria hlášeny s incidencí 0,9% ve srovnání s 0,3% žen, které byly léčeny placebem.
d) Účinky na prsní tkáň
Raloxifen nestimuluje prsní tkáň. Ve všech placebem kontrolovaných klinických studiích byl raloxifen k nerozeznání od placeba s ohledem na frekvenci a závažnost příznaků prsu (žádné zvětšení prsou, citlivost a bolest).
Na konci 4leté studie léčby osteoporózy (zahrnující 7 705 pacientek) léčba raloxifenem snížila riziko celkového karcinomu prsu o 62% ve srovnání s placebem (relativní riziko 0,38, interval spolehlivosti 0,21, 0,69), 71% riziko invazivního prsu rakoviny (relativní riziko 0,29, interval spolehlivosti 0,13, 0,58) a riziko invazivního karcinomu prsu pozitivního na estrogenový receptor (ER) 79% (relativní riziko 0,21, interval spolehlivosti 0,07, 0,50). Raloxifen nemá žádný vliv na riziko ER negativního rakovina prsu. Tato pozorování podporují závěr, že raloxifen nevykazuje „vnitřní agonistickou aktivitu estrogenu v prsní tkáni.
e) Účinky na kognitivní funkce
Nebyly pozorovány žádné nežádoucí účinky na kognitivní funkce.
05.2 Farmakokinetické vlastnosti
Vstřebávání
Po perorálním podání je raloxifen rychle absorbován. Přibližně 60% perorální dávky je absorbováno. Pre-systémová glukuronidace je rozsáhlá. Absolutní biologická dostupnost raloxifenu je 2%. Čas do dosažení průměrné maximální plazmatické koncentrace a biologické dostupnosti závisí na systémové konverzi a entero-hepatální cirkulaci raloxifenu a jeho metabolitů glukuronidů.
Rozdělení
Raloxifen je široce distribuován po celém těle. Distribuční objem není závislý na dávce. Raloxifen se silně váže na plazmatické bílkoviny (98 - 99%).
Biotransformace
Raloxifen prochází výrazným metabolickým procesem prvního průchodu následujícím glukuronidovým konjugátům: raloxifen-4 "-glukuronid, raloxifen-6-glukuronid a raloxifen-6,4" -diglukuronid. Nebyly objeveny žádné další metabolity. Raloxifen obsahuje méně než 1% kombinovaných koncentrací raloxifenu a glukuronidových metabolitů.Úrovně raloxifenu jsou udržovány enterohepatální recirkulací s plazmatickým poločasem 27,7 hodiny.
Výsledky jednorázových perorálních dávek raloxifenu predikují farmakokinetické profily vyvolané vícenásobným dávkováním. Zvýšení dávek raloxifenu má za následek téměř úměrné zvýšení plazmatické koncentrace plochy pod křivkou (AUC) / čas.
Odstranění
Většina dávky metabolitů raloxifenu a glukuronidů je eliminována do 5 dnů, v podstatě se nachází ve stolici, zatímco méně než 6% je vyloučeno močí. Zvláštní populace
Renální insuficience - Méně než 6% celkové dávky se vyloučí močí. V populační farmakokinetické studii vedlo 47% snížení clearance kreatininu korigované na libovou tělesnou hmotnost k 17% a 15% snížení clearance raloxifenu a konjugátu.
Porucha funkce jater - Kinetika jedné dávky raloxifenu u pacientů s cirhózou a středně těžkou poruchou funkce jater (Child -Pugh třída A) byla srovnávána s kinetikou zdravých subjektů. Plazmatické koncentrace raloxifenu byly 2,5krát vyšší než u kontrol a korelovaly s koncentracemi bilirubinu.
05.3 Předklinické údaje vztahující se k bezpečnosti
Ve dvouleté studii kancerogenity na potkanech byl u samic léčených vysokými dávkami (279 mg / kg za den) pozorován nárůst ovariálních nádorů původu granulosa / theca. V této skupině byla celková absorpce (AUC) raloxifen byl přibližně 400krát vyšší než u postmenopauzálních žen léčených dávkou 60 mg. Ve 21měsíční studii karcinogenity na myších byl u mužských vzorků podaných 41 nebo 210 mg / kg pozorován „zvýšený výskyt intersticiálních nádorů varlat, adenomů a adenokarcinomů prostaty a u samců, kteří obdrželi 210 mg, leiomyoblastomy prostaty / kg. U samic myší byl „zvýšený výskyt nádorů vaječníků zjištěn u zvířat, která dostávala 9 až 242 mg / kg (0,3 při 32násobku„ AUC u lidí “), včetně benigních a maligních nádorů původu granulosa / theca a benigní nádory původu epiteliálních buněk. V těchto studiích byly hlodavce ošetřeny během reprodukčního života, kdy jejich vaječníky byly funkční a vysoce citlivé na hormonální stimulaci. Na rozdíl od vysoké citlivosti vaječníků v tomto modelu hlodavců je lidský vaječník po menopauze relativně necitlivý na stimulaci pohlavními hormony.
Raloxifen nebyl genotoxický v žádném z mnoha provedených testů.
Účinky na reprodukci a vývoj pozorované u zvířat jsou v souladu se známým farmakologickým profilem raloxifenu. V dávkách v rozmezí od 0,1 do 10 mg / kg denně podávaných samicím potkanů raloxifen přerušil jejich estrusové cykly během léčebného období, ale nezdržoval období plodného páření po přerušení léčby a jen okrajově to mělo za následek snížení potomstva, prodloužení těhotenství a změna délky událostí v novorozeneckém vývoji. Při podávání v období před hnízděním raloxifen zpozdil a přerušil uhnízdění embryí, což mělo za následek prodloužení březosti a snížení počtu potomků, ale nemělo to vliv na vývoj potomstva při odstavu. Teratologické studie byly provedeny u králíků a potkanů. U králíků, potratů a byla pozorována nízká míra defektů komorového septa (≥ 0,1 mg / kg) a hydrocefalu (≥ 10 mg / kg). Zpoždění vývoje plodu, malformace se vyskytly u potkanů. žebra a cysty ledvin (≥ 1 mg / kg).
Raloxifen je účinný antiestrogen na krysí děloze a bylo prokázáno, že brání růstu prsních nádorů závislých na estrogenu u potkanů a myší.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Jádro tabletu:
Glykolát sodného škrobu (Primogel)
Monohydrát kyseliny citronové
Mikrokrystalická celulóza
Difázický fosforečnan vápenatý
Poloxamer 407
Stearát hořečnatý
Potah tablety: Hypromelóza
Monohydrát laktózy
Oxid titaničitý (E171)
Macrogol / PEG 4000.
06.2 Neslučitelnost
Irelevantní.
06.3 Doba platnosti
3 roky
06.4 Zvláštní opatření pro skladování
Uchovávejte blistr v původním obalu, aby byl chráněn před světlem a vlhkostí. Chraňte před mrazem.
06.5 Charakter vnitřního obalu a obsah balení
Tablety Raloxifene Sandoz jsou baleny v průhledném PVC / PE / PVDC blistru s hliníkovou fólií.
Krabice obsahují 14, 28, 30, 84 nebo 90 tablet.
Na trhu nemusí být všechny velikosti balení.
06.6 Návod k použití a zacházení
Žádné zvláštní pokyny
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Sandoz S.p.A., L.go U. Boccioni 1, 21040 Origgio (VA)
08.0 REGISTRAČNÍ ČÍSLO
„60 mg potahované tablety“ 14 tablet v PVC / PE / PVDC / AL blistru - AIC č. 040742013 /
„60 mg potahované tablety“ 28 tablet v PVC / PE / PVDC / AL blistru - AIC č. 040742025 /
„60 mg potahované tablety“ 30 tablet v PVC / PE / PVDC / AL blistru - AIC č. 040742037 /
„60 mg potahované tablety“ 84 tablet v PVC / PE / PVDC / AL blistru - AIC č. 040742049 /
„60 mg potahované tablety“ 90 tablet v PVC / PE / PVDC / AL blistru - AIC č. 040742052 /
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
18/04/2013