Aktivní složky: Oxytryptofan (L-5-hydroxytryptofan)
Tript-OH 50 mg tvrdé tobolky Tript-OH 100 mg tvrdé tobolky Tript-OH 200 mg tvrdé tobolky Tript-OH 25 mg granule pro perorální roztok
Indikace Proč se používá Tript-oh? K čemu to je?
Tript-OH obsahuje účinnou látku L-5-hydroxytryptofan, látku, která zprostředkovává chemické reakce v mozku a ze které pochází serotonin, přírodní látka přítomná v těle.
Tript-OH je indikován k léčbě „postanoxického myoklonusu“, tj. Násilné a nedobrovolné kontrakce svalu nebo skupiny svalů, ke které dochází po poklesu nebo nepřítomnosti kyslíku v mozku.
Kontraindikace Pokud by Tript-oh neměl být používán
Neužívejte Tript-OH
- jestliže jste alergický (á) na L-5-hydroxytryptofan nebo na kteroukoli další složku tohoto přípravku
- jestliže máte závažné selhání ledvin.
Opatření pro použití Co potřebujete vědět před užitím Tript-oh
Před užitím přípravku Tript-OH se poraďte se svým lékařem nebo lékárníkem.
Váš lékař může před předepsáním Tript-OH provést testy k vyhodnocení funkce ledvin a srdce.
Jak bylo uvedeno u doplňků stravy na bázi L-tryptofanu, Tript-OH může také vést k onemocnění, které způsobuje zesílení kůže (syndrom sklerodermie) nebo zvýšení typu bílých krvinek (eozinofilů) doprovázené bolestí svalů . (syndrom eozinofilie a myalgie).
Během léčby může lékař pravidelně podstupovat klinická vyšetření a krevní testy ke zjištění časných svalových problémů nebo zvýšení počtu bílých krvinek (eozinofilů) ve vaší krvi.
Před užitím Tript-OH řekněte svému lékaři:
- pokud máte nebo jste měl sebepoškozující chování nebo sebevražedné myšlenky, protože Trip-OH může zvýšit riziko vzniku sebevražedných sklonů, zvláště na začátku léčby a v případě změny dávky., Váš lékař vás bude během Tript- pečlivě sledovat. OH léčba,
Sdělte svému lékaři nebo svému pečovateli, aby sdělili svému lékaři, pokud během léčby přípravkem Tript-OH zaznamenáte:
- zhoršení vašeho stavu,
- změny chování
- vzhled sebevražedného chování nebo myšlenek. Během léčby přípravkem Tript-OH se u vás nevyvine závislost (ztráta účinnosti léku v průběhu času) ani závislost.
Interakce Které léky nebo potraviny mohou ovlivnit účinek Tript-oh
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval (a) nebo které možná budete používat.
Informujte svého lékaře, pokud používáte jeden nebo více níže uvedených léků, protože vás budou během léčby přípravkem Tript-OH sledovat:
- léky používané k léčbě deprese (inhibitory monoaminooxidázy, tricyklická a kvadricyklická antidepresiva)
- alfa methyldopa (lék používaný k léčbě vysokého krevního tlaku)
- methysergid (lék používaný k léčbě migrény)
Varování Je důležité vědět, že:
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek užívat.
Pokud jste těhotná nebo kojíte, lék vám bude předepsán pouze tehdy, když je to zjevně nutné a pod přímým dohledem vašeho lékaře.
Řízení dopravních prostředků a obsluha strojů
Nejsou známy žádné negativní účinky přípravku Tript-OH na schopnost řídit nebo obsluhovat stroje.
Tript-OH granule pro perorální roztok obsahuje sacharózu
Pokud vám lékař řekl, že nesnášíte některé cukry, kontaktujte svého lékaře před užitím tohoto léčivého přípravku. Tento léčivý přípravek obsahuje 5 g sacharózy v jedné dávce. To je třeba vzít v úvahu u lidí s diabetes mellitus. Může to být špatné pro vaše zuby.
Dávka, způsob a doba podání Jak používat Tript-oh: Dávkování
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud máte pochybnosti, poraďte se se svým lékařem nebo lékárníkem.
Doporučená dávka je 600-1000 mg denně ve 3 oddělených podáních.
Obsah jednoho sáčku rozpusťte v půl sklenici vody.
Délka léčby se může u jednotlivých pacientů lišit a v některých případech může trvat několik měsíců. Neměli byste léčbu ukončit náhle a bez předchozí konzultace s lékařem.
Jestliže jste zapomněl (a) užít Tript-OH
Nezdvojnásobujte následující dávku, abyste nahradil (a) vynechanou dávku.
Jestliže jste přestal užívat Tript-OH
Neměli byste léčbu ukončit náhle a bez předchozí konzultace s lékařem.
Máte -li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře.
Předávkování Co dělat, když jste užil příliš mnoho Tript-oh
V případě náhodného požití nadměrné dávky Tript-OH okamžitě informujte svého lékaře nebo jděte do nejbližší nemocnice.
K dnešnímu dni nebyly hlášeny žádné případy požití předávkování přípravkem Tript-OH.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Tript-oh
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Po podání vysokých dávek Tript-OH byly příležitostně hlášeny následující:
- nevolnost
- mírné žaludeční potíže
Někdy byly hlášeny následující:
- Změny krevního tlaku (návrat k normálu do 48 hodin)
Zřídka byly hlášeny:
- Sebevražedné myšlenky a chování
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48100 41 Praha 10 Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
Expirace a retence
Uchovávejte v původním obalu, aby byl přípravek chráněn před světlem.
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na obalu za EXP. Datum exspirace se vztahuje k poslednímu dni uvedeného měsíce.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Jiná informace
Co Tript-OH obsahuje
Tript-OH tvrdé tobolky
- Účinnou látkou je L-5-hydroxytryptofan. Jedna tobolka obsahuje 50 mg nebo 100 mg nebo 200 mg L-5-hydroxytryptofanu.
- Dalšími složkami jsou škrob, mannitol, stearát hořečnatý. • Kapsle se skládá ze zvířecí želatiny, indigokarmínu (tobolky 50 mg a 200 mg), oxidu titaničitého, žlutého oxidu železitého (tobolky 100 mg a 200 mg), erythrosinu (tobolky 100 mg a 200 mg).
Tript-OH 25 mg granule pro perorální roztok
- Léčivou látkou je L-5-hydroxytryptofan. Každý sáček obsahuje 25 mg L-5-hydroxytryptofan.
- Dalšími složkami jsou meruňkové aroma, makrogol 4000, sacharóza.
Popis, jak vypadá Tript-OH a obsah balení
Každé balení 50 mg tvrdých tobolek Tript-OH obsahuje jeden blistr s 30 tvrdými tobolkami. Každé balení 100 mg tvrdých tobolek Tript-OH obsahuje jeden blistr s 20 tvrdými tobolkami. Každé balení 200 mg tvrdých tobolek Tript-OH obsahuje jeden blistr s 20 tvrdými tobolkami. Každé balení 25 mg granulátu pro perorální roztok Tript-OH obsahuje 20 sáčků po 5 g granulí.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
TRIPT-OH
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
TRIPT-OH 50 mg tvrdé tobolky
Jedna 50 mg tvrdá tobolka obsahuje:
Aktivní princip
L-5-hydroxytryptofan 50 mg
TRIPT-OH 100 mg tvrdé tobolky
Jedna 100mg tvrdá tobolka obsahuje:
Aktivní princip
L-5-hydroxytryptofan 100 mg
TRIPT-OH 200 mg tvrdé tobolky
Jedna 200 mg tvrdá tobolka obsahuje:
Aktivní princip
L-5-hydroxytryptofan 200 mg
TRIPT-OH 25 mg granule pro perorální roztok
Jeden 25mg sáček obsahuje:
Aktivní princip
L-5-hydroxytryptofan 25 mg
Pomocné látky viz 6.1
03.0 LÉKOVÁ FORMA
Tvrdé a granulované tobolky pro perorální roztok ve sáčcích.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Postanoxický myoklonus.
04.2 Dávkování a způsob podání
Dospělí: 600-1000 mg / den. Denní dávka by měla být rozdělena do tří dávek. Obsah sáčku by měl být rozpuštěn v půl sklenici vody.
04.3 Kontraindikace
Těžká renální insuficience, přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Pokud jde o možnost, že přípravek, podobně jako je uváděn také po použití doplňků stravy na bázi L-tryptofanu, může vést k syndromu sklerodermie a syndromu eosinofiliální myalgie, považuje se za vhodné, aby byli léčení pacienti vystaveni pravidelné klinické kontroly a leukocytový vzorec, aby bylo možné včas detekovat přítomnost myalgie nebo možné hypereosinofilie.
V některých případech je vhodné před léčbou provést důkladné vyšetření ledvin a srdce.
Droga nepředstavuje žádné riziko závislosti nebo závislosti.
Sebevražedné myšlenky / chování:
Sebevražda / sebevražedné myšlenky:
Deprese je spojena se zvýšeným rizikem sebevražedných myšlenek, sebepoškozování a sebevraždy (sebevražda / související příhody). Toto riziko přetrvává, dokud nedojde k významné remisi. Protože během prvních nebo bezprostředních týdnů léčby nemusí dojít ke zlepšení, měli by být pacienti pečlivě sledováni, dokud nedojde ke zlepšení. Obecně je klinickou zkušeností, že riziko sebevraždy se může v počátečních fázích zlepšování zvýšit.
Se zvýšeným rizikem sebevražedného chování mohou být spojeny i další psychiatrické stavy, pro které je přípravek TRIPT-OH předepisován. Tyto stavy mohou být navíc spojeny s těžkou depresivní poruchou. Při léčbě pacientů s velkými depresivními poruchami by proto měla být dodržována stejná opatření jako při léčbě pacientů s jinými psychiatrickými poruchami.
Pacienti s anamnézou sebevražedného chování nebo myšlenek nebo vykazující významný stupeň sebevražedných myšlenek před zahájením léčby mají zvýšené riziko sebevražedných myšlenek nebo pokusů o sebevraždu a měli by být během léčby pečlivě sledováni.Klinické studie prováděné s antidepresivy ve srovnání s placebem v terapii psychiatrických poruch prokázal zvýšené riziko sebevražedného chování ve věkové skupině do 25 let pacientů léčených antidepresivy ve srovnání s placebem.
Léková terapie antidepresivy by měla být vždy spojena s pečlivým sledováním pacientů, zejména těch s vysokým rizikem, zejména v počátečních fázích léčby a po změnách dávky. Pacienti (nebo pečovatelé) by měli být upozorněni na nutnost sledovat a okamžitě hlásit svému lékaři jakékoli klinické zhoršení, nástup sebevražedného chování nebo myšlenek nebo změny v chování.
Uchovávejte tento přípravek mimo dosah dětí
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
L-5-HTP je možné spojit s jinými specifickými terapiemi (například anxiolytiky). Alfa-methyldopa a methysergid blokují periferní dekarboxylaci TRIPT-OH; proto u pacientů léčených těmito látkami by měl být lék podáván opatrně.
Spojení s IMAO by mělo být prováděno opatrně.Je třeba mít na paměti možné posílení tricyklických a kvadricyklických antidepresiv, u nichž může být nutné snížit dávky.
04.6 Těhotenství a kojení
Teratogenní studie vyloučily negativní účinky na plod u zvířat.Používání přípravku TRIPT-OH během březosti a laktace by však mělo být omezeno na případy naprosté nezbytnosti pod přímým dohledem lékaře.
04.7 Účinky na schopnost řídit a obsluhovat stroje
TRIPT-OH neovlivňuje schopnost řídit a obsluhovat stroje.
04.8 Nežádoucí účinky
Ve velkých dávkách může droga příležitostně způsobit nevolnost a menší žaludeční poruchy; v tomto případě obecně stačí snížit dávku na několik dní a poté se vrátit k užitečné dávce; v případě potřeby lze použít antacidová léčiva nebo modifikátory chování trávicího systému.Někdy lze pozorovat mírné změny krevního tlaku s návratem k normálu do 48 hodin.
Vzácné: sebevražedné myšlenky / chování (viz bod 4.4 Zvláštní upozornění a zvláštní opatření pro použití).
04.9 Předávkování
Protože L-5-HTP je biologická látka, nejsou na klinice hlášeny žádné příznaky předávkování.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Léčivou látkou přípravku TRIPT-OH je L-5-hydroxytryptofan, přímý fyziologický prekurzor serotoninu, který hraje v mozku roli nepostradatelného chemického mediátoru.
ATC: N06AX01
Mezi různými patogenetickými faktory psychických (zejména deprese) a neurologických onemocnění je role, kterou hrají biochemické alterace mozku, již dlouho zkoumána: byl proveden velký výzkum změn v metabolismu biogenních aminů, až po hypotézu „aminu“ "patogeneze výše uvedených poruch."
Existuje dostatek důkazů, které lze považovat za důležité v genezi neuropsychiatrických poruch, „změně mozkové aktivity“ způsobené nerovnováhou v syntéze, skladování, uvolňování nebo inaktivaci aminů a zejména serotoninu: to je ve skutečnosti v mozku sníženo tkáň depresivních jedinců, jak se snížila, a v likéru těchto pacientů rychlost jejího metabolitu, „kyseliny 5-hydroxyindolactové. Byla také zjištěna pozitivní korelace mezi závažností deprese a koncentrací tohoto metabolitu, stejně jako zvýšení fází klinického zotavení po léčbě elektrošoky nebo tricyklickými a anti-MAO antidepresivy Podobně existuje nedostatek serotoninu u některých neurologických syndromů. Protože exogenní serotonin je nepoužitelný, musí být syntetizován v akčních místech počínaje prekurzorovou aminokyselinou: tryptofanem. Ale pouze 1% exogenního tryptofanu je transformováno na serotonin. Naopak L-5-hydroxytryptofan snadno prochází hematoencefalickou bariérou, vyhýbá se nucenému průchodu tryptofan-hydroxylací a díky přítomnosti specifického enzymu, 5-hydroxytryptofan-dekarboxylázy v mozkové tkáni, je zcela přeměněn na serotonin.
05.2 Farmakokinetické vlastnosti
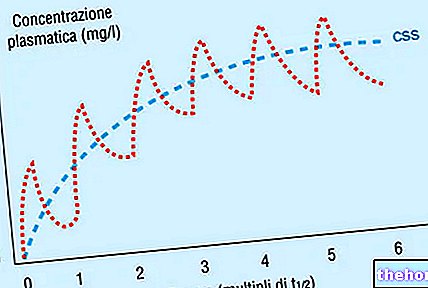
L-5-HTP je dobře absorbován orálně; na rozdíl od svého prekurzoru se neváže na syrovátkové bílkoviny a je rychle dekarboxylován. Průchod hematoencefalickou bariérou je stejně rychlý.U potkanů albínů po podání L-5-HTP dochází ke zvýšení cerebrálního serotoninu, který dosahuje svého vrcholu za 30 minut. Mcg. U opic dávka 30 mg / kg výrazně zvyšuje hladinu serotoninu v mozku za hodinu, dvakrát až šestkrát v závislosti na zkoumaných oblastech. K eliminaci dochází ledvinami ve formě kyseliny 5-hydroxyindolové. Octový, serotoninový katabolit . Po jednorázovém perorálním podání 200 mg / kg u potkanů se vrchol eliminace objeví ve 24. hodině.
05.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje na základě konvenčních studií farmakologické bezpečnosti, toxicity po opakovaném podávání, genotoxicity, karcinogenního potenciálu a reprodukční toxicity neodhalily žádné riziko pro člověka.
Studie prováděné na potkanech a myších ukázaly, že LD50 je zanedbatelný ve srovnání s dávkami očekávanými v terapii (LD50 per os u myší 2500 mg / kg: LD50 i.p. 1400 mg / kg).
Chronická toxicita studovaná u psa v dávkách 25 a 50 mg / kg po dobu 16 týdnů neprokázala žádnou změnu tělesné hmotnosti, různých orgánů a systémů, ani hematologických a krevních chemických parametrů. Mírná albuminurie se objevila u potkanů v dávkách 100 mg / kg.
U koček endoduodenální podání 15 mg / kg nezpůsobuje změny krevního tlaku, srdeční dynamiky, duodenální motility.
L-5-HTP nevykazoval teratogenní aktivitu u potkanů a králíků.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
TRIPT-OH 50 mg tvrdé tobolky
Pomocné látky:
škrob, mannitol, stearát hořečnatý.
Komponenty kapslí: indigokarmín, oxid titaničitý, želatina.
TRIPT-OH 100 mg tvrdé tobolky
Pomocné látky:
škrob, mannitol, stearát hořečnatý.
Komponenty kapslí: oxid titaničitý, želatina, erythrosin, žlutý oxid železitý.
TRIPT-OH 200 mg tvrdé tobolky
Pomocné látky:
škrob, mannitol, stearát hořečnatý.
Komponenty kapslí: oxid titaničitý, želatina, indigokarmín, erythrosin, žlutý oxid železitý.
TRIPT-OH 25 mg granule pro perorální roztok
Pomocné látky:
meruňková příchuť, makrogol 4000, sacharóza.
06.2 Neslučitelnost
L-5-HTP nepředstavuje absolutní inkompatibilitu s jinými specifickými léky, ale je třeba mít na paměti při používání jakékoli jevy interakce s jinými psychotropními léky.
06.3 Doba platnosti
Stabilita je 3 roky pro všechna balení.
06.4 Zvláštní opatření pro skladování
Výrobek by měl být skladován mimo dosah světla.
06.5 Charakter vnitřního obalu a obsah balení
Karton 30 tvrdých tobolek po 50 mg v blistru
Krabička s 20 tvrdými tobolkami po 100 mg v blistru
Krabička s 20 tvrdými tobolkami po 200 mg v blistru
Krabice s 20 sáčky po 5 g granulí
obsahující 25 mg účinné látky
06.6 Návod k použití a zacházení
Obsah sáčku by měl být rozpuštěn v půl sklenici vody.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Sigma-Tau Industrie Farmaceutiche Riunite S.p.A.
Viale Shakespeare, 47 - 00144 Řím
Prodejce na prodej
BIOFUTURA PHARMA S.p.A. - Via Pontina km 30,400 - 00040 Pomezia (RM)
08.0 REGISTRAČNÍ ČÍSLO
Tvrdé tobolky 50 mg AIC č. 024158014
Tvrdé tobolky 100 mg AIC č. 024158026
Tvrdé tobolky 200 mg AIC č. 024158040
5 g sáčků granulí AIC č. 024158038
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Oprávnění
50 mg tvrdé tobolky: březen 1980
100 mg tvrdé tobolky: březen 1980
200 mg tvrdé tobolky: červenec 1987
5 g sáčků granulí: březen 1980
Obnovení autorizace
Června 2000
10.0 DATUM REVIZE TEXTU
01/07/2007















----tiamfenicolo.jpg)