Účinné látky: cyklofosfamid
Endoxan Baxter 50 mg potahované tablety
Endoxan Baxter 200 mg prášek pro injekční roztok
Endoxan Baxter 500 mg prášek pro injekční roztok
Endoxan Baxter 1 g prášek pro injekční roztok
Proč se používá Endoxan Baxter? K čemu to je?
FARMAKOTERAPEUTICKÁ KATEGORIE
Antineoplastické, analogy dusičnaté hořčice
TERAPEUTICKÉ INDIKACE
Cytostatická léčba
Kontraindikace Kdy by neměl být Endoxan Baxter používán
Endoxan Baxter by neměl být podáván pacientům s:
- přecitlivělost na léčivou látku, její metabolity nebo na kteroukoli pomocnou látku
- těžce narušená funkce kostní dřeně (zejména u pacientů, kteří podstoupili předběžnou léčbu cytotoxickými látkami a / nebo radioterapii),
- zánět močového měchýře (cystitida),
- obstrukce toku moči,
- probíhající infekce,
- během těhotenství a kojení.
Opatření pro použití Co potřebujete vědět před užitím přípravku Endoxan Baxter
Rizikové faktory toxicity cyklofosfamidu a jejich důsledky popsané v tomto a dalších oddílech mohou představovat kontraindikace, pokud léčivý přípravek není používán k léčbě život ohrožujících stavů. V těchto situacích je nutné individuální posouzení poměru očekávaného přínosu / rizika.
UPOZORNĚNÍ
Toxicita ledvin a močových cest
- Během léčby cyklofosfamidem byla hlášena hemoragická cystitida, pyelitida, uretritida a hematurie. Může se také vyvinout ulcerace / nekróza močového měchýře, fibróza / kontraktura a sekundární nádory.
- Urotoxicita může vyžadovat přerušení léčby.
- V případě fibrózy, krvácení nebo sekundárních nádorů může být nutná cystektomie.
- Byly hlášeny případy urotoxicity s fatálními následky.
- Urotoxicita se může objevit při krátkodobé i dlouhodobé léčbě cyklofosfamidem. Po jednorázové dávce cyklofosfamidu byla hlášena hemoragická cystitida.
- Následná nebo souběžná radioterapie nebo léčba busulfanem může zvýšit riziko hemoragické cystitidy vyvolané cyklofosfamidem.
- Cystitida je zpočátku sterilní, ale může dojít k sekundární mikrobiální kolonizaci.
- Před zahájením terapie bude nutné odstranit nebo opravit eferentní obstrukce močových cest, cystitidu a infekce.
- Adekvátní terapie Uromitexanem (INN: mesna) nebo silná hydratace mohou výrazně snížit frekvenci a závažnost toxicity močového měchýře. Zajistěte, aby pacienti pravidelně vyprazdňovali močový měchýř.
- Pokud se během léčby přípravkem Endoxan Baxter objeví cystitida spojená s mikro nebo makrohematurií, přerušte léčbu přípravkem Endoxan Baxter až do normalizace. K tomu obvykle dochází několik dní po vysazení léku, ale cystitida může také přetrvávat.
- V případě závažné hemoragické cystitidy by léčba přípravkem Endoxan Baxter měla být obecně ukončena.
- Cyklofosfamid je také spojován s nefrotoxicitou včetně tubulární nekrózy.
- V souvislosti s podáváním cyklofosfamidu byla hlášena hyponatrémie spojená se zvýšenou celkovou tělesnou vodou, akutní intoxikací vodou a syndromem podobným SIADH (syndrom nedostatečné sekrece antidiuretického hormonu). Byly také hlášeny fatální následky.
- Pacienti s poruchou funkce ledvin by měli být během léčby přípravkem Endoxan Baxter pečlivě sledováni na přítomnost erytrocytů a další známky uro / nefrotoxicity (viz také „Doporučení pro úpravu dávkování u pacientů s jaterní nebo renální insuficiencí“ v části „Dávka, metoda a doba podání “).
Myelosuprese, Imunosuprese, Infekce
Obecně by měl být přípravek Endoxan Baxter, stejně jako všechna ostatní cytostatika, používán s maximální péčí u slabých nebo starších subjektů au subjektů, které již dříve podstoupily radioterapii.
Jedinci s oslabeným imunitním systémem, jako jsou pacienti s diabetes mellitus, chronickým onemocněním jater nebo ledvin, by měli být také pečlivě sledováni.
- Léčba cyklofosfamidem může způsobit myelosupresi a významné potlačení imunitní odpovědi.
- Očekává se těžká myelosuprese, zejména u pacientů, kteří dříve podstoupili chemoterapii a / nebo radioterapii nebo u pacientů s poruchou funkce ledvin.
- Cyklofosfamidem indukovaná myelosuprese může způsobit leukopenii, neutropenii, trombocytopenii (spojenou s vyšším rizikem krvácení) a anémii.
- Silná imunosuprese vedla k závažným, někdy smrtelným infekcím. Byly také hlášeny sepse a septický šok. Mezi infekce hlášené cyklofosfamidem patří jak zápal plic, tak další infekce bakteriálního, plísňového, virového, protozoálního a parazitického původu.
- Latentní infekce lze reaktivovat. Reaktivace byla hlášena u různých infekcí bakteriálního, houbového, virového, protozoálního a parazitárního původu.
- S infekcemi je třeba zacházet odpovídajícím způsobem.
- Podle uvážení ošetřujícího lékaře může být v některých případech neutropenie indikována antimikrobiální profylaxe.
- V případě neutropenické horečky a / nebo leukopenie by měla být jako profylaxe podávána antibiotika a / nebo antimykotika.
- V případě potřeby by měl být cyklofosfamid používán s opatrností u pacientů s těžkým poškozením funkce kostní dřeně a u pacientů s těžkou imunosupresí.
- Léčba cyklofosfamidem nemusí být indikována nebo by měla být ukončena nebo by mělo být sníženo dávkování u pacientů, kteří mají nebo se u nich vyvine závažná infekce.
- Čím vyšší je dávka, tím je teoreticky pokles počtu buněk a destiček v periferní krvi a času potřebného k zotavení vyšší.
- Nejnižší počty leukocytů a krevních destiček se obvykle vyskytují jeden až dva týdny po zahájení léčby.Kostní dřeň se obnovuje poměrně rychle a hodnoty krve se normálně normalizují asi po 20 dnech.
- Proto je vhodné, aby během léčby všichni pacienti prováděli pečlivou hematologickou kontrolu s pravidelně prováděným krevním obrazem. o Před každým podáním a ve vhodných intervalech, v případě potřeby každý den, by měl být zkontrolován počet bílých krvinek a krevních destiček a hodnoty hemoglobinu. o Kontroly leukocytů musí být prováděny pravidelně během léčby, v intervalech 5-7 dní na začátku léčby a každé 2 dny, pokud počet klesne pod 3000 / mm3 (viz také odstavec „Dávka, způsob a doba podání“ ).
- Pokud to není nezbytně nutné, Endoxan Baxter by neměl být podáván pacientům s počtem bílých krvinek pod 2500 / µl a / nebo počtem krevních destiček pod 50 000 / µl.
- Rovněž se doporučuje pravidelné sledování sedimentu moči na přítomnost erytrocytů.
Kardiotoxicita, použití u pacientů s onemocněním srdce
- Během léčby cyklofosfamidem byla hlášena myokarditida a myopikarditida, které mohou být doprovázeny výrazným perikardiálním výpotkem a srdeční tamponádou a vedly k závažnému, někdy smrtelnému městnavému srdečnímu selhání.
- Histopatologické vyšetření prokázalo zejména hemoragickou myokarditidu, hemoperikard se vyskytoval jako sekundární účinek hemoragické myokarditidy a nekrózy myokardu.
- Akutní srdeční toxicita byla pozorována při jednorázové dávce cyklofosfamidu nižší než 20 mg / kg.
- Po expozici léčebným režimům včetně cyklofosfamidu byly u pacientů s jinými příznaky kardiotoxicity nebo bez nich hlášeny supraventrikulární arytmie (včetně fibrilace síní a flutteru) a ventrikulární arytmie (včetně závažných prodloužení QT spojených s komorovou tachyarytmií).
- Bylo prokázáno, že použití vysokých dávek cyklofosfamidu u pacientů v pokročilém věku a u pacientů, kteří měli předchozí radioterapii v srdeční oblasti a / nebo souběžnou léčbu antracykliny a pentostatinem nebo jinými kardiotoxickými látkami (viz bod 4.5).) může zesílit kardiotoxický účinek přípravku Endoxan Baxter. V této souvislosti bude nutné pravidelně kontrolovat elektrolyty a věnovat zvláštní pozornost pacientům s „anamnézou srdečních chorob“.
Plicní toxicita
- Souběžně s léčbou cyklofosfamidem nebo po ní byla hlášena pneumonie a plicní fibróza. Byly také hlášeny plicní venookluzivní choroby a jiné formy plicní toxicity. Byla hlášena plicní toxicita vedoucí k respiračnímu selhání.
- Zatímco výskyt plicní toxicity související s cyklofosfamidem je nízký, prognóza pro postižené pacienty je špatná.
- Pozdní nástup pneumonie (více než 6 měsíců po zahájení léčby cyklofosfamidem) se zdá být spojen se zvláště vysokou úmrtností. Pneumonie může také vzniknout roky po léčbě cyklofosfamidem.
- Po jedné dávce cyklofosfamidu byla hlášena akutní plicní toxicita.
Sekundární nádory
- Stejně jako u cytostatické terapie obecně, léčba cyklofosfamidem také nese riziko sekundárních nádorů a jejich prekurzorů jako pozdních následků.
- Zvyšuje riziko vzniku karcinomu močových cest a myelodysplastických změn, které částečně procházejí do akutní leukémie. Mezi další rakoviny hlášené po léčbě cyklofosfamidem nebo cyklofosfamidem patří lymfom, rakovina štítné žlázy a sarkomy.
- V některých případech se sekundární rakovina vyvinula několik let po ukončení léčby cyklofosfamidem. Nádory byly také hlášeny po expozici in utero.
- Riziko rakoviny močového měchýře lze výrazně snížit prevencí hemoragické cystitidy.
Venookluzivní patologie jater
- Venookluzivní onemocnění jater (VOLD) bylo hlášeno u pacientů užívajících cyklofosfamid.
- .. Jako hlavní rizikový faktor pro rozvoj VOLD byla identifikována cytoredukční léčba v rámci přípravy na transplantaci kostní dřeně, která se skládá z cyklofosfamidu v kombinaci s integrálním ozařováním, busulfanem nebo jinými činidly (viz bod 4.5). Po cytoredukční terapii se klinický syndrom klinicky vyvíjí 1 až 2 týdny po transplantaci a je charakterizován rychlým přírůstkem hmotnosti, bolestivou hepatomegalií, ascitem a hyperbilirubinémií / žloutenkou.
- Postupný vývoj VOLD byl však zaznamenán u pacientů dlouhodobě léčených nízkými dávkami imunosupresivních dávek cyklofosfamidu.
- Jako komplikace VOLD se může vyvinout hepatorenální syndrom a multiorgánové selhání. U VOLD spojeného s cyklofosfamidem byl hlášen smrtelný výsledek.
- Mezi rizikové faktory, které předurčují pacienta k rozvoji VOLD s vysokodávkovými cytoredukčními terapiemi, patří: o již existující poruchy funkce jater o radiační terapie břicha a nízké skóre výkonu.
Genotoxicita
- Endoxan Baxter je genotoxický a mutagenní v somatických i zárodečných buňkách samců i samic. Ženy by se proto měly během užívání přípravku Endoxan Baxter vyvarovat otěhotnění a muži by měli zabránit početí dětí.
- Muži by se měli vyhnout početí dětí po dobu až 6 měsíců po ukončení léčby.
- Studie na zvířatech naznačují, že expozice oocytů během vývoje folikulů může mít za následek nižší míru implantace a nerizikového těhotenství a větší riziko malformací. Tento účinek je třeba vzít v úvahu v případě oplodnění nebo těhotenství. Dobrovolný po ukončení léčby cyklofosfamidem Přesné trvání vývoje folikulů u lidí není známo, ale může být delší než 12 měsíců.
- Sexuálně aktivní muži a ženy budou muset během tohoto období používat účinné metody antikoncepce. Viz také část 4.6.
Účinek na plodnost
- Cyklofosfamid zasahuje do oogeneze a spermatogeneze a může způsobit neplodnost u obou pohlaví.
- Zdá se, že vývoj neplodnosti závisí na dávce cyklofosfamidu, délce léčby a stavu gonadálních funkcí v době léčby.
- Sterilita vyvolaná cyklofosfamidem může být u některých pacientů nevratná.
Pacientky
- Přechodná nebo trvalá amenorea spojená se sníženou sekrecí estrogenu a zvýšenou sekrecí gonadotropinů se vyvíjí u významné části žen léčených cyklofosfamidem.
- Zejména u zralejších žen může být amenorea trvalá.
- Oligomenorea byla také hlášena v souvislosti s léčbou cyklofosfamidem.
- Dívky léčené cyklofosfamidem v předpubescenci obecně vyvíjejí sekundární sexuální charakteristiky normálně a mají pravidelné cykly.
- Dívky ošetřené cyklofosfamidem v prepubescenci následně počaly děti.
- Dívky léčené cyklofosfamidem, které si po ukončení léčby zachovaly ovariální funkce, mají vyšší riziko vzniku předčasné menopauzy (přerušení cyklu před 40. rokem věku).
Mužští pacienti
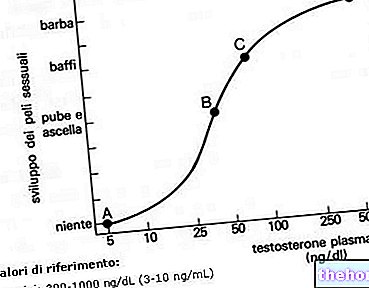
- U mužů léčených cyklofosfamidem se může vyvinout oligospermie nebo azoospermie, které jsou normálně spojeny se zvýšenou sekrecí gonadotropinu, ale s normální sekrecí testosteronu.
- Sexuální síla a libido u těchto pacientů obecně nejsou narušeny.
- U chlapců léčených předpubescenčním cyklofosfamidem se mohou normálně vyvinout sekundární sexuální charakteristiky, ale mohou mít oligospermii nebo azoospermii.
- Atrofie varlat se může vyskytovat v různé míře.
- Cyklofosfamidem indukovaná azoospermie je u některých pacientů reverzibilní, i když k reverzibilitě nemusí dojít několik let po ukončení léčby.
- Muži dočasně sterilní cyklofosfamidem později počali děti.
- Protože léčba přípravkem Endoxan Baxter může zvýšit riziko trvalé neplodnosti u mužů, měli by být muži před léčbou informováni o skladování spermií.
Anafylaktické reakce, zkřížená citlivost s jinými alkylačními činidly
- V souvislosti s cyklofosfamidem byly hlášeny anafylaktické reakce včetně reakcí s fatálními následky.
- Byla hlášena možná zkřížená citlivost s jinými alkylačními činidly.
Změna procesu hojení ran
- Cyklofosfamid může interferovat s normálním procesem hojení ran.
OPATŘENÍ
Alopecie
- Byla hlášena alopecie, která se může vyskytovat častěji se zvyšujícím se dávkováním.
- Alopecie může přejít do plešatosti.
- Vlasy by měly po léčbě tímto lékem nebo dokonce během léčby znovu narůst, i když se mohou lišit strukturou a barvou.
Nevolnost a zvracení
- Podávání cyklofosfamidu může způsobit nevolnost a zvracení.
- Je třeba vzít v úvahu aktuální pokyny. o používání antiemetik k prevenci a zlepšení nevolnosti a zvracení.
- Alkohol může zvýšit emetické účinky a nevolnost způsobenou cyklofosfamidem; z těchto důvodů je třeba se vyvarovat konzumace alkoholu u pacientů léčených cyklofosfamidem.
Stomatitida
- Podávání cyklofosfamidu může způsobit stomatitidu (orální mukozitidu)
- Je třeba vzít v úvahu aktuální pokyny pro prevenci a zlepšení stomatitidy.
- Věnujte zvláštní pozornost ústní hygieně, abyste snížili výskyt stomatitidy
Paravenózní podání
- Protože k cytostatickému účinku Endoxanu Baxter dochází po jeho aktivaci, která probíhá hlavně v játrech, existuje v případě náhodného paravenózního podání jen minimální riziko poškození tkáně.
Poznámka:
V případě náhodného podání paravenózní injekcí okamžitě zastavte infuzi, odsajte kapalinu přenesenou aplikovanou kanylou a proveďte další vhodná opatření, např. Oblast zavlažte fyziologickým roztokem a znehybněte končetinu. Použití u pacientů s renální insuficiencí U pacientů s renální insuficiencí, zvláště pokud je závažná, může snížená renální eliminace vést ke zvýšení plazmatických hladin cyklofosfamidu a jeho metabolitů. To může vést ke zvýšené toxicitě a mělo by se to vzít v úvahu při určování dávkování pro tento typ pacienta. Viz také část 4.2.
Použití u pacientů s jaterní insuficiencí
Těžká jaterní insuficience může být spojena se sníženou aktivací cyklofosfamidu. To může změnit účinnost terapie cyklofosfamidem a mělo by se to vzít v úvahu při určování dávky a interpretaci odpovědi na zvolenou dávku. Zneužívání alkoholu může zvýšit riziko vzniku dysfunkce jater.
Použití u pacientů s adrenalektomií
Pacienti s adrenální insuficiencí mohou vyžadovat zvýšené náhradní dávky kortikoidů, pokud jsou vystaveni stresu vyplývajícímu z toxicity cytostatik, včetně cyklofosfamidu.
Diagnostické vyšetřování
U diabetických pacientů je nutné pravidelně kontrolovat hladinu cukru v krvi, aby bylo možné rychle přizpůsobit antidiabetickou terapii (viz také odstavec „Interakce“)
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Endoxan Baxter
Informujte svého lékaře nebo lékárníka o všech lécích, které jste v nedávné době užíval (a), a to i bez lékařského předpisu.
Souběžné nebo následné plánované podávání jiných látek nebo léčebných postupů, které by mohly zvýšit pravděpodobnost nebo závažnost toxických účinků (prostřednictvím farmakodynamických nebo farmakokinetických interakcí), vyžaduje pečlivé individuální zvážení očekávaných přínosů a rizik. Pacienti, kteří dostávají takové kombinace, by měli být pečlivě sledováni s ohledem na příznaky toxicity, a proto by měli umožnit rychlou intervenci. U pacientů léčených cyklofosfamidem a látkami snižujícími jeho aktivaci by mělo být sledováno potenciální snížení terapeutické účinnosti a nutnost úpravy dávkování.
Interakce ovlivňující farmakokinetiku cyklofosfamidu a jeho metabolitů
Při současném podávání alopurinolu nebo hydrochlorothiazidu lze zesílit hypoglykemický účinek sulfonylmočovin a myelosupresivní účinek.
Snížená aktivace cyklofosfamidu může změnit účinnost léčby cyklofosfamidem. Mezi látky, které zpomalují aktivaci cyklofosfamidu, patří:
- Openspitant
- Bupropion
- Busulfan: Podávání vysokých dávek přípravku Endoxan Baxter do 24 hodin po léčbě vysokými dávkami busulfanu může mít za následek snížení clearance a „prodloužení eliminačního poločasu“ cyklofosfamidu.
- Ciprofloxacin: Podávání antibiotik na bázi fluorochinolonů (jako je ciprofloxacin) před zahájením léčby přípravkem Endoxan Baxter (zejména v případě kondicionování před transplantací kostní dřeně) může snížit účinnost přípravku Endoxan Baxter, a proto vést ke zhoršení primární patologie.
- Chloramfenikol: Současné podávání chloramfenikolu vede k prodloužení cyklofosfamidu na polovinu a ke zpomalení metabolismu.
- Flukonazol, itrakonazol: Je známo, že azolová antimykotika (flukonazol, itrakonazol) inhibují aktivitu cyklofosfamidu metabolizující cytochrom P450. U pacientů léčených itrakonazolem byla pozorována zvýšená expozice toxickým metabolitům Endoxanu Baxter.
- Prasugrel
- Sulfonamidy
- Thiotepa: Silná inhibice bioaktivace cyklofosfamidu thiotepou byla pozorována v režimech vysokých dávek chemoterapie, pokud byly podávány jednu hodinu před Endoxan Baxter. Sekvence a načasování podávání těchto dvou látek mohou být kritickými faktory.
Ke zvýšení koncentrace cytotoxických metabolitů může dojít při:
- Allopurinol
- Chloralhydrát
- Cimetidin
- Disulfiram
- Glyceraldehyd
- Induktory lidských jaterních a extrahepatálních mikrozomálních enzymů (např.enzymy cytochromu P450): Potenciální indukce jaterních a extrahepatálních mikrozomálních enzymů by měla být vzata v úvahu v případě předchozí nebo souběžné léčby látkami, o nichž je známo, že indukují zvýšení aktivity takových enzymů, jako je rifampicin, fenobarbital, karbamazepin, benzodiazepiny , fentoin, třezalka a kortikosteroidy.
- Inhibitory proteázy: Souběžné použití inhibitorů proteázy může zvýšit koncentraci cytotoxických metabolitů.U pacientů, kterým byl podáván cyklofosfamid, doxorubicin a etoposid (CDE), bylo použití léčby inhibitorem proteázy spojeno s vyšším výskytem infekcí a neutropenie než s použití léčby založené na NNRTI.
- Ondansetron: Mezi ondansetronem a Endoxanem Baxter (při vysokých dávkách) byly zjištěny farmakokinetické interakce, které vedly ke snížení AUC (plocha pod křivkou) cyklofosfamidu.
Protože grapefruit obsahuje sloučeninu schopnou inhibovat aktivaci cyklofosfamidu a následně jeho účinnost, pacient by neměl konzumovat grapefruit nebo grapefruitovou šťávu.
Farmakodynamické interakce a interakce s neznámými mechanismy ovlivňujícími použití cyklofosfamidu
Kombinace nebo následné použití cyklofosfamidu a dalších látek s podobnou toxicitou může způsobit kombinované (velké) toxické účinky.
Zvýšení hematotoxicity a / nebo imunosuprese může být důsledkem kombinace účinků cyklofosfamidu a například:
- Inhibitory ACE: Inhibitory ACE mohou způsobit leukopenii.
- Natalizumab
- Paclitaxel: Při podání cyklofosfamidu po infuzi paklitaxelu byla hlášena zvýšená hematotoxicita.
- Diuretika na bázi thiazidu nebo zidovudinu
Zvýšená kardiotoxicita může být důsledkem kombinace účinků cyklofosfamidu a například:
- Antracykliny
- Pentostatin
- Cytarabin - Podávání vysokých dávek přípravku Endoxan Baxter a cytarabinu ve stejný den, tedy ve velmi omezeném časovém intervalu, může vést ke zvýšení kardiotoxického účinku s přihlédnutím k tomu, že každá látka je již sama o sobě kardiotoxická.
- Radioterapie do oblasti srdce.
- Trastuzumab
Zvýšení plicní toxicity může být důsledkem kombinace účinků cyklofosfamidu a například:
- Amiodaron
- G-CSF nebo GM-CSF (faktor stimulující kolonie granulocytových makrofágů a faktor stimulující kolonie granulocytů): Zprávy naznačují zvýšené riziko plicní toxicity (pneumonie, alveolární fibróza) u pacientů léčených chemoterapií s cytotoxickými látkami, mezi něž patří Endoxan Baxter a G-CSF nebo GM-CSF.
Zvýšení nefrotoxicity může být důsledkem kombinace účinků cyklofosfamidu a například:
- Amfotericin B
- Indomethacin: Souběžné podávání indomethacinu by mělo být prováděno s maximální péčí, protože v jednom případě byla zjištěna akutní intoxikace vodou.
Zvýšení dalších toxicit:
- Azathioprin: Zvýšené riziko hepatotoxicity (nekróza jater) Busulfan: zvýšený výskyt venookluzivních chorob a mukozitidy.
- Inhibitory proteázy: zvýšený výskyt mukozitidy
Další interakce:
- Alkohol: Snížená protinádorová aktivita byla pozorována u zvířat s rakovinou, když byl souběžně s nízkými perorálními dávkami cyklofosfamidu podáván ethanol (alkohol). U některých pacientů může alkohol zvýšit emetické účinky a nevolnost způsobenou cyklofosfamidem.
- Etanercept: U pacientů s Wegenerovou granulomatózou bylo přidání etanerceptu ke standardní léčbě cyklofosfamidem spojeno s vyšším výskytem nekožních solidních nádorů.
- Metronidazol: U pacienta léčeného cyklofosfamidem a metronidazolem byla pozorována akutní encefalopatie. Příčinná souvislost není jasná.Ve studii na zvířatech byla kombinace cyklofosfamidu a metronidazolu spojena se zvýšenou toxicitou cyklofosfamidu.
- Tamoxifen: Souběžné užívání tamoxifenu a chemoterapie může zvýšit riziko tromboembolických komplikací.
Interakce ovlivňující farmakokinetiku a / nebo účinek jiných léčivých přípravků
- Bupropion: Metabolismus cyklofosfamidu prostřednictvím CYP2B6 může inhibovat metabolismus bupropionu.
- Kumariny: U pacientů léčených warfarinem a cyklofosfamidem byl hlášen zvýšený i snížený účinek warfarinu.
- Cyklosporiny: U pacientů léčených kombinací přípravku Endoxan Baxter a cyklosporinu byla zjištěna nižší sérová koncentrace cyklosporinu než u pacientů, kterým byl podáván samotný cyklosporin. Tato interakce by mohla vést ke zvýšenému výskytu reakcí na odmítnutí.
- Depolarizující svalová relaxancia: Pokud se současně aplikují depolarizující svalové relaxanci (např. Sukcinylcholinhalogenidy), může dojít k prodloužené „apnoe způsobené“ významnou a trvalou inhibicí aktivity cholinesterázy. Pokud byl pacient léčen cyklofosfamidem do 10 dnů od „celkové anestezie, měl by být poučen anesteziolog. "
- Digoxin, β-acetyldigoxin: Bylo hlášeno, že cytostatická léčba zhoršuje střevní absorpci tablet digoxinu a β-acetyldigoxinu.
- Vakcíny: Vzhledem k tomu, že cyklofosfamid má imunosupresivní účinky, může pacient vykazovat sníženou odpověď na souběžné očkování; očkování aktivními vakcínami může být spojeno s infekcí vyvolanou vakcínou.
- Verapamil: Bylo hlášeno, že cytostatická léčba narušuje střevní absorpci perorálně podávaného verapamilu
Varování Je důležité vědět, že:
Plodnost, těhotenství a kojení
Před užitím jakéhokoli léku se poraďte se svým lékařem nebo lékárníkem
- Měl by být zvážen možný průchod Endoxanu Baxter přes mateřskou placentu. Léčba cyklofosfamidem může způsobit abnormality genotypu u mužů a žen.
- Pokud během prvního trimestru těhotenství existují nějaká rizika pro život pacientky, bude naprosto nezbytné poradit se s lékařem, aby bylo možné těhotenství přerušit.
- U dětí narozených matkám léčeným cyklofosfamidem během prvního trimestru těhotenství byly hlášeny malformace. Byly však také hlášeny děti bez malformací narozené ženám vystaveným během prvního trimestru.
- Pokud po prvním trimestru těhotenství nelze léčbu odložit a pacientka si přeje v těhotenství pokračovat, lze po informování pacientky o menším, ale možném riziku teratogenních účinků, použít chemoterapii.
- Expozice cyklofosfamidem in utero může způsobit ukončení těhotenství, zpomalení růstu plodu a fetotoxické účinky vyskytující se u novorozence, včetně leukopenie, anémie, pancytopenie, závažné hypoplazie kostní dřeně a gastroenteritidy.
- Během léčby přípravkem Endoxan Baxter a až 6 měsíců po ukončení léčby by se ženy měly vyvarovat otěhotnění a muži by se měli vyhýbat početí dětí.
- Výsledky studií na zvířatech naznačují, že zvýšené riziko ukončení těhotenství a malformací může přetrvávat i po vysazení cyklofosfamidu, pokud existují oocyty / folikuly, které byly vystaveny cyklofosfamidu v kterémkoli stádiu zrání.
- Pokud se cyklofosfamid používá během těhotenství nebo pokud pacientka otěhotní během užívání tohoto léku nebo po ukončení léčby, měla by být pacientka informována o potenciálních rizicích pro plod.
- Protože cyklofosfamid přechází do mateřského mléka, matky během léčby nebudou muset kojit. U kojenců žen užívajících cyklofosfamid byla hlášena neutropenie, trombocytopenie, nízký hemoglobin a průjem.
- Muži, kteří budou léčeni přípravkem Endoxan Baxter, budou muset být před léčbou informováni o skladování spermií.
Účinky na schopnost řídit a obsluhovat stroje
Vzhledem k možnosti nežádoucích účinků vyplývajících z podávání cyklofosfamidu, jako je nevolnost, zvracení, závratě, rozmazané vidění a zhoršené vidění, které mohou narušit schopnost řídit nebo obsluhovat stroje, bude lékař muset o své schopnosti individuálně rozhodnout. pacient řídit vozidla nebo obsluhovat stroje
Důležité informace o některých složkách
Tablety obsahují laktózu a sacharózu, proto v případě zjištěné nesnášenlivosti cukrů kontaktujte svého lékaře před užitím léku.
Dávkování a způsob použití Jak používat Endoxan Baxter: Dávkování
- Endoxan Baxter by měl podávat pouze lékařský personál se zkušenostmi s onkologií.
- Léčba obvykle začíná intravenózními injekcemi. Pokud to není možné, lze přípravek Endoxan Baxter aplikovat intramuskulárně. Ve zvláštních případech je možná intrapleurální, intraperitoneální nebo in situ aplikace.Pro prodlouženou léčbu nebo terapii udržovací dávkou se po regresi symptomů doporučuje orální podání.
- Aktivace cyklofosfamidu vyžaduje jaterní metabolismus, proto by se podávání mělo přednostně provádět orálně nebo intravenózně.
Parenterální použití
- Léčivé přípravky používané parenterálně by měly být před podáním vizuálně zkontrolovány na přítomnost částic a změnu barvy roztoku, pokud to roztok a obal dovolí.
- Intravenózní podání by mělo být přednostně podáváno jako infuze.
- Aby se snížila pravděpodobnost nežádoucích účinků, které se zdají souviset s rychlostí podávání (např. Otok obličeje, bolest hlavy, ucpaný nos, zánět pokožky hlavy), měl by být léčivý přípravek injekčně nebo infuzí podáván velmi pomalu. Trvání infuze by navíc mělo být přiměřené objemu a typu transportního roztoku, který má být podán.
- Pokud je injekce podána přímo, musí být roztok Endoxan Baxter rekonstituován fyziologickým roztokem (0,9% chlorid sodný). Při přípravě injekčního roztoku postupujte podle pokynů uvedených v bodě 6.6
- Před parenterálním podáním musí být léčivý přípravek zcela rozpuštěn.
Dávkování by mělo být přizpůsobeno potřebám každého jednotlivého pacienta, s přihlédnutím k obecným reakcím a krevnímu obrazu. Pokud není předepsáno jinak, doporučují se následující dávky:
a) kontinuální léčba: 3-6 mg / kg tělesné hmotnosti (ekvivalent 120 - 240 mg / m2 povrchu těla) i.v.;
b) terapie v intervalech 2-5 dnů: 10-15 mg / kg tělesné hmotnosti (odpovídá 400-600 mg / m2 tělesného povrchu) i.v. ;
c) 10-20denní intervalová terapie: 20 až 40 mg / kg tělesné hmotnosti (ekvivalent 800 - 1600 mg / m2 tělesného povrchu) i.v.
Trvání terapie a intervaly mezi jedním a druhým podáním budou záviset na indikacích, na onkologických lécích, které mohou být spojeny s cyklofosfamidem, na celkovém stavu pacienta, na laboratorních parametrech, zejména na krevním obrazu.
Pro udržovací terapii se podává 50-200 mg denně (1-4 potahované tablety), v případě potřeby lze podat vyšší dávky.
Během nebo bezprostředně po požití by mělo být požito nebo podáno dostatečné množství tekutin ke stimulaci diurézy, aby se snížilo riziko toxicity pro moč. Proto by měl být léčivý přípravek přednostně užíván ráno. Je důležité zajistit, aby byl pacient zajištěn s vodou. vyprazdňování močového měchýře v pravidelných intervalech.
Výše uvedené dávkování se týká hlavně léčby, při níž se účinná látka cyklofosfamid používá jako monoterapie. Pokud je přípravek Endoxan Baxter kombinován s jinými cytostatiky podobné toxicity, může být nutné buď snížení dávky, nebo prodloužení intervalu.
Lze očekávat, že použití činidel stimulujících krvetvorbu (faktory stimulující kolonie a činidla stimulující erytropoézu) sníží riziko myelosupresivních komplikací a / nebo pomůže usnadnit plánované dávkování.
Doporučení pro snížení dávky u pacientů s myelosupresí
Doporučení pro úpravu dávkování u pacientů s jaterní nebo renální insuficiencí
- Těžká jaterní nebo renální insuficience vyžaduje snížení dávky.
- Těžká jaterní insuficience může být spojena se sníženou aktivací cyklofosfamidu. To může změnit účinnost terapie cyklofosfamidem a mělo by se to vzít v úvahu při určování dávky a interpretaci odpovědi na zvolenou dávku.
- U pacientů s renální insuficiencí, zvláště pokud je závažná, může snížená renální eliminace vést ke zvýšení plazmatických hladin cyklofosfamidu a jeho metabolitů. To může vést ke zvýšené toxicitě a mělo by se to vzít v úvahu při určování dávkování pro tento typ pacienta.
- Pro hodnoty bilirubinu v séru mezi 3,1 a 5 mg / 100 ml se doporučuje 25% snížení a pro glomerulární filtraci nižší než 10 ml / minutu 50% snížení.
- Cyklofosfamid a jeho metabolity jsou dialyzovatelné, i když mohou existovat rozdíly v clearance podle typu použité dialyzační techniky. U pacientů vyžadujících dialýzu by měl být mezi podáním cyklofosfamidu a dialýzou zachován významný interval.
Senioři
- U starších osob by sledování toxicity a nutnost úpravy dávkování mělo odrážet vyšší frekvenci jaterních, renálních, srdečních nebo jiných orgánových abnormalit a souběžnou přítomnost jiných onemocnění nebo terapii jinými léčivými přípravky.
Zacházení
- Manipulace a příprava cyklofosfamidu by měla být vždy prováděna v souladu s aktuálními pokyny pro bezpečné zacházení s cytotoxickými látkami.
- Potahování tablet brání přímému kontaktu s účinnou látkou pro osoby, které s nimi manipulují. Aby se zabránilo neúmyslnému vystavení účinné látky třetím stranám, tablety by se neměly dělit ani drtit.
Příprava injekčního roztoku:
Endoxan Baxter pro intravenózní podání se připravuje ve skleněných lahvích typu III. K přípravě injekčního roztoku musí být do suchého prášku přidáno následující množství fyziologického roztoku (0,9%chlorid sodný):
Před parenterálním podáním musí být látka zcela rozpuštěna
Látka se snadno rozpouští, pokud se lahve po přidání rozpouštědla (fyziologického roztoku) intenzivně protřepávají půl nebo jednu minutu.
Pokud se látka nerozpustí okamžitě bez zanechání zbytků, je vhodné nechat roztok několik minut odstát, dokud není čirý. Vstřikováním rozpouštědla do láhve vzniká přetlak, kterému lze zabránit zavedením druhé sterilní jehly do gumové zátky, aby vzduch z lahve unikal.
Cyklofosfamid rekonstituovaný ve vodě je hypotonický a neměl by být podáván přímo.
Pokud je cyklofosfamid podáván infuzí, může být rekonstituován přidáním sterilní vody a infuzován do doporučených intravenózních roztoků.
Tento léčivý přípravek je kompatibilní s následujícími infuzními roztoky: roztokem chloridu sodného, roztokem glukózy, roztokem chloridu sodného a glukózy, roztokem chloridu sodného a chloridu draselného, roztokem chloridu draselného a glukózy.
Roztok by měl být vstříknut co nejdříve po přípravě. Doba použitelnosti roztoku: od 2 do 3 hodin.
Předávkování Co dělat, pokud jste užili příliš mnoho přípravku Endoxan Baxter
- Mezi závažné důsledky předávkování patří projevy na dávce závislé toxicity, jako je myelosuprese, urotoxicita, kardiotoxicita (včetně srdečního selhání), venookluzivní onemocnění jater a stomatitida. Viz bod 4.4.
- Protože konkrétní protijed pro cyklofosfamid není znám, doporučuje se postupovat s velkou opatrností, kdykoli je použit.
- Cyklofosfamid lze dialyzovat. Proto je v případě předávkování nebo náhodné intoxikace nebo za účelem sebevraždy indikována rychlá hemodialýza. Dialyzační clearance 78 ml / min byla vypočtena z koncentrace nemetabolizovaného cyklofosfamidu v dialyzátu (normální renální clearance je přibližně 5-11 ml / min). Druhá pracovní skupina hlásila hodnotu 194 ml / min. Po 6 hodinách dialýzy bylo v dialyzátu nalezeno 72% podané dávky cyklofosfamidu.
- Předávkování může mimo jiné způsobit myelosupresi, převážně leukocytopenii. Závažnost a trvání myelosuprese závisí na rozsahu předávkování.Jsou nutné časté kontroly krevního obrazu a sledování pacienta.V případě neutropenie zabraňte infekci a léčte antibiotiky. Pokud dojde k rozvoji trombocytopenie, zajistěte výměnu trombocytů podle potřeby.
- Je nezbytné, aby se profylaxe cystitidy prováděla s Uromitexanem (mesna), protože může pomoci zabránit nebo omezit urotoxické účinky předávkování cyklofosfamidem.
V případě náhodného požití / předávkování přípravkem ENDOXAN BAXTER okamžitě informujte svého lékaře nebo jděte do nejbližší nemocnice.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Endoxan Baxter
Podobně jako všechny léky, může mít i ENDOXAN BAXTER nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Nežádoucí účinky z klinických studií
Seznam nežádoucích účinků souvisejících s cyklofosfamidem je založen na postmarketingových údajích (viz níže).
Postmarketingové nežádoucí účinky
Frekvence je založena na následující stupnici: velmi časté (≥ 1/10); časté (≥1 / 100-
* včetně smrtelných následků
1 Následující projevy byly spojeny s myelosupresí a imunosupresí způsobenou cyklofosfamidem: zvýšené riziko a závažnost pneumonie (včetně fatálních následků), další bakteriální, plísňové, virové, protozoální a parazitické infekce; reaktivace latentních infekcí, včetně virové hepatitidy, tuberkulózy, viru JC s progresivní multifokální leukoencefalopatií (včetně fatálních následků), Pneumocystis jiroveci, herpes zoster, Strongyloides.
2 Akutní myeloidní leukémie, Akutní promyelocytová leukémie
3 Non-Hodgkinův lymfom
4 Myelosuprese se projevuje selháním kostní dřeně
5 komplikované krvácením
6 s trombotickou mikroangiopatií
7 Další srdeční patologie jsou: městnavé srdeční selhání, dysfunkce levé komory, myokarditida, karditida. Perikardiální výpotek může přejít do srdeční tamponády.
8 Jiné vaskulární patologie: zrudnutí
9 Další onemocnění ledvin: hemolyticko -uremický syndrom (HUS)
Dodržování pokynů obsažených v příbalové informaci snižuje riziko nežádoucích účinků.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Expirace a retence
Expirace: viz datum spotřeby vytištěné na obalu.
Datum exspirace se vztahuje na produkt v neporušeném obalu, správně skladovaný. UPOZORNĚNÍ: přípravek nepoužívejte po uplynutí doby použitelnosti uvedené na obalu.
Uchovávejte lék při teplotě nepřesahující + 25 ° C.
Lahve nesmějí být skladovány při teplotě vyšší, než je uvedeno, protože v tomto případě by mohlo dojít k degradaci účinné látky identifikovatelné nažloutlým zbarvením obsahu lahve, které může nabýt vzhled roztavené látky.
Váš lékař nebo zdravotnický pracovník by neměl používat lahve, jejichž obsah má vzhled popsaný výše.
Léčivé přípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
UCHOVÁVEJTE LÉČIVÝ MIMO DOSAH A DOHLED DĚTÍ
SLOŽENÍ
Endoxan Baxter 50 mg potahované tablety
Jedna potahovaná tableta obsahuje:
Účinná látka: Cyklofosfamid monohydrát 53,5 mg odpovídá bezvodému Cyklofosfamid 50 mg;
Pomocné látky: 85% glycerol, želatina, stearát hořečnatý, mastek, hydrogenfosforečnan vápenatý, laktóza, kukuřičný škrob;
Další složky (povlak): Ethylenglykolester kyseliny montanové, Polysorbát 20, Sodná sůl karmelózy, Povidon, Koloidní oxid křemičitý, Makrogol 35000, Uhličitan vápenatý, Mastek, Sacharóza, Oxid titaničitý.
Endoxan Baxter 200 mg prášek pro injekční roztok
Jedna skleněná láhev typu III obsahuje:
Účinná látka: cyklofosfamid monohydrát 213,8 mg odpovídá bezvodému cyklofosfamid 200 mg;
Pomocná látka: žádná.
Endoxan Baxter 500 mg prášek pro injekční roztok
Jedna skleněná láhev typu III obsahuje:
Účinná látka: Cyklofosfamid monohydrát 534,5 mg odpovídá bezvodému Cyklofosfamid 500 mg;
Pomocná látka: žádná.
Endoxan Baxter 1 g prášek pro injekční roztok
Jedna skleněná láhev typu III obsahuje:
Účinná látka: monohydrát cyklofosfamidu 1,069 g, což odpovídá bezvodému cyklofosfamidu 1 g; Pomocná látka: žádná.
LÉKOVÁ FORMA A OBSAH
Potahované tablety a prášek pro injekční roztok.
Endoxan Baxter 50 mg potahované tablety: 50 tablet uzavřených v 5 blistrech po 10 tabletách
Endoxan Baxter 200 mg Prášek pro injekční roztok: 10 skleněných lahviček typu III
Endoxan Baxter 500 mg prášek pro injekční roztok: 1 skleněná lahvička typu III
Endoxan Baxter 1 g prášek pro injekční roztok: 1 skleněná lahvička typu III
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
ENDOXAN BAXTER
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Endoxan Baxter 50 mg potahované tablety
Jedna potahovaná tableta obsahuje:
Účinná látka: Cyklofosfamid monohydrát 53,5 mg, což odpovídá bezvodému cyklofosfamidu 50 mg.
Pomocné látky: laktóza, sacharóza
Endoxan Baxter 200 mg prášek pro injekční roztok
Jedna skleněná láhev typu III obsahuje:
Účinná látka: Cyklofosfamid monohydrát 213,8 mg, což odpovídá 200 mg bezvodého cyklofosfamidu.
Endoxan Baxter 500 mg prášek pro injekční roztok
Jedna skleněná láhev typu III obsahuje:
Účinná látka: Cyklofosfamid monohydrát 534,5 mg, což odpovídá 500 mg bezvodého cyklofosfamidu.
Endoxan Baxter 1 g prášek pro injekční roztok
Jedna skleněná láhev typu III obsahuje:
Účinná látka: Cyklofosfamid monohydrát 1,069 g, což odpovídá 1 g bezvodého cyklofosfamidu.
Úplný seznam pomocných látek viz bod 6.1
03.0 LÉKOVÁ FORMA
Prášek pro injekční roztok.
Potahovaná tableta.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Cytostatická léčba.
04.2 Dávkování a způsob podání
• Endoxan Baxter by měl podávat pouze lékařský personál se zkušenostmi s onkologií.
• Léčba obvykle začíná intravenózními injekcemi. Pokud to není možné, lze přípravek Endoxan Baxter aplikovat intramuskulárně. Ve zvláštních případech je možná intrapleurální, intraperitoneální nebo in situ aplikace.Pro prodlouženou léčbu nebo terapii udržovací dávkou se po regresi symptomů doporučuje orální podání.
• Aktivace cyklofosfamidu vyžaduje jaterní metabolismus, proto by se podávání mělo přednostně provádět orálně nebo intravenózně.
Parenterální použití
• Léčivé přípravky používané parenterálně by měly být před podáním vizuálně zkontrolovány na přítomnost částic a změnu barvy roztoku, pokud to roztok a obal dovolí.
• Intravenózní podání by mělo být přednostně podáváno jako infuze.
Aby se snížila pravděpodobnost nežádoucích účinků, které se zdají souviset s rychlostí podávání (např. Otok obličeje, bolest hlavy, ucpaný nos, zánět pokožky hlavy), měl by být léčivý přípravek injekčně nebo infuzí podáván velmi pomalu. Trvání infuze by navíc mělo být přiměřené objemu a typu transportního roztoku, který má být podán.
• Pokud je injekce podána přímo, musí být roztok Endoxan Baxter rekonstituován fyziologickým roztokem (0,9% chlorid sodný). Při přípravě injekčního roztoku postupujte podle pokynů uvedených v bodě 6.6
• Před parenterálním podáním musí být léčivý přípravek zcela rozpuštěn.
Dávkování by mělo být přizpůsobeno potřebám každého jednotlivého pacienta, s přihlédnutím k obecným reakcím a krevnímu obrazu.
Pokud není předepsáno jinak, doporučují se následující dávky.
Pro léčbu lze zvážit následující:
a) kontinuální léčba: 3-6 mg / kg tělesné hmotnosti (ekvivalent 120 - 240 mg / m2 tělesného povrchu) i.v.
b) terapie v intervalech 2-5 dnů: 10-15 mg / kg tělesné hmotnosti (odpovídá 400-600 mg / m2 tělesného povrchu) i.v.
c) 10-20denní intervalová terapie: 20 až 40 mg / kg tělesné hmotnosti (ekvivalent 800 - 1600 mg / m2 tělesného povrchu) i.v.
Trvání terapie a intervaly mezi jedním a druhým podáním budou záviset na indikacích, na onkologických lécích, které mohou být spojeny s cyklofosfamidem, na celkovém stavu pacienta, na laboratorních parametrech, zejména na krevním obrazu.
Pro udržovací terapii se podává 50-200 mg denně (1-4 potahované tablety), v případě potřeby lze podat vyšší dávky.
Ke snížení rizika toxicity močových cest by mělo být požito nebo infuzováno dostatečné množství tekutin ke stimulaci diurézy, aby se snížilo riziko toxicity močových cest, a proto by měl být léčivý přípravek přednostně užíván ráno. (viz bod 4.4). Je důležité zajistit, aby pacient v pravidelných intervalech vyprazdňoval močový měchýř. Výše uvedené dávkování se týká hlavně léčby, při níž se účinná látka cyklofosfamid používá jako monoterapie.
Pokud je přípravek Endoxan Baxter kombinován s jinými cytostatiky podobné toxicity, může být nutné buď snížení dávky, nebo prodloužení intervalu.
Lze očekávat, že použití činidel stimulujících krvetvorbu (faktory stimulující kolonie a činidla stimulující erytropoézu) sníží riziko myelosupresivních komplikací a / nebo pomůže usnadnit plánované dávkování.
Doporučení pro snížení dávky u pacientů s myelosupresí
Doporučení pro úpravu dávkování u pacientů s jaterní nebo renální insuficiencí
• Těžká jaterní nebo renální insuficience vyžaduje snížení dávky.
• Závažná jaterní insuficience může být spojena se sníženou aktivací cyklofosfamidu. To může změnit účinnost terapie cyklofosfamidem a mělo by se to vzít v úvahu při určování dávky a interpretaci odpovědi na zvolenou dávku.
• U pacientů s renální insuficiencí, zvláště pokud je závažná, může snížená renální eliminace vést ke zvýšení plazmatických hladin cyklofosfamidu a jeho metabolitů. To může vést ke zvýšené toxicitě a mělo by se to vzít v úvahu při určování dávkování pro tento typ pacienta.
• Pro hodnoty bilirubinu v séru mezi 3,1 a 5 mg / 100 ml se doporučuje snížení o 25% a pro glomerulární filtraci nižší než 10 ml / minutu 50% snížení.
• Cyklofosfamid a jeho metabolity jsou dialyzovatelné, i když mohou existovat rozdíly v clearance podle typu použité dialyzační techniky. U pacientů vyžadujících dialýzu by měl být mezi podáním cyklofosfamidu a dialýzou zachován významný interval.
Senioři
U starších osob by sledování toxicity a nutnost úpravy dávkování mělo odrážet vyšší frekvenci jaterních, renálních, srdečních nebo jiných orgánových abnormalit a souběžnou přítomnost jiných onemocnění nebo terapii jinými léčivými přípravky.
04.3 Kontraindikace
Endoxan Baxter by neměl být podáván pacientům s:
- přecitlivělost na léčivou látku, její metabolity nebo na kteroukoli pomocnou látku
- těžce narušená funkce kostní dřeně (zejména u pacientů, kteří podstoupili předběžnou léčbu cytotoxickými látkami a / nebo radioterapii),
- zánět močového měchýře (cystitida),
- obstrukce toku moči,
- probíhající infekce,
- během těhotenství a kojení (viz 4.6).
04.4 Zvláštní upozornění a vhodná opatření pro použití
Rizikové faktory toxicity cyklofosfamidu a jejich důsledky popsané v tomto a dalších oddílech mohou představovat kontraindikace, pokud léčivý přípravek není používán k léčbě život ohrožujících stavů. V těchto situacích je nutné individuální posouzení poměru očekávaného přínosu / rizika.
UPOZORNĚNÍ
Toxicita ledvin a močových cest
• Během léčby cyklofosfamidem byla hlášena hemoragická cystitida, pyelitida, uretritida a hematurie. Může se také vyvinout ulcerace / nekróza močového měchýře, fibróza / kontraktura a sekundární nádory.
• Urotoxicita může vyžadovat přerušení léčby.
• U fibrózy, krvácení nebo sekundárních nádorů může být nutná cystektomie.
• Byly hlášeny případy urotoxicity s fatálními následky.
• Urotoxicita se může objevit při krátkodobé i dlouhodobé léčbě cyklofosfamidem. Po jednorázové dávce cyklofosfamidu byla hlášena hemoragická cystitida.
• Následná nebo souběžná radioterapie nebo léčba busulfanem může zvýšit riziko hemoragické cystitidy vyvolané cyklofosfamidem.
• Obecně je cystitida zpočátku sterilní, ale může dojít k sekundární mikrobiální kolonizaci.
• Různé obstrukce močových cest, cystitida a infekce musí být odstraněny nebo napraveny před zahájením terapie.
• Adekvátní terapie Uromitexanem (INN: mesna) nebo silná hydratace mohou výrazně snížit frekvenci a závažnost toxicity močového měchýře. Zajistěte, aby pacienti pravidelně vyprazdňovali močový měchýř.
• Pokud se během léčby přípravkem Endoxan Baxter objeví cystitida spojená s mikro nebo makrohematurií, přerušte léčbu přípravkem Endoxan Baxter až do normalizace.
K tomu obvykle dochází několik dní po vysazení léku, ale cystitida může také přetrvávat.
• V případě závažné hemoragické cystitidy by léčba přípravkem Endoxan Baxter měla být obecně ukončena.
• Cyklofosfamid byl také spojován s nefrotoxicitou včetně tubulární nekrózy.
• V souvislosti s podáváním cyklofosfamidu byla hlášena hyponatrémie spojená se zvýšenou celkovou tělesnou vodou, akutní intoxikací vodou a syndromem podobným SIADH (syndrom nedostatečné sekrece antidiuretického hormonu). Byly také hlášeny fatální následky.
• Pacienti s poruchou funkce ledvin by měli být během léčby přípravkem Endoxan Baxter pečlivě sledováni na přítomnost erytrocytů a další známky uro / nefrotoxicity (viz také „Doporučení pro úpravu dávkování u pacientů s jaterní nebo renální insuficiencí“ bod 4.2 „Dávkování a způsob podání“).
Myelosuprese, Imunosuprese, Infekce
Obecně by měl být přípravek Endoxan Baxter, stejně jako všechna ostatní cytostatika, používán s maximální péčí u slabých nebo starších subjektů au subjektů, které již dříve podstoupily radioterapii.
Jedinci s oslabeným imunitním systémem, jako jsou pacienti s diabetes mellitus, chronickým onemocněním jater nebo ledvin, by měli být také pečlivě sledováni.
• Léčba cyklofosfamidem může způsobit myelosupresi a významné potlačení imunitní odpovědi.
• Očekává se těžká myelosuprese, zejména u pacientů, kteří již dříve podstoupili chemoterapii a / nebo radioterapii nebo u pacientů s poruchou funkce ledvin.
• Cyklofosfamidem indukovaná myelosuprese může způsobit leukopenii, neutropenii, trombocytopenii (spojenou s vyšším rizikem krvácení) a anémii.
• Silná imunosuprese vedla k závažným, někdy smrtelným infekcím. Byly také hlášeny sepse a septický šok. Mezi infekce hlášené cyklofosfamidem patří jak zápal plic, tak další infekce bakteriálního, plísňového, virového, protozoálního a parazitického původu.
• Latentní infekce lze znovu aktivovat. Reaktivace byla hlášena u různých infekcí bakteriálního, houbového, virového, protozoálního a parazitárního původu.
• S infekcemi musí být zacházeno odpovídajícím způsobem.
• Podle uvážení ošetřujícího lékaře může být v některých případech neutropenie indikována antimikrobiální profylaxe.
• V případě neutropenické horečky a / nebo leukopenie by měla být jako profylaxe podávána antibiotika a / nebo antimykotika.
• V případě potřeby by měl být cyklofosfamid používán s opatrností u pacientů s těžkým poškozením funkce kostní dřeně a u pacientů s těžkou imunosupresí.
• Léčba cyklofosfamidem nemusí být indikována nebo by měla být ukončena nebo by mělo být sníženo dávkování u pacientů, kteří mají nebo se u nich vyvine závažná infekce.
• Teoreticky je pokles počtu buněk periferních krvinek a krevních destiček a doba potřebná k zotavení tím vyšší, čím vyšší je dávka.
• Nejnižší počet leukocytů a krevních destiček se obvykle vyskytuje jeden až dva týdny po zahájení léčby. Kostní dřeň se obnovuje poměrně rychle a hodnoty krve se normálně normalizují asi po 20 dnech.
• Proto je vhodné, aby během léčby všichni pacienti podstoupili pečlivou hematologickou kontrolu s pravidelně prováděným krevním obrazem.
- Počty bílých krvinek a krevních destiček a hodnoty hemoglobinu by měly být kontrolovány před každým podáním a ve vhodných intervalech, v případě potřeby každý den.
- Kontroly leukocytů by měly být prováděny pravidelně během léčby, v intervalech 5-7 dní na začátku léčby a každé 2 dny, pokud počet klesne pod 3000 / mm3 (viz také bod 4.2 „Dávkování a způsob podání“).
• Pokud to není nezbytně nutné, Endoxan Baxter by neměl být podáván pacientům s počtem bílých krvinek nižším než 2 500 / mcl a / nebo počtem krevních destiček pod 50 000 / mcl.
• Rovněž se doporučuje pravidelné sledování sedimentu moči na přítomnost erytrocytů.
Kardiotoxicita, použití u pacientů s onemocněním srdce
• Během léčby cyklofosfamidem byla hlášena myokarditida a myopikarditida, které mohou být doprovázeny výrazným perikardiálním výpotkem a srdeční tamponádou a vedly k závažnému, někdy smrtelnému městnavému srdečnímu selhání.
• Histopatologické vyšetření prokázalo hlavně hemoragickou myokarditidu. Jako sekundární účinek hemoragické myokarditidy a nekrózy myokardu došlo k hemoperikardu.
• Při jednorázové dávce cyklofosfamidu nižší než 20 mg / kg byla pozorována akutní srdeční toxicita.
• Po expozici léčebným režimům zahrnujícím cyklofosfamid, byly u pacientů s jinými příznaky kardiotoxicity nebo bez nich hlášeny supraventrikulární arytmie (včetně fibrilace síní a flutteru) a ventrikulární arytmie (včetně závažných prodloužení QT spojených s komorovou tachyarytmií).
• Bylo prokázáno, že použití vysokých dávek cyklofosfamidu u pacientů v pokročilém věku a u pacientů, kteří měli předchozí radioterapii v oblasti srdce a / nebo souběžnou léčbu antracykliny a pentostatinem nebo jinými kardiotoxickými látkami (viz bod 4.5) může zesílit kardiotoxický účinek přípravku Endoxan Baxter. V této souvislosti bude nutné pravidelně kontrolovat elektrolyty a věnovat zvláštní pozornost pacientům s „anamnézou srdečních chorob“.
Plicní toxicita
• Pneumonie a plicní fibróza byly hlášeny v souvislosti s léčbou cyklofosfamidem nebo po ní. Byly také hlášeny plicní venookluzivní choroby a jiné formy plicní toxicity. Byla hlášena plicní toxicita vedoucí k respiračnímu selhání.
• I když je výskyt plicní toxicity spojený s cyklofosfamidem nízký, prognóza pro postižené pacienty je špatná.
• Pozdní nástup pneumonie (více než 6 měsíců po zahájení léčby cyklofosfamidem) se zdá být spojen se zvláště vysokou úmrtností. Pneumonie může také vzniknout roky po léčbě cyklofosfamidem.
• Akutní plicní toxicita byla hlášena po jedné dávce cyklofosfamidu.
Sekundární nádory
• Stejně jako u cytostatické terapie obecně, léčba cyklofosfamidem také nese riziko sekundárních rakovin a jejich prekurzorů jako pozdních následků.
• Zvyšuje riziko vzniku karcinomu močových cest a myelodysplastických změn, které částečně procházejí do akutní leukémie. Mezi další rakoviny hlášené po léčbě cyklofosfamidem nebo cyklofosfamidem patří lymfom, rakovina štítné žlázy a sarkomy.
• V některých případech se sekundární rakovina vyvinula několik let po ukončení léčby cyklofosfamidem. Nádory byly také hlášeny po expozici in utero.
• Riziko rakoviny močového měchýře lze významně snížit prevencí hemoragické cystitidy.
Venookluzivní patologie jater
• Venookluzivní onemocnění jater (VOLD) bylo hlášeno u pacientů užívajících cyklofosfamid.
• Jako hlavní rizikový faktor pro rozvoj VOLD byla identifikována cytoredukční léčba v rámci přípravy na transplantaci kostní dřeně, která se skládá z cyklofosfamidu v kombinaci s integrálním ozařováním, busulfanem nebo jinými činidly (viz bod 4.5). Po cytoredukční terapii se klinický syndrom klinicky vyvíjí 1 až 2 týdny po transplantaci a je charakterizován rychlým přírůstkem hmotnosti, bolestivou hepatomegalií, ascitem a hyperbilirubinémií / žloutenkou.
• Postupný vývoj VOLD byl však hlášen u pacientů dlouhodobě léčených nízkými dávkami imunosupresivních dávek cyklofosfamidu.
• Jako komplikace VOLD se může vyvinout hepatorenální syndrom a multiorgánové selhání. U VOLD spojeného s cyklofosfamidem byl hlášen smrtelný výsledek.
• Mezi rizikové faktory, které předurčují pacienta k rozvoji VOLD pomocí vysokodávkových cytoredukčních terapií, patří:
- již existující poruchy funkce jater
- radiační terapie břicha e
- nízké skóre výkonu
Genotoxicita
• Endoxan Baxter je genotoxický a mutagenní v samčích i samičích somatických a zárodečných buňkách. Ženy by se proto měly během užívání přípravku Endoxan Baxter vyvarovat otěhotnění a muži by měli zabránit početí dětí.
• Muži by se měli vyhnout početí dětí po dobu až 6 měsíců po ukončení léčby.
• Studie na zvířatech naznačují, že expozice oocytů během vývoje folikulů může mít za následek nižší míru implantace a nerizikového těhotenství a větší riziko malformací. Tento účinek je třeba vzít v úvahu v případě oplodnění nebo dobrovolného těhotenství po ukončení léčby cyklofosfamidem. přesné trvání vývoje folikulů u lidí není známo, ale může být delší než 12 měsíců.
• Sexuálně aktivní muži a ženy by v tomto období měli používat účinné metody antikoncepce.
Viz také část 4.6.
Účinek na plodnost
• Cyklofosfamid zasahuje do oogeneze a spermatogeneze a může způsobit neplodnost u obou pohlaví.
• Zdá se, že vývoj neplodnosti závisí na dávce cyklofosfamidu, délce léčby a stavu gonadálních funkcí v době léčby.
• Sterilita vyvolaná cyklofosfamidem může být u některých pacientů nevratná.
Pacientky
• Přechodná nebo trvalá amenorea, spojená se sníženou sekrecí estrogenu a zvýšenou sekrecí gonadotropinů, se vyvíjí u významného podílu žen léčených cyklofosfamidem.
• Zvláště u starších žen může být amenorea trvalá.
• Oligomenorea byla také hlášena v souvislosti s léčbou cyklofosfamidem.
• Dívky léčené cyklofosfamidem v prepubescenci obecně vyvíjejí sekundární sexuální charakteristiky normálně a mají pravidelné cykly.
• Dívky ošetřené cyklofosfamidem v prepubescenci následně počaly děti.
• Dívky léčené cyklofosfamidem, které si po ukončení léčby zachovaly ovariální funkce, mají vyšší riziko vzniku předčasné menopauzy (přerušení cyklu před 40. rokem věku).
Mužští pacienti
• U mužů léčených cyklofosfamidem se může vyvinout oligospermie nebo azoospermie, které jsou normálně spojeny se zvýšenou sekrecí gonadotropinu, ale s normální sekrecí testosteronu.
• Sexuální síla a libido u těchto pacientů obecně nejsou narušeny.
• U chlapců léčených cyklofosfamidem v prepubescenci se mohou normálně vyvinout sekundární sexuální charakteristiky, ale mohou mít oligospermii nebo azoospermii.
• Atrofie varlat se může vyskytovat v různé míře.
• Azoospermie vyvolaná cyklofosfamidem je u některých pacientů reverzibilní, i když k reverzibilitě nemusí dojít několik let po ukončení léčby.
• Muži dočasně sterilní cyklofosfamidem následně počali děti.
• Protože léčba přípravkem Endoxan Baxter může zvýšit riziko trvalé neplodnosti u mužů, měli by být muži před léčbou informováni o skladování spermií.
Anafylaktické reakce, zkřížená citlivost s jinými alkylačními činidly
• V souvislosti s cyklofosfamidem byly hlášeny anafylaktické reakce včetně reakcí s fatálními následky.
• Byla hlášena možná zkřížená citlivost s jinými alkylačními činidly.
Změna procesu hojení ran
• Cyklofosfamid může narušovat normální proces hojení ran.
Alopecie
• Byla hlášena alopecie, která se může vyskytovat častěji se zvyšujícím se dávkováním.
• Alopecie může přejít do plešatosti.
• Vlasy by měly po léčbě tímto lékem nebo dokonce během léčby znovu narůst, přestože se mohou lišit strukturou a barvou.
Nevolnost a zvracení
• Podávání cyklofosfamidu může způsobit nevolnost a zvracení.
• Je třeba vzít v úvahu aktuální pokyny k používání antiemetik k prevenci a zlepšení nevolnosti a zvracení.
• Alkohol může zvýšit emetické účinky a nevolnost způsobenou cyklofosfamidem; z těchto důvodů je třeba se vyvarovat konzumace alkoholu u pacientů léčených cyklofosfamidem.
Stomatitida
• Podávání cyklofosfamidu může způsobit stomatitidu (orální mukozitidu)
• Je třeba vzít v úvahu aktuální pokyny pro prevenci a zlepšení stomatitidy.
• Zvláštní pozornost věnujte ústní hygieně, abyste snížili výskyt stomatitidy.
Diagnostické vyšetřování
U diabetických pacientů by měla být pravidelně kontrolována hladina cukru v krvi, aby bylo možné rychle přizpůsobit antidiabetickou terapii (viz také bod 4.5 "Interakce s jinými léčivými přípravky a jiné formy" interakce ")
BEZPEČNOSTNÍ OPATŘENÍ PRO POUŽITÍ
Paravenózní podání
• Protože k cytostatickému účinku Endoxanu Baxter dochází po jeho aktivaci, která probíhá hlavně v játrech, existuje jen minimální riziko poškození tkáně v případě náhodného paravenózního podání.
Poznámka:
V případě náhodného podání paravenózní injekcí okamžitě zastavte infuzi, odsajte kapalinu přenesenou aplikovanou kanylou a proveďte další vhodná opatření, např. Oblast zavlažte fyziologickým roztokem a znehybněte končetinu.
Použití u pacientů s renální insuficiencí
U pacientů s renální insuficiencí, zvláště pokud je závažná, může snížená renální eliminace vést ke zvýšení plazmatických hladin cyklofosfamidu a jeho metabolitů. To může vést ke zvýšené toxicitě a mělo by se to vzít v úvahu při určování dávkování pro tento typ pacienta. Viz také část 4.2.
Použití u pacientů s jaterní insuficiencí
Těžká jaterní insuficience může být spojena se sníženou aktivací cyklofosfamidu. To může změnit účinnost terapie cyklofosfamidem a mělo by se to vzít v úvahu při určování dávky a interpretaci odpovědi na zvolenou dávku. Zneužívání alkoholu může zvýšit riziko vzniku dysfunkce jater.
Použití u pacientů s adrenalektomií
Pacienti s adrenální insuficiencí mohou vyžadovat zvýšené náhradní dávky kortikoidů, pokud jsou vystaveni stresu vyplývajícímu z toxicity cytostatik, včetně cyklofosfamidu.
Tablety obsahují laktózu, takže nejsou vhodné pro osoby s nedostatkem laktázy, galaktosémií nebo syndromem malabsorpce glukózy / galaktózy; obsahují také sacharózu, takže nejsou vhodné pro osoby s dědičnou intolerancí fruktózy, syndromem malabsorpce glukózy / galaktózy nebo nedostatkem sacharázy-izomaltázy.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Souběžné nebo následné plánované podávání jiných látek nebo léčebných postupů, které by mohly zvýšit pravděpodobnost nebo závažnost toxických účinků (prostřednictvím farmakodynamických nebo farmakokinetických interakcí), vyžaduje pečlivé individuální zvážení očekávaných přínosů a rizik. Pacienti, kteří dostávají takové kombinace, by měli být pečlivě sledováni s ohledem na příznaky toxicity, a proto by měli umožnit rychlou intervenci. U pacientů léčených cyklofosfamidem a látkami snižujícími jeho aktivaci by mělo být sledováno potenciální snížení terapeutické účinnosti a nutnost úpravy dávkování.
Interakce ovlivňující farmakokinetiku cyklofosfamidu a jeho metabolitů
• Hypoglykemický účinek sulfonylmočovin může být zesílen, stejně jako myelosupresivní účinek, pokud je alopurinol nebo hydrochlorothiazid podáván současně.
• Snížená aktivace cyklofosfamidu může změnit účinnost léčby cyklofosfamidem. Mezi látky, které zpomalují aktivaci cyklofosfamidu, patří:
- Apripitant
- Bupropion
- Busulfan: Podávání vysokých dávek přípravku Endoxan Baxter do 24 hodin po léčbě vysokými dávkami busulfanu může způsobit snížení clearance a „prodloužení eliminačního poločasu“ cyklofosfamidu.
- Ciprofloxacin: Podávání antibiotik na bázi fluorochinolonů (jako je ciprofloxacin) před zahájením léčby přípravkem Endoxan Baxter (zejména v případě kondicionování před transplantací kostní dřeně) může snížit účinnost přípravku Endoxan Baxter, a proto vést ke zhoršení primární patologie.
- Chloramfenikol: Současné podávání chloramfenikolu vede k prodloužení cyklofosfamidu na polovinu a ke zpomalení metabolismu.
- Flukonazol, itrakonazol: Je známo, že azolová antimykotika (flukonazol, itrakonazol) inhibují aktivitu cyklofosfamidu metabolizující cytochrom P450. U pacientů léčených itrakonazolem byla pozorována zvýšená expozice toxickým metabolitům Endoxanu Baxter.
- Prasugrel
- Sulfonamidy
- Thiotepa: Silná inhibice bioaktivace cyklofosfamidu thiotepou byla pozorována u režimů vysokých dávek chemoterapie, pokud byly podány jednu hodinu před Endoxan Baxter. Sekvence a načasování podávání těchto dvou látek mohou přispívat.
• Ke zvýšení koncentrace cytotoxických metabolitů může dojít při:
- Allopurinol
- Chloralhydrát
- Cimetidin
- Disulfiram
- Glyceraldehyd
- Induktory jaterních a extrahepatálních lidských mikrozomálních enzymů (např. Enzymy cytochromu P450): Potenciální indukce jaterních a extrahepatálních mikrozomálních enzymů by měla být vzata v úvahu v případě předchozí nebo souběžné léčby látkami, o nichž je známo, že indukují zvýšení „aktivity takové enzymy jako rifampicin, fenobarbital, karbamazepin, benzodiazepiny, fentoin, třezalka a kortikosteroidy.
- Inhibitory proteázy: Souběžné použití inhibitorů proteázy může zvýšit koncentraci cytotoxických metabolitů.U pacientů, kterým byl podáván cyklofosfamid, doxorubicin a etoposid (CDE), bylo prokázáno, že použití léčby inhibitorem proteázy je spojeno s vyšším výskytem infekcí a neutropenie než při použití léčby založené na NNRTI.
- Ondansetron: Mezi ondansetronem a Endoxan Baxter (při vysokých dávkách) byly zjištěny farmakokinetické interakce, které vedly ke snížení AUC (plocha pod křivkou) cyklofosfamidu.
• Protože grapefruit obsahuje sloučeninu, která může inhibovat aktivaci cyklofosfamidu a následně jeho účinnost, pacient by neměl konzumovat grapefruit nebo grapefruitovou šťávu.
Farmakodynamické interakce a interakce s neznámými mechanismy ovlivňujícími použití cyklofosfamidu
Kombinace nebo následné použití cyklofosfamidu a dalších látek s podobnou toxicitou může způsobit kombinované (velké) toxické účinky.
• Zvýšení hematotoxicity a / nebo imunosuprese může být důsledkem kombinace účinků cyklofosfamidu a například:
- Inhibitory ACE: Inhibitory ACE mohou způsobit leukopenii.
- Natalizumab
- Paclitaxel: Při podání cyklofosfamidu po infuzi paklitaxelu bylo hlášeno zvýšení hematotoxicity.
- Diuretika na bázi thiazidů
- Zidovudin
• Zvýšená kardiotoxicita může být důsledkem kombinace účinků cyklofosfamidu a například:
- Antracykliny
- Pentostatiny
- Cytarabin - Podávání vysokých dávek přípravku Endoxan Baxter a cytarabinu ve stejný den, tedy ve velmi omezeném časovém intervalu, může vést ke zvýšení kardiotoxického účinku s ohledem na to, že každá látka je již sama o sobě kardiotoxická.
- Radioterapie do oblasti srdce.
- Trastuzumab
• Zvýšení plicní toxicity může být důsledkem kombinace účinků cyklofosfamidu a například:
- Amiodaron
-G-CSF nebo GM-CSF (faktor stimulující kolonie granulocytových makrofágů a faktor stimulující kolonie granulocytů): Zprávy naznačují zvýšené riziko plicní toxicity (pneumonie, alveolární fibróza) u pacientů léčených cytotoxickou chemoterapií, která zahrnuje Endoxan Baxter a GCSF
- GM-CSF.
• Zvýšení nefrotoxicity může být důsledkem kombinace účinků cyklofosfamidu a například:
- Amfotericin B
- Indomethacin: Souběžné podávání indomethacinu by mělo být prováděno s maximální péčí, protože byla hlášena akutní intoxikace vodou.
• Zvýšení dalších toxicit:
- Azathioprin: zvýšené riziko hepatotoxicity (nekróza jater)
- Busulfan: Byl hlášen vyšší výskyt venookluzivních patologií a mukozitidy.
- Inhibitory proteázy: zvýšený výskyt mukozitidy.
Další interakce:
• Alkohol: Snížená protinádorová aktivita byla pozorována u zvířat s rakovinou, když byl souběžně s nízkými perorálními dávkami cyklofosfamidu podáván ethanol (alkohol). U některých pacientů může alkohol zvýšit emetické účinky a nevolnost způsobenou cyklofosfamidem.
• Etanercept: U pacientů s Wegenerovou granulomatózou bylo přidání etanerceptu ke standardní léčbě cyklofosfamidem spojeno s vyšším výskytem nekožních solidních nádorů.
• Metronidazol: Akutní encefalopatie byla pozorována u pacienta léčeného cyklofosfamidem a metronidazolem. Příčinná souvislost není jasná.Ve studii na zvířatech byla kombinace cyklofosfamidu a metronidazolu spojena se zvýšenou toxicitou cyklofosfamidu.
• Tamoxifen: Souběžné užívání tamoxifenu a chemoterapie může zvýšit riziko tromboembolických komplikací.
Interakce ovlivňující farmakokinetiku a / nebo účinek jiných léčivých přípravků
• Bupropion: Metabolismus cyklofosfamidu prostřednictvím CYP2B6 může inhibovat metabolismus bupropionu.
• Kumariny: U pacientů léčených warfarinem a cyklofosfamidem byl hlášen zvýšený i snížený účinek warfarinu.
• Cyklosporiny: U pacientů léčených kombinací přípravku Endoxan Baxter a cyklosporinu byla zjištěna nižší sérová koncentrace cyklosporinu než u pacientů, kterým byl podáván samotný cyklosporin. Tato interakce by mohla vést ke zvýšenému výskytu reakcí na odmítnutí.
• Depolarizující myorelaxancia: Pokud se depolarizující myorelaxancia (např. Sukcinylcholinhalogenidy) aplikují současně, může dojít k prodloužené „apnoe způsobené“ významnou a trvalou inhibicí aktivity cholinesterázy. Pokud byl pacient léčen cyklofosfamidem do 10 dnů po „celkové anestezii, “měl by být poučen anesteziolog.
• Digoxin, β; -acetyldigoxin: Bylo hlášeno, že cytostatická léčba narušuje střevní absorpci tablet digoxinu a β; -acetyldigoxinu.
• Vakcíny: Vzhledem k tomu, že cyklofosfamid má imunosupresivní účinky, může pacient vykazovat sníženou odpověď na souběžné očkování; očkování aktivními vakcínami může být spojeno s infekcí vyvolanou vakcínou.
• Verapamil: Bylo hlášeno, že cytostatická léčba narušuje střevní absorpci perorálně podávaného verapamilu.
04.6 Těhotenství a kojení
• Měl by být zvážen možný průchod Endoxan Baxter přes mateřskou placentu. Léčba cyklofosfamidem může při podávání těhotným ženám způsobit abnormality genotypu.
• Pokud existují rizika pro život pacientky během prvního trimestru těhotenství, bude naprosto nezbytné poradit se s lékařem, aby bylo možné těhotenství přerušit.
• U dětí narozených matkám léčeným cyklofosfamidem během prvního trimestru těhotenství byly hlášeny malformace. Byly však také hlášeny děti bez malformací narozené ženám vystaveným během prvního trimestru.
• Pokud po prvním trimestru těhotenství nelze terapii odložit a pacientka si přeje v těhotenství pokračovat, lze po informování pacientky o menším, ale možném riziku teratogenních účinků, použít chemoterapii.
• Expozice cyklofosfamidu in utero může způsobit ukončení těhotenství, zpomalení růstu plodu a fetotoxické účinky vyskytující se u novorozenců, včetně leukopenie, anémie, pancytopenie, závažné hypoplazie kostní dřeně a grastroenteritidy.
• Během léčby přípravkem Endoxan Baxter a až 6 měsíců po ukončení léčby by se ženy měly vyvarovat otěhotnění a muži by se měli vyhýbat početí dětí.
• Výsledky studií na zvířatech naznačují, že zvýšené riziko přerušení těhotenství a malformací může přetrvávat i po vysazení cyklofosfamidu, pokud existují oocyty / folikuly, které byly vystaveny cyklofosfamidu v kterémkoli stádiu zrání. Odkaz na bod 4.4, Genotoxicita .
• Pokud se cyklofosfamid používá během těhotenství nebo pokud pacientka otěhotní během užívání tohoto léku nebo po ukončení léčby (viz bod 4.4, Genotoxicita), měla by být pacientka informována o možných rizicích pro plod.
• Protože cyklofosfamid přechází do mateřského mléka, matky během léčby nebudou muset kojit. U kojenců žen užívajících cyklofosfamid byla hlášena neutropenie, trombocytopenie, nízký hemoglobin a průjem.
• Muži, kteří budou léčeni přípravkem Endoxan Baxter, by měli být před léčbou informováni o skladování spermií.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Vzhledem k možnosti nežádoucích účinků vyplývajících z podávání cyklofosfamidu (např. Nevolnost, zvracení, závratě, rozmazané vidění a zhoršené vidění), které mohou zhoršit schopnost řídit nebo obsluhovat stroje, bude lékař muset rozhodnout individuálně. schopnost řídit vozidla nebo obsluhovat stroje.
04.8 Nežádoucí účinky
Nežádoucí účinky z klinických studií
Seznam nežádoucích účinků souvisejících s cyklofosfamidem je založen na postmarketingových údajích (viz níže).
Postmarketingové nežádoucí účinky
Frekvence je založena na následující stupnici: velmi časté (≥ 1/10); časté (≥1 / 100-
* včetně smrtelných následků
1 Následující projevy byly spojeny s myelosupresí a imunosupresí způsobenou cyklofosfamidem: zvýšené riziko a závažnost pneumonie (včetně fatálních následků), další bakteriální, plísňové, virové, protozoální a parazitické infekce; reaktivace latentních infekcí, včetně virové hepatitidy, tuberkulózy, viru JC s progresivní multifokální leukoencefalopatií (včetně fatálních následků), Pneumocystis jiroveci, pásový opar, Strongyloidy.
2 Akutní myeloidní leukémie, Akutní promyelocytová leukémie
3 Non-Hodgkinův lymfom
4 Myelosuprese se projevuje selháním kostní dřeně
5 komplikované krvácením
6 s trombotickou mikroangiopatií
7 Další srdeční patologie jsou: městnavé srdeční selhání, dysfunkce levé komory, myokarditida, karditida.
Perikardiální výpotek může přejít do srdeční tamponády.
8 Jiné vaskulární patologie: zrudnutí
9 Další onemocnění ledvin: hemolyticko -uremický syndrom (HUS)
04.9 Předávkování
• Vážné důsledky předávkování zahrnují projevy toxicity závislé na dávce, jako je myelosuprese, urotoxicita, kardiotoxicita (včetně srdečního selhání), venookluzivní onemocnění jater a stomatitida. Viz bod 4.4.
• Protože specifické antidotum pro cyklofosfamid není známo, doporučujeme při jeho použití postupovat velmi opatrně.
• Cyklofosfamid lze dialyzovat. Proto je rychlá hemodialýza indikována v případě předávkování nebo náhodné intoxikace nebo sebevraždy. Dialyzační clearance 78 ml / min byla vypočtena z koncentrace nemetabolizovaného cyklofosfamidu v dialyzátu (normální renální clearance je přibližně 5-11 ml / min). Druhá pracovní skupina hlásila hodnotu 194 ml / min. Po 6 hodinách dialýzy bylo v dialyzátu nalezeno 72% podané dávky cyklofosfamidu.
• Předávkování může mimo jiné způsobit myelosupresi, převážně leukocytopenii. Závažnost a trvání myelosuprese závisí na rozsahu předávkování.Jsou nutné časté kontroly krevního obrazu a sledování pacienta.V případě neutropenie zabraňte infekci a léčte antibiotiky. Pokud dojde k rozvoji trombocytopenie, zajistěte výměnu trombocytů podle potřeby.
• Profylaxe cystitidy přípravkem Uromitexan (mesna) může pomoci zabránit nebo omezit urotoxické účinky předávkování cyklofosfamidem.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Antineoplasty, analogy dusičnaté hořčice.
ATC kód: L01AA01.
Cyklofosfamid je cytostat oxazafosforinové skupiny a je chemicky navázán na N-methyl-bis (2-chlorethyl) amin.
Cyklofosfamid je inaktivován in vitro a aktivován in vivo jaterními mikrozomálními enzymy na 4-hydroxycyklofosfamid, který je v rovnováze s vlastním tautomerním aldofosfamidem.
Cytotoxický účinek cyklofosfamidu je založen na interakci mezi jeho alkylačními metabolity a DNA. Tato alkylace produkuje lámání a spojování řetězců DNA a tvorbu příčných vazeb proteinů DNA. V buněčném cyklu je průchod fází G2 opožděn. Cytotoxický účinek není specifický pro fázi buněčného cyklu, ale pro buněčný cyklus .
Křížovou rezistenci nelze vyloučit, zvláště u strukturálně podobných cytostatik, jako je ifosfamid a další alkylační činidla.
05.2 Farmakokinetické vlastnosti
Cyklofosfamid je téměř úplně absorbován z gastrointestinálního traktu.
U lidí po jedné intravenózní injekci značeného cyklofosfamidu do 24 hodin následuje výrazné snížení plazmatických koncentrací cyklofosfamidu a jeho metabolitů, přestože detekovatelné hladiny mohou v plazmě přetrvávat až 72 hodin. Cyklofosfamid je in vitro neaktivní a je bioaktivován. v organismu.
Průměrný poločas cyklofosfamidového séra je přibližně 7 hodin u dospělých a přibližně 4 hodiny u dětí. Cyklofosfamid a jeho metabolity jsou z velké části vylučovány ledvinami.
Krevní hladiny po intravenózních a orálních dávkách jsou bioekvivalentní.
05.3 Předklinické údaje vztahující se k bezpečnosti
Akutní toxicita
Ve srovnání s jinými cytostatiky je akutní toxicita cyklofosfamidu relativně nízká. To bylo prokázáno experimenty na myších, morčatech, králících a psech. Po jediné intravenózní injekci byl LD50 u potkanů přibližně 160 mg / kg, u myší a morčat 400 mg / kg, u králíků 130 mg / kg a u psů 40 mg / kg.
Chronická toxicita
Chronické podávání toxických dávek vedlo k poškození jater projevující se formou tukové degenerace následované nekrózou. Střevní sliznice nebyla ovlivněna. Hranice hepatotoxických účinků je 100 mg / kg u králíků a 10 mg / kg u psů. Při pokusech na zvířatech vykazoval cyklofosfamid a jeho aktivní metabolity mutagenní, karcinogenní a teratogenní účinky.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Prášek pro injekční roztok: žádný.
Potahované tablety: Glycerol 85%, želatina, stearan hořečnatý, mastek, hydrogenfosforečnan sodný, laktóza, kukuřičný škrob, makrogol 35 000, uhličitan vápenatý, koloidní oxid křemičitý, povidon, sodná sůl karamelosy, polysorbát 20, sacharóza, oxid titaničitý, ester ethylenglykolu „kyselina montanová.
06.2 Neslučitelnost
Roztoky obsahující benzylalkohol mohou snížit stabilitu cyklofosfamidu.
06.3 Doba platnosti
3 roky.
06.4 Zvláštní opatření pro skladování
Uchovávejte lék při teplotě nepřesahující + 25 ° C.
Roztok by měl být vstříknut co nejdříve po přípravě.
Doba použitelnosti roztoku: od 2 do 3 hodin.
Lahve nesmějí být skladovány při teplotě vyšší, než je uvedeno, protože v tomto případě by mohlo dojít k degradaci účinné látky identifikovatelné nažloutlým zbarvením obsahu lahve, které může nabýt vzhled roztavené látky.
Nepoužívejte lahve, jejichž obsah má vzhled popsaný výše.
06.5 Charakter vnitřního obalu a obsah balení
Bílé skleněné lahve typu III s butylovou gumovou zátkou a hliníkovým víčkem.
PVC / PVDC / hliníkové blistry.
Obal:
„200 mg prášek pro injekční roztok“ 10 200 mg injekčních lahviček ze skla typu III;
„500 mg prášek pro injekční roztok“ 1 skleněná láhev typu III 500 mg;
„1 g prášek pro injekční roztok“ 1 skleněná láhev typu III 1 g;
„50 mg potahované tablety“ 5 blistrů po 10 50 mg potahovaných tabletách.
Na trhu nemusí být všechna balení.
06.6 Návod k použití a zacházení
Manipulace a příprava cyklofosfamidu by měla být vždy prováděna v souladu s aktuálními pokyny pro bezpečné zacházení s cytotoxickými látkami.
Potahování tablet brání přímému kontaktu s účinnou látkou pro osoby, které s nimi manipulují. Aby se zabránilo neúmyslnému vystavení účinné látky třetím stranám, tablety by se neměly dělit ani drtit.
Příprava injekčního roztoku:
Endoxan Baxter pro intravenózní podání se připravuje ve skleněných lahvích typu III.
K přípravě injekčního roztoku musí být do suchého prášku přidáno následující množství fyziologického roztoku (0,9%chlorid sodný):
Před parenterálním podáním musí být látka zcela rozpuštěna. Látka se snadno rozpouští, pokud se lahve po přidání rozpouštědla (fyziologického roztoku) intenzivně protřepávají půl nebo jednu minutu.
Pokud se látka nerozpustí okamžitě bez zanechání zbytků, je vhodné nechat roztok několik minut odstát, dokud není čirý. Vstřikováním rozpouštědla do láhve vzniká přetlak, kterému lze zabránit zavedením druhé sterilní jehly do gumové zátky, aby vzduch z lahve unikal.
Cyklofosfamid rekonstituovaný ve vodě je hypotonický a neměl by být podáván přímo.
Pokud je cyklofosfamid podáván infuzí, může být rekonstituován přidáním sterilní vody a infuzován do doporučených intravenózních roztoků.
Tento léčivý přípravek je kompatibilní s následujícími infuzními roztoky: roztokem chloridu sodného, roztokem glukózy, roztokem chloridu sodného a glukózy, roztokem chloridu sodného a chloridu draselného, roztokem chloridu draselného a glukózy.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Baxter S.p.A. - Piazzale dell "Industria, 20 - 00144 Řím
08.0 REGISTRAČNÍ ČÍSLO
Endoxan Baxter
50 mg potahované tablety: AIC 015628011
200 mg Prášek pro injekční roztok 10 skleněných lahví typu III 200 mg: AIC 015628062
500 mg Prášek pro injekční roztok 1 skleněná lahvička typu III 500 mg: AIC 015628074
1 g Prášek pro injekční roztok 1 skleněná lahvička typu III 1 g: AIC 015628086
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
První AIC: září 1959.
Poslední obnovení ACI: říjen 2012
10.0 DATUM REVIZE TEXTU
Stanovení AIFA z října 2012