Účinné látky: flutikason (flutikason -propionát)
FLUSPIRAL 500 mcg / 2 ml suspenze k rozprašování - mlhoviny
Fluspirální příbalové letáky jsou k dispozici pro velikosti balení:- FLUSPIRAL 50 mcg Tlaková suspenze pro inhalaci
- Fluspiral 125 mcg Tlaková inhalační suspenze, Fluspiral 250 mcg Tlaková inhalační suspenze
- Fluspiral 100 mcg inhalační prášek, Fluspiral 250 mcg inhalační prášek, Fluspiral 500 mcg inhalační prášek,
- FLUSPIRAL 500 mcg / 2 ml suspenze k rozprašování - mlhoviny
Indikace Proč se přípravek Fluspiral používá? K čemu to je?
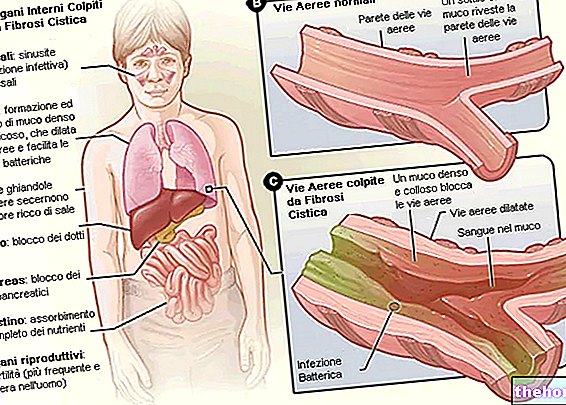
Tento léčivý přípravek obsahuje léčivou látku flutikason-propionát, která patří do skupiny léčiv nazývaných kortikosteroidy, léky používané k léčbě astmatu (k léčbě astmatu, zánětlivého onemocnění charakterizovaného „reverzibilní obstrukcí dolních cest dýchacích) vdechováním.
Flutikason-propionát snižuje otoky a záněty v plicích (protizánětlivé působení).
Tento léčivý přípravek je indikován k léčbě astmatických onemocnění a stavů bronchostenózy (snížení průdušek).
Kontraindikace Kdy by neměl být přípravek Fluspiral používán
Nepoužívejte přípravek Fluspiral
- jestliže jste alergický (á) na flutikason -propionát nebo na kteroukoli další složku tohoto přípravku.
Opatření pro použití Co potřebujete vědět, než začnete přípravek Fluspiral užívat
Před užitím přípravku Fluspiral se poraďte se svým lékařem nebo lékárníkem. Obraťte se na svého lékaře zejména v případě:
- máte aktivní nebo klidovou tuberkulózu (TBC, nakažlivé onemocnění způsobené bakterií).
- je diabetický pacient
- máte respirační onemocnění zvané Chronická obstrukční plicní nemoc (CHOPN)
- přechází z perorální terapie steroidy na inhalační flutikason. V tomto případě byste měl být léčen se zvláštní péčí svého lékaře, který bude muset pravidelně sledovat vaši funkci nadledvin a postupně přerušovat orální terapii po zavedení inhalační terapie.Je proto vhodné mít u sebe visačku označující, že můžete potřebovat terapii. s kortikosteroidy v době stresu.
Pokud se vám po použití přípravku Fluspiral zpomalí dýchání (bronchospasmus se zvýšenou dušností), přestaňte lék užívat a okamžitě se poraďte se svým lékařem.Ve skutečnosti není flutikason -propionát podávaný rozprašováním indikován k léčbě symptomů záchvatu akutního bronchospasmu Suspenze flushpirálního rozprašovače nenahrazuje nouzovou terapii, která se místo toho vyskytuje u kortikosteroidů podávaných orálně nebo intravenózně.
Interakce Které léky nebo potraviny mohou ovlivnit účinek přípravku Fluspiral
Informujte svého lékaře, zdravotní sestru nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval (a) nebo které možná budete užívat.
Zejména informujte svého lékaře nebo lékárníka, pokud užíváte některý z následujících léků:
- ritonavir, typ antivirotika známý jako „inhibitor proteázy“;
- ketokonazol, lék používaný k léčbě houbových infekcí;
Fluspiral s jídlem a pitím
Fluspiral můžete používat kdykoli během dne, s jídlem nebo bez jídla.
Varování Je důležité vědět, že:
Nahrazení léčby systémovými kortikosteroidy inhalačními kortikosteroidy může vyvolat alergická onemocnění.
Léčba astmatu musí být obvykle prováděna v rámci terapeutického plánu přizpůsobeného závažnosti onemocnění; Vaše odpověď na terapii by měla být ověřena lékařem jak klinicky, tak pomocí plicních funkčních testů.
Potřeba častěji používat léky k potlačení symptomů astmatu naznačuje zhoršení kontroly nad nemocí; za těchto okolností musí váš léčebný plán změnit lékař.
Náhlé zhoršení astmatu je potenciálně život ohrožující a v tomto případě by měl lékař zvážit zvýšení dávky kortikosteroidů.
Je důležité, abyste užil (a) dávku podle pokynů svého lékaře. Dávku byste neměli zvyšovat ani snižovat, aniž byste požádali o radu svého lékaře. Léčbu flutikason -propionátem náhle nepřerušujte.
Při použití inhalačních glukokortikoidů (jako je flutikason -propionát), zvláště pokud jsou předepisovány ve vysokých dávkách po delší dobu, mohou nastat systémové (celotělové) účinky.Tyto účinky jsou méně pravděpodobné než při perorální léčbě glukokortikoidy.
Mezi možné systémové účinky patří Cushingova choroba (klinický stav charakterizovaný nadbytkem glukokortikoidů v krvi, který vede k obezitě, nedostatečnému výrazu v obličeji, červené kůži, rozsáhlým striím a hustým ochlupením, zejména na obličeji), vzhled cushingoidů (typický pro lidi) postiženo Cushingovou chorobou), útlum nadledvin (snížená funkce nadledvin), zpomalení růstu u dětí a mladistvých, snížená minerální hustota kostí, šedý zákal (zakalení čočky uvnitř oka), glaukom (závažné oční onemocnění) a vzácněji rozsah psychických nebo behaviorálních účinků včetně psychomotorické hyperaktivity, podrážděnosti, poruch spánku, úzkosti, deprese nebo poruch chování (zejména u dětí) (viz bod 4 „Možné nežádoucí účinky“). Je proto důležité, aby dávka inhalačního kortikosteroidu byla nejnižší možná dávka, se kterou je podáván účinná kontrola astmatu byla zachována.
U dětí dlouhodobě léčených inhalačními kortikosteroidy se doporučuje pravidelné sledování výšky.Ve velmi vzácných případech se vyskytly akutní adrenální krize u dětí vystavených vyšším než doporučeným dávkám (přibližně 1 000 mikrogramů denně) po delší dobu (několik měsíců nebo let).
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se před použitím tohoto přípravku se svým lékařem nebo lékárníkem.
Řízení dopravních prostředků a obsluha strojů
Je nepravděpodobné, že by Fluspiral ovlivňoval schopnost řídit nebo obsluhovat stroje.
Dávka, způsob a doba podání Jak používat Fluspiral: Dávkování
Vždy používejte tento přípravek přesně podle pokynů svého lékaře. Pokud máte pochybnosti, poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem.
Měli byste být informováni, že léčba tímto léčivým přípravkem je preventivní a že lék by měl být užíván pravidelně i bez příznaků.
Účinek tohoto léku trvá 4–7 dní a je velmi důležité, abyste jej pravidelně používal.
Nevstřikujte ani nepolykejte tekutinu.
Vezměte Fluspiral Suspension k rozprašování pomocí aerosolu generovaného pouze nebulizátorem.
Nepoužívejte suspenzi FLUSPIRAL ke stříkání ultrazvukovými rozprašovači.
- Nebulizátor vytváří mlhu, která je vdechována bukálním inhalátorem nebo inhalační maskou.
- Každá malá plastová nádoba (Nebules®) obsahuje kapalinu.
- Kapalina se vloží do nebulizátoru. To vytváří jemnou mlhu, která je vdechována maskou nebo náustkem. Použití náustku brání tomu, aby lék zasáhl pokožku obličeje, což se může stát, pokud používáte masku delší dobu. Pokud dáváte přednost masce nebo pokud používáte masku pro své dítě, můžete Po ošetření je třeba pokožku obličeje chránit krémem nebo si důkladně umýt obličej. Pokud použijete masku, může dojít k vdechnutí nosu. Použijte rozprašovač v dobře větrané místnosti, protože mlha uvolněná do vzduchu může být částečně vdechována i od ostatních.
Váš lékař předepíše vhodné dávkování pro tento léčivý přípravek po zhodnocení závažnosti vašeho astmatu a vaší individuální odpovědi. Lékař může dávku postupně snižovat, pokud je váš dech stabilizovaný.
Dospělí a mladiství starší 16 let
- Obvykle doporučená dávka je 250 mcg (½ láhve 500 mcg NEBULES) dvakrát denně.
- Fluspirální nebulizační suspenze 0,5 mg / 2 ml poskytuje dávku 500 mikrogramů.
Následně by měla být dávka upravována, dokud není dosaženo kontroly astmatu (500-2000 mcg dvakrát denně), nebo snížena podle individuální odpovědi, dokud není dosaženo minimální účinné udržovací dávky.
K léčbě epizod exacerbace se doporučuje použít vysokou dávku (na horním okraji doporučeného rozmezí dávek) po dobu 7 dnů po exacerbaci.
Následně by mělo být zváženo snížení dávky.
Děti (4 až 16 let)
- Obvykle doporučená dávka je 250 mcg (½ láhve 500 mcg NEBULES) dvakrát denně.
Pacienti by měli být léčeni počáteční nebulizační dávkou flutikason -propionátu přiměřenou závažnosti jejich onemocnění. Poté by měla být dávka upravována, dokud není dosaženo kontroly astmatu, nebo snížena podle individuální odpovědi, dokud není dosaženo minimální účinné udržovací dávky.
Při léčbě epizod exacerbací astmatu je doporučená dávka 1 mg 2krát denně (2 nádoby NEBULES po 500 mcg 2krát denně) po dobu až 7 dnů léčby.
Poté by mělo být dávkování upraveno podle individuální odpovědi.
Doporučuje se, aby lékař pravidelně sledoval výšku dětí léčených steroidy, včetně suspenze rozprašovače Fluspiral.
Pokud již delší dobu používáte vysoké dávky inhalačního steroidu, někdy může být nutné použít další dávky steroidu například během stresových okolností, jako je například dopravní nehoda nebo před operací. Váš lékař se během této doby může rozhodnout předepsat steroidní doplněk.
Pacienti, kteří byli dlouhodobě léčeni vysokými dávkami steroidů, včetně suspenze Fluspiral Nebulizer, by neměli náhle přestat užívat lék, aniž by o tom nejprve informovali svého lékaře. Náhlé ukončení léčby může způsobit malátnost a příznaky jako zvracení, ospalost, nevolnost, bolest hlavy, únava, ztráta chuti k jídlu, nízká hladina cukru v krvi (hypoglykémie) a změny hmotnosti.
Pokyny k používání mlhovin
- Kontejner Nebules je zabalen do obalu. Neotevírejte balíček, dokud jej nepotřebujete. Před použitím se ujistěte, že je obsah nádoby dobře promíchán.Uchopte nádobu vodorovně od označeného konce, několikrát klepněte na opačný konec a protřepejte. Tento postup několikrát opakujte, dokud se celý obsah nádoby úplně nerozmíchá.
- Chcete -li otevřít nádobu, otočte zašroubováním horní části.
- Vložte suspenzi do nebulizátoru podle pokynů výrobce pro použití nebulizátoru.
Ředění suspenze mlhovin
Neřeďte obsah suspenze Nebules, pokud vám to lékař neřekne
- Pokud vám lékař řekl, abyste zředil roztok, vyprázdněte obsah mlhovin do ampule nebulizátoru.
- Přidejte množství fyziologického roztoku pro injekční použití, které vám lékař řekl k použití.
Jestliže jste zapomněl (a) použít přípravek Fluspiral
- Nezdvojnásobujte následující dávku, abyste nahradil (a) vynechanou dávku.
Jestliže jste přestal (a) užívat přípravek Fluspiral
- Nepřerušujte léčbu, i když se cítíte lépe, pokud vám to lékař neřekne. Pokud ano, nepřestávejte Fluspiral náhle.
Máte -li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
Předávkování Co dělat, když jste užil příliš mnoho přípravku Fluspiral
V případě náhodného požití / požití předávkování přípravkem Fluspiral okamžitě informujte svého lékaře nebo jděte do nejbližší nemocnice.
Akutní inhalace přípravku Fluspiral ve vyšších než doporučených dávkách může vést k dočasnému potlačení funkce nadledvin (příznaky viz „Upozornění a opatření“).
Není nutné zavádět nouzové zásahy, protože funkce nadledvin se během několika dnů vrátí do normálu.
Pokud jsou však delší dobu používány vyšší než doporučené dávky, může dojít k určitému stupni útlumu nadledvin. Váš lékař může nařídit testy, aby zkontroloval, jak dobře funguje vaše nadledvina.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Fluspiral
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Přestaňte ho užívat a okamžitě kontaktujte svého lékaře, pokud po užití přípravku Fluspiral zaznamenáte některý z následujících příznaků:
- alergické reakce charakterizované kožními vyrážkami (přecitlivělost kůže);
- otok obličeje, rtů, úst, jazyka nebo hrdla, který může způsobit potíže s polykáním (angioedém);
- dýchací potíže (dušnost a / nebo bronchospasmus, paradoxní bronchospasmus).
Mezi další nežádoucí účinky patří:
Velmi časté (mohou postihnout více než 1 z 10 lidí)
- drozd v ústech a krku (bolestivé, krémově žluté vyvýšené skvrny).
Časté (mohou postihnout až 1 z 10 lidí)
- pohmožděniny
- chraplavý hlas (chrapot).
Problémy s ústy a krkem lze omezit některými konkrétními opatřeními, jako je čištění zubů nebo výplach ústa vypláchnout vodou bezprostředně po vdechnutí dávky. Kromě toho byla u pacientů s chronickou obstrukční plicní nemocí (CHOPN) hlášena pneumonie. infekce).
Velmi vzácné (mohou postihnout až 1 z 10 000 lidí)
- drozd (kandidóza) v jícnu;
- úzkost, poruchy spánku a poruchy chování, včetně hyperaktivity a podrážděnosti (převážně u dětí);
- zvýšený obsah cukru (glukózy) v krvi (hyperglykémie);
- zpomalení růstu u mladých lidí;
- Cushingův syndrom, stav charakterizovaný nadbytkem steroidních hormonů v krevním řečišti, což má za následek zaoblený vzhled obličeje; řídnutí kostí; oční problémy, jako je katarakta (zakalení oční čočky) a glaukom (zvýšený nitrooční tlak); účinky na nadledvinu (malá žláza umístěná vedle ledviny).
Není známo (frekvenci nelze z dostupných údajů určit):
- deprese, agrese. Tyto účinky se pravděpodobněji vyskytují u dětí.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48100 41 Praha 10 Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
Expirace a retence
- Uchovávejte tento přípravek mimo dohled a dosah dětí.
- Uchovávejte mlhoviny Fluspiral v obalu uvnitř krabice.
- Uchovávejte při teplotě do 30 ° C. Uchovávejte obal ve vnějším obalu, aby byl chráněn před světlem a mrazem.
- Pokud nebyl obal odstraněn, nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na obalu za „EXP“. Datum se vztahuje k poslednímu dni daného měsíce.
- Lahvičky s mlhovinami vyjmuté z obalu musí být chráněny před světlem a spotřebovány do 1 měsíce.
- Otevřené lahvičky Nebules je třeba uchovávat v chladničce a spotřebovat do 12 hodin od otevření. Neuchovávejte v mrazničce.
- Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Jiná informace
Co přípravek Fluspiral obsahuje
- Léčivou látkou je fluticasoni propionas.
- Dalšími složkami jsou polysorbát 20, sorbitan monolaurát, dihydrát hydrogenfosforečnanu sodného, bezvodý hydrogenfosforečnan sodný, chlorid sodný (sůl), voda.
Jak Fluspiral vypadá Tlaková suspenze a obsah balení
- Injekční lahvičky Fluspiral Nebules jsou baleny v 5 ml blistru v obalu. Jedna krabička obsahuje 10 ml 2ml lahviček.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
FLUSPIRAL 500 MCG / 2 ML SUSPENSION K NEBULIZE
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
2ml nádoba NEBULES obsahuje:
Účinná látka: Fluticason propionát (mikronizovaný) 500 mcg
Úplný seznam pomocných látek viz bod 6.1
03.0 LÉKOVÁ FORMA
Suspenze k rozprašování (pomocí aerosolového zařízení).
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Suspenze nebulizátoru FLUSPIRAL je indikována při kontrole vývoje astmatického onemocnění a stavů bronchostenózy.
04.2 Dávkování a způsob podání
Pacienti by měli být poučeni o profylaktické povaze léčby inhalačním flutikason -propionátem a o tom, že by měla být používána pravidelně, i když příznaky odezní.
Suspenze rozprašovače FLUSPIRAL musí být podávána aerosolem generovaným nebulizátorem, podle pokynů lékaře.
Přečtěte si pokyny k použití doporučené výrobcem nebulizátoru.
Použití suspenze FLUSPIRAL k rozprašování ultrazvukovými rozprašovači se nedoporučuje.
Suspenze rozprašovače FLUSPIRAL není pro injekční použití.
FLUSPIRAL Nebulizer Suspension by měl být používán ústním inhalátorem a doporučuje se použití ústního inhalátoru.U dětí školního věku se doporučuje hlavně použití ústního inhalátoru; u mladších dětí může být naopak užitečná inhalační maska. V případě použití inhalační obličejové masky může dojít k vdechnutí nosu.
Maximálního zlepšení astmatu lze dosáhnout za 4-7 dní od zahájení léčby; Ukázalo se však, že flutikason -propionát vykazuje terapeutický účinek během prvních 24 hodin u pacientů, kteří nebyli dříve léčeni inhalačními steroidy.
Pokud si pacient všimne snížení účinnosti krátkodobě působících bronchodilatancií nebo vyšší frekvence jejich užívání, je nutné vyhledat lékařskou pomoc.
Pro podávání malých objemů nebo pokud je žádoucí prodloužit dobu nebulizace, lze suspenzi ředit bezprostředně před použitím fyziologickým roztokem pro injekční použití.
Vzhledem k tomu, že mnoho rozprašovačů pracuje v kontinuálním proudu, je pravděpodobné, že se nebulizované léčivo uvolní do životního prostředí. FLUSPIRAL Nebulizer Suspension by proto měl být podáván v dobře větrané místnosti, zejména v nemocnicích, kde lze léčit více pacientů současně.
Dospělí a mladiství starší 16 let
Obvykle doporučená dávka je 250 mcg (½ láhve 500 mcg NEBULES) dvakrát denně.
Pacienti by měli být léčeni počáteční nebulizační dávkou flutikason -propionátu přiměřenou závažnosti jejich onemocnění.
Následně by měla být dávka upravována, dokud není dosaženo kontroly astmatu (500-2000 mcg 2krát denně), nebo snížena podle individuální odpovědi, dokud není dosaženo minimální účinné udržovací dávky.
K léčbě epizod exacerbace se doporučuje použít vysokou dávku (na horním okraji doporučeného rozmezí dávek) po dobu 7 dnů po exacerbaci.
Následně by mělo být zváženo snížení dávky.
Děti a mladiství od 4 do 16 let
Obvykle doporučená dávka je 250 mcg (½ láhve 500 mcg NEBULES) dvakrát denně.
Pacienti by měli být léčeni počáteční nebulizační dávkou flutikason -propionátu přiměřenou závažnosti jejich onemocnění.
Poté by měla být dávka upravována, dokud není dosaženo kontroly astmatu, nebo snížena podle individuální odpovědi, dokud není dosaženo minimální účinné udržovací dávky.
Při léčbě epizod exacerbací astmatu je doporučená dávka 1 mg 2krát denně (2 NEBULES 500 mcg nádoby, 2krát denně) po dobu až 7 dnů léčby.
Poté by mělo být dávkování upraveno podle individuální odpovědi.
Každý kontejner NEBULES je vybaven zářezem označujícím poloviční dávku.
Zvláštní populace pacientů
U starších pacientů nebo pacientů s jaterní nebo renální insuficiencí není nutné snižovat dávku léku.
04.3 Kontraindikace
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Léčba astmatu musí být obvykle prováděna v rámci terapeutického plánu přizpůsobeného závažnosti onemocnění; odpověď pacienta na terapii by měla být ověřena jak klinicky, tak pomocí plicních funkčních testů, jsou -li k dispozici.
Potřeba častějšího používání rychle působících inhalačních beta2-agonistů ke kontrole symptomů naznačuje zhoršení kontroly astmatu; za této okolnosti musí být plán léčby pacienta upraven.
Náhlé a progresivní zhoršení astmatu je potenciálně život ohrožující a je třeba zvážit zvýšení dávky kortikosteroidů. U pacientů považovaných za rizikové může lékař doporučit denní sledování maximálního průtoku.
U inhalačních kortikosteroidů se mohou objevit systémové účinky, zvláště pokud jsou předepisovány ve vysokých dávkách po delší dobu. Tyto účinky jsou méně pravděpodobné než u léčby perorálními kortikosteroidy. Mezi možné systémové účinky patří Cushingův syndrom, cushingoidní aspekt, adrenální suprese, zpomalení růstu u dětí a mladistvých, snížená minerální hustota kostí, katarakta, glaukom a vzácněji řada psychologických nebo behaviorálních účinků včetně psychomotorické hyperaktivity, poruchy spánku, úzkost, deprese nebo agrese (zejména u dětí). Je proto důležité, aby dávka inhalačního kortikosteroidu byla nejnižší možnou dávkou, se kterou je udržována účinná kontrola astmatu (viz bod 4.8).
Doporučuje se pravidelně sledovat výšku dětí dlouhodobě léčených inhalačními kortikosteroidy.
Vzhledem k možnosti nedostatečné adrenální reakce by pacienti dříve léčeni perorálními steroidy, kteří jsou převedeni na léčbu inhalačním flutikason -propionátem, měli být léčeni se zvláštní péčí a funkce nadledvin by měla být pravidelně sledována.
Přerušení léčby systémovými steroidy by mělo být postupné a pacienti by měli být poučeni, aby měli u sebe ukazatel, který naznačuje, že mohou během stresové situace vyžadovat doplňkovou léčbu kortikosteroidy.
Vždy je třeba mít na paměti možnost nedostatečné nadledvinové reakce v nouzových situacích (včetně chirurgických zákroků) a také při volitelných intervencích, které mohou způsobit stres, zvláště u pacientů dlouhodobě užívajících vysoké dávky. Je třeba zvážit další léčbu kortikosteroidy vhodnou pro klinickou situaci (viz bod 4.9).
Nahrazení léčby systémovými kortikosteroidy inhalační terapií může odhalit alergie, jako je alergická rýma nebo ekzém, které byly dříve maskovány systémovými léky.
Léčba flutikason -propionátem by neměla být náhle ukončena.
Byly velmi vzácně hlášeny případy zvýšení hladin glukózy v krvi (viz bod 4.8) a toto je třeba vzít v úvahu při předepisování léku pacientům s anamnézou diabetes mellitus.
Stejně jako všechny inhalační kortikosteroidy je nutná zvláštní péče u pacientů s aktivními nebo klidovými formami plicní tuberkulózy.
Po uvedení přípravku na trh byly u pacientů léčených flutikason-propionátem a ritonavirem hlášeny případy klinicky významných lékových interakcí, které vedly k systémovým účinkům kortikosteroidů, včetně Cushingova syndromu a adrenální suprese. prospěch pro pacienta převažuje nad rizikem vzniku systémových nežádoucích účinků kortikosteroidů (viz bod 4.5).
Stejně jako u jiných inhalačních léků může dojít k paradoxnímu bronchospasmu se zvýšenou dušností bezprostředně po užití léku. V takovém případě okamžitě vezměte rychle působící bronchodilatátor, okamžitě přerušte léčbu flutikason-propionátem, přehodnoťte pacienta a v případě potřeby zahájte alternativní léčbu (viz. bod 4.8).
Ve studiích pacientů s CHOPN, kteří dostávali flutikason -propionát v dávce 500 mikrogramů (viz bod 4.8), došlo k nárůstu hlášení pneumonie (viz bod 4.8). Lékaři by měli dávat pozor na možný vývoj zápalu plic u pacientů s CHOPN, protože klinické rysy pneumonie a exacerbace se často překrývají.
Flutikason-propionát podávaný nebulizací není indikován jako monoterapie k řešení symptomů vyplývajících z akutního záchvatu bronchospasmu, u kterého je také vyžadován krátkodobý krátkodobě působící inhalační bronchodilatátor (např. Salbutamol). Propionát podávaný nebulizací je určen k pravidelná denní léčba a jako protizánětlivá terapie při akutních exacerbacích astmatu.
Těžké astma vyžaduje pravidelný lékařský dohled, protože může být pro pacienta život ohrožujícím stavem.
Náhlé zhoršení symptomů může vyžadovat zvýšení dávky kortikosteroidů, které je nutné naléhavě podávat pod lékařským dohledem.
Suspenze nebulizátoru FLUSPIRAL nenahrazuje injekční nebo orální terapii kortikosteroidy v nouzové situaci.
Pacienti, kteří dostávají flutikason -propionát podávaný nebulizací, by měli být upozorněni, že v případě zhoršení jejich stavu by neměli zvyšovat dávku nebo frekvenci podávání, ale měli by vyhledat lékařskou pomoc.
Doporučuje se podávat nebulizovaný flutikason pomocí bukálního inhalátoru, aby se zabránilo možnosti, že při dlouhodobém používání inhalační obličejové masky mohou nastat atrofické změny na kůži obličeje.
Při použití inhalační obličejové masky by měla být exponovaná kůže chráněna ochrannými krémy nebo umytím obličeje po spreji.
Prodloužená léčba suspenzí rozprašovače FLUSPIRAL by měla být postupně snižována pod lékařským dohledem a neměla by být náhle ukončena.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Za normálních okolností jsou po inhalačním podání dosaženy nízké plazmatické koncentrace flutikason -propionátu v důsledku rozsáhlého first -pass metabolismu a vysoké systémové clearance zprostředkované cytochromem P450 3A4 ve střevě a játrech. Interakce jsou proto nepravděpodobné. Klinicky významný lék zprostředkovaný flutikason -propionátem.
Interakční studie provedená na zdravých dobrovolnících ukázala, že ritonavir (velmi účinný inhibitor cytochromu P450 3A4) může významně zvýšit plazmatické koncentrace flutikason -propionátu, což má za následek výrazně snížené sérové koncentrace kortizolu.
Během postmarketingového používání byly u pacientů léčených intranazálním nebo inhalačním flutikason-propionátem a ritonavirem hlášeny případy klinicky významných lékových interakcí, což mělo za následek systémové účinky kortikosteroidů, včetně Cushingova syndromu a adrenální suprese.
Proto je třeba se vyhnout souběžnému užívání flutikason -propionátu a ritonaviru, pokud potenciální přínos pro pacienta nepřeváží rizika systémových vedlejších účinků kortikosteroidů.
Studie ukázaly, že jiné inhibitory cytochromu P450 3A4 produkují zanedbatelné (erythromycin) a malé (ketokonazol) zvýšení systémové expozice flutikason -propionátu bez výrazného snížení sérových koncentrací kortizolu. Doporučuje se však opatrnost v případě silných inhibitorů cytochromu P450 3A4 (např. ketokonazol) jsou podávány souběžně, protože by mohlo dojít k potenciálně zvýšené systémové expozici flutikason -propionátu.
04.6 Těhotenství a kojení
Plodnost
Nejsou k dispozici žádné údaje o lidské plodnosti. Studie s flutikasonem na zvířatech neprokázaly žádné účinky na mužskou a ženskou plodnost. Studie na zvířatech s cílem vyhodnotit jakoukoli interferenci flutikason -propionátu s reprodukční funkcí prokázaly pouze ty účinky charakteristické pro glukokortikoidy při úrovních systémové expozice, které jsou mnohem vyšší než účinky pozorované při doporučené terapeutické dávce při vdechování.
Těhotenství
Údaje o těhotných ženách jsou omezené. Podávání flutikason -propionátu během těhotenství by mělo být zvažováno pouze tehdy, pokud očekávaný přínos pro matku převáží možná rizika pro plod.
Výsledky retrospektivní epidemiologické studie ukazují, že riziko závažných vrozených vývojových vad (MCM) po expozici samotnému flutikason -propionátu a v kombinaci se salmeterolem není vyšší než riziko zjištěné po expozici jiným inhalačním kortikosteroidům., Během prvního trimestru těhotenství (viz. bod 5.1 Klinické studie).
Čas krmení
Není známo, zda se flutikason -propionát vylučuje do lidského mateřského mléka. Po subkutánním podání u potkanů byla přítomnost flutikason -propionátu v mateřském mléce zjištěna pouze za přítomnosti měřitelných plazmatických koncentrací. Plazmatické hladiny jsou však pravděpodobně nízké u pacientů užívajících flutikason -propionát v doporučených dávkách.
Podávání během laktace by mělo být zvažováno pouze tehdy, pokud očekávaný přínos pro matku převáží možná rizika pro plod.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Následky po použití flutikason -propionátu pravděpodobně nenastanou.
04.8 Nežádoucí účinky
Nežádoucí účinky jsou uvedeny níže podle orgánů, orgánů / systémů a podle frekvence. Frekvence jsou definovány jako: velmi časté (≥1 / 10), časté (≥1 / 100,
Infekce a infestace
Velmi časté: Kandidóza úst a hrdla.
U některých pacientů se může objevit orofaryngeální kandidóza (drozd). Tito pacienti mohou mít prospěch z vypláchnutí úst vodou po užití léku.Symptomatickou kandidózu lze léčit topickou antifungální terapií bez přerušení používání fluticason propionátu.
Časté: Pneumonie (u pacientů s CHOPN)
Velmi vzácné: kandidóza jícnu
Poruchy imunitního systému
Byly hlášeny následující reakce přecitlivělosti:
Méně časté: Reakce přecitlivělosti kůže.
Velmi vzácné: Angioedém (hlavně edém obličeje a orofaryngu), respirační příznaky (dušnost a / nebo bronchospasmus) a anafylaktické reakce.
Endokrinní patologie
Mezi možné systémové účinky patří (viz bod 4.4):
Velmi vzácné: Cushingův syndrom, vzhled Cushingoidů, útlum nadledvin, zpomalení růstu, snížení minerální denzity kostí, katarakta, glaukom.
Poruchy metabolismu a výživy
Velmi vzácné: Hyperglykémie.
Psychiatrické poruchy
Velmi vzácné: Úzkost, poruchy spánku a poruchy chování, včetně psychomotorické hyperaktivity a podrážděnosti (převážně u dětí).
Není známo: deprese, agrese (převážně u dětí).
Respirační, hrudní a mediastinální poruchy
Časté: chrapot.
U některých pacientů se může objevit chrapot; i v těchto případech může být výhodné vypláchnout ústa vodou bezprostředně po vdechnutí.
Velmi vzácné: paradoxní bronchospasmus (viz bod 4.4).
Není známo: epistaxe
Poruchy kůže a podkožní tkáně
Časté: modřiny
Hlášení podezření na nežádoucí účinky.
Hlášení podezření na nežádoucí účinky, ke kterým dochází po registraci léčivého přípravku, je důležité, protože umožňuje průběžné sledování poměru přínosů a rizik léčivého přípravku. Zdravotničtí pracovníci jsou požádáni, aby hlásili jakékoli podezření na nežádoucí účinky prostřednictvím národního systému hlášení. "Adresa www. agenziafarmaco.gov.it/it/responsabili.
04.9 Předávkování
Příznaky a příznaky
Akutní vdechnutí léčiva ve vyšších než doporučených dávkách může vést k dočasnému potlačení osy hypotalamus-hypofýza-nadledviny. To obvykle nevyžaduje zavedení nouzových intervencí, protože adrenokortikální funkce se obvykle vrátí do normálu během několika dnů.
Pokud jsou delší dobu používány dávky vyšší než schválené, může dojít k výraznému potlačení funkce nadledvin. Může být nutné sledování nadledvinové rezervy.
Vyskytly se velmi vzácné případy akutní adrenální krize u dětí vystavených vyšším než doporučeným dávkám (obvykle 1000 mcg / den a vyšším) po delší dobu (několik měsíců nebo let); pozorované projevy zahrnovaly hypoglykémii a následky sníženého vědomí a / nebo křeče).
Situace, které mohou potenciálně vyvolat akutní adrenální krizi, zahrnují vystavení traumatu, chirurgickému zákroku, infekci nebo jakémukoli rychlému snížení dávky.
Léčba
Pacienti léčení vyššími než schválenými dávkami by měli být pečlivě sledováni a dávku postupně snižovat.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Léky na obstrukční syndromy dýchacích cest - inhalační glukokortikoidy.
ATC kód: R03BA05.
Mechanismus účinku
Flutikason-propionát podávaný inhalací v doporučených dávkách má v plicích silnou protizánětlivou aktivitu, snižuje symptomy a epizody exacerbace astmatu.
Klinické studie
Léky obsahující flutikason -propionát u těhotných žen s astmatem
Byla provedena epidemiologická observační retrospektivní kohortová studie s využitím elektronických zdravotních záznamů z Velké Británie za účelem posouzení rizika MCM po expozici kombinaci inhalačního flutikason-propionátu a salmeterol-flutikason-propionátu oproti inhalačním kortikosteroidům neobsahujícím flutikason-propionát. Během prvního trimestru těhotenství Žádné srovnání s v této studii bylo vyrobeno placebo.
V kohortě 5 362 těhotných žen s astmatem vystavených v prvním trimestru inhalačním kortikosteroidům bylo za jeden rok identifikováno 131 diagnóz MCM; 1612 (30%) bylo vystaveno fluticason propionátu nebo salmeterol-fluticason propionátu, z nichž 42 bylo diagnostikováno s MCM. Upravený poměr pravděpodobnosti pro diagnózy MCM nad jeden rok byl 1,1 (95% CI: 0,5 - 2,3) u žen se středně těžkým astmatem vystavených flutikason -propionátu oproti ženám vystaveným kortikosteroidům neobsahujícím flutikason -propionát a 1, 2 (95% CI: 0,7 - 2,0) u žen se značným až závažným astmatem Nebyly identifikovány žádné rozdíly v riziku MCM po expozici flutikason-propionátu v prvním trimestru oproti kombinaci salmeterol-flutikason-propionát. Absolutní riziko MCM v různých rozmezích závažnosti astmatu se pohybovalo od 2,0 do 2,9 na 100 těhotenství vystavených flutikason -propionátu.
05.2 Farmakokinetické vlastnosti
Vstřebávání
Absolutní biologická dostupnost flutikason -propionátu pro každý typ regulátoru vdechnutí byla hodnocena ve srovnávacích studiích a srovnávacích studiích farmakokinetických údajů po inhalačním nebo intravenózním podání. U zdravých dospělých subjektů byla hodnocena. Absolutní biologická dostupnost prášku flutikason -propionátu pro inhalaci v inhalátoru Diskus (7,8%), respektive byla hodnocena inhalační tlaková suspenze flutikason -propionátu (10,9%). U subjektů s astmatem nebo chronickou obstrukční plicní nemocí (CHOPN) byla pozorována nižší úroveň systémové expozice vdechovanému flutikason -propionátu. K systémové absorpci dochází především prostřednictvím plíce a je zpočátku rychlý a poté prodloužený. Zbývající část inhalované dávky lze požit, ale zanedbatelně přispívá k systémové expozici v důsledku nízké rozpustnosti ve vodě a presystémového metabolismu, přičemž orální dostupnost je nižší než 1%. Existuje lineární zvýšení systémové expozice ve vztahu ke zvýšení inhalační dávky.
Rozdělení
Flutikason-propionát má velký distribuční objem v ustáleném stavu (přibližně 300 l). Vazba na plazmatické bílkoviny je středně vysoká (91%).
Biotransformace
Flutikason -propionát je velmi rychle odstraňován ze systémového oběhu, hlavně metabolizací na neaktivní sloučeninu karboxylové kyseliny, cytochromem P450 enzymatického systému CYP3A4. Při podávání léků, o nichž je známo, že inhibují enzymatický systém CYP3A4, je třeba postupovat opatrně, protože existuje možnost zvýšené systémové expozice flutikason -propionátu.
Odstranění
Eliminace flutikason-propionátu je charakterizována "vysokou plazmatickou clearance (1150 ml / min) a" terminálním eliminačním poločasem přibližně 8 hodin. Renální clearance flutikason-propionátu je zanedbatelná (méně než 0,2%) a méně než 5 % je eliminováno jako metabolit.
05.3 Předklinické údaje vztahující se k bezpečnosti
Toxikologické testy ukázaly při dávkách vyšších, než jsou dávky navržené pro terapeutické použití, jedinou třídu účinků typických pro vysoce účinný kortikosteroid.
Studie chronické toxicity neodhalily účinky jiné povahy, stejně jako studie reprodukční toxikologie a teratogeneze.
Bylo zjištěno, že flutikason-propionát je nemutagenní in vitro a in vivo a ne-onkogenní u hlodavců.
Na zvířecích modelech bylo zjištěno, že fluticason propionát není dráždivý a nesenzibilizující.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Polysorbát 20, sorbitan monolaurát, dihydrát dihydrogenfosforečnanu sodného, bezvodý hydrogenfosforečnan sodný, chlorid sodný, voda na injekci.
06.2 Neslučitelnost
Nenahlásit.
06.3 Doba platnosti
3 roky.
06.4 Zvláštní opatření pro skladování
Uchovávejte výrobek ve vzpřímené poloze, jak je uvedeno na obalu.
Uchovávejte při teplotě do 30 ° C.
Chraňte před mrazem a světlem.
Po otevření ochranného obalu musí být jednodávkové obaly použity do jednoho měsíce.
Chraňte před mrazem. Otevřené nádoby musí být vloženy do chladničky a spotřebovány do 12 hodin od otevření.
06.5 Charakter vnitřního obalu a obsah balení
FLUSPIRAL suspenze k nebulizaci je dodávána v 2,5 ml farmaceutickém obalu z nízkohustotního polyetylenu NEBULES
FLUSPIRAL 500 mcg / 2 ml - suspenze k rozprašování: 10 jednodávkových obalů po 2 ml NEBULES
06.6 Návod k použití a zacházení
Při používání nebulizátoru se řiďte pokyny výrobce.
Je důležité zajistit, aby byl obsah nádoby před použitím dobře promíchán. Držte nádobu vodorovně od označeného konce, několikrát poklepejte na opačný konec a protřepejte. Tento postup několikrát opakujte, dokud se celý obsah nádoby důkladně nerozmixuje.
Chcete -li otevřít nádobu, otočte zašroubováním horní části.
Ředění
Pokud je to nutné, zřeďte fyziologickým roztokem pro injekci.
Zlikvidujte veškerou nepoužitou část suspenze do nebulizátoru.
Doporučuje se podávat ústním inhalátorem.
Pokud používáte inhalační masku, po ošetření si důkladně umyjte obličej.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
A. Menarini Industrie Farmaceutiche Riunite s.r.l., Via Sette Santi, 3 - Florencie
na základě licence od společnosti GlaxoSmithKline S.p.A. - Verona
Prodejce na prodej:
Luso Farmaco Institute of Italy S.p.A. - Milanofiori - silnice 6 - budova L - Rozzano (MI)
08.0 REGISTRAČNÍ ČÍSLO
FLUSPIRAL 500 mcg / 2 ml - Suspenze k rozprašování - 10 jednodávkových obalů po 2 ml NEBULES A.I.C.: 028675294
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Říjen 2001 / květen 2008
10.0 DATUM REVIZE TEXTU
Března 2017