Upravil Dr. Giovanni Chetta
ECM je obecně popisován jako složený z několika velkých tříd biomolekul:
- Strukturální proteiny (kolagen a elastin)
- Specializované proteiny (fibrillin, fibronectin, laminin atd.)
- Proteoglykany (agregány, syndekany) a glusaminoglykany (hyaluronany, chondroitin -sulfáty, heparansulfáty atd.)
Strukturální proteiny
Kolageny tvoří nejvíce zastoupenou rodinu glykoproteinů v živočišné říši. Jsou to nejpřítomnější proteiny v extracelulární matrix (ale ne nejdůležitější) a jsou základními složkami vlastních pojivových tkání (chrupavky, kosti, fascie, šlachy, vazy).
Existuje nejméně 16 různých typů kolagenu, z nichž jsou na úrovni typických fibril nejčastěji přítomny typy I, II a III (typ IV tvoří jakési retikulum, které představuje hlavní složku bazálních lamel).
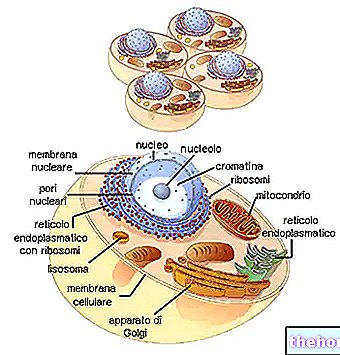
Kolageny jsou většinou syntetizovány fibroblasty, ale epiteliální buňky jsou také schopny je syntetizovat.
Kolagenová vlákna nepřetržitě interagují s obrovským množstvím dalších molekul extracelulární matrix, což představuje biologické kontinuum zásadní pro život buňky. Přidružené kolageny ve fibrilech hrají dominantní roli při tvorbě a udržování struktur schopných odolávat napínacím silám, jsou téměř nepružné (glukosaminy mohou působit na odolnost vůči stlačení). Kolagen se nějakým způsobem vyrábí a re-metabolizuje v závislosti na mechanickém zatížení a jeho viskoelastické vlastnosti, jak uvidíme v odstavci „Viskoelasticita fascia “, velký dopad na držení těla. Jako další demonstrace schopnosti kolagenu měnit se podle vlivů prostředí, za předpokladu např. variabilní stupně tuhosti, pružnosti a odolnosti, existují kolageny, definované pojmem FACIT (Fibril Associated Collagen with Interrupted Triple helix) schopné fungovat funkčně jako proteoglykany (popsáno v odstavci „Glukosaminoglykany a proteoglykany“).
Kolagenová vlákna díky svému povlaku PG / GAG (proteoglykany / glukosaminoglykany) mají vlastnosti biosenzorů a biovodičů: relativní elektrické náboje vedou k větší schopnosti vázat vodu a vyměňovat ionty, tedy i větší elektrickou kapacitu.
Víme, že jakákoli mechanická síla schopná generovat strukturální deformaci namáhá mezimolekulární vazby a vytváří mírný elektrický tok, tj. piezoelektrický proud (Athenstaedt, 1969). V takových případech kolagenová vlákna rozdělují kladné náboje na jejich konvexní povrch a negativní na konkávní, čímž se transformují na polovodiče (umožňují tok elektronů na jejich jednosměrném povrchu). Vzhledem k tomu, že piezoelektrická energie (stejně jako pyroelektrická energie generovaná tepelným napětím) je ve velmi krátkém čase (přibližně 10-7-10-9 sekund) neutralizována cirkulujícími ionty, je uspořádání PG / GAG na signálu je rozhodující pro šíření signálu.povrch vláken, jako například "opakovače" elektrického impulsu. Zejména podélná periodicita cca. 64 nm (což se pod optickým mikroskopem jeví jako pruh) umožňuje rychlost šíření impulsu přibližně 64 m / s (což odpovídá rychlosti vedení rychlých nervových vláken) - Rengling, 2001. Silný dipolární moment kolagenových fibril a jejich rezonanční kapacita (vlastnost společná pro všechny peptidové struktury), stejně jako nízká dielektrická konstanta MEC, usnadňují přenos elektromagnetických signálů.Proto trojrozměrná a všudypřítomná kolagenová síť má také zvláštní charakteristiku vedení bioelektrických signálů v tři rozměry prostoru, založené na relativním uspořádání mezi kolagenovými vlákny a buňkami, v aferentním směru (od ECM k buňkám) nebo naopak eferentní.
To vše představuje komunikační systém buněk MEC v reálném čase a takové elektromagnetické biosignály mohou vést k důležitým biochemickým změnám, například v kosti nemohou osteoklasty „strávit“ piezoelektricky nabitou kost (Oschman, 2000).
Na závěr je třeba zdůraznit, že buňka nepřekvapivě produkuje nepřetržitě a se značným výdejem energie (přibližně 70%) materiálu, který musí být nutně vyloučen, a to většinou prostřednictvím výhradního skladování protokolulagenu (biologického prekurzoru kolagenu) v konkrétních vezikuly (Albergati, 2004).
Drtivá většina tkání obratlovců vyžaduje současnou přítomnost dvou životně důležitých vlastností: síly a pružnosti. Skutečná síť elastických vláken, umístěná uvnitř ECM těchto tkání, umožňuje návrat do počátečních podmínek po silných tahech. Elastická vlákna jsou schopna zvýšit roztažnost orgánu nebo jeho části nejméně pětkrát. Mezi elastická vlákna jsou proložena dlouhá, nepružná kolagenová vlákna s přesným úkolem omezit „nadměrné deformace v důsledku tahu tkání. L“elastin představuje hlavní složku elastických vláken. Je to extrémně hydrofobní protein, dlouhý asi 750 aminokyselin, protože kolagen je bohatý na prolin a glycin, ale na rozdíl od kolagenu není glykovaný a obsahuje mnoho zbytků hydroxyprolinu, nikoli hydroxylisinu. Elastin se jeví jako skutečná biochemická síť nepravidelného trojrozměrného tvaru, složená z vláken a lamel, které prostupují ECM všech pojivových tkání. Ve zvláště hojném množství se nachází v cévách s elastickými vlastnostmi (je to protein ECM více přítomný v tepnách a představuje více než 50% celkové suché hmotnosti aorty), ve vazech, v plicích a v kůži. V dermis, na rozdíl od toho, co se děje u kolagenu, se hustota a objem elastinu v průběhu času zvyšuje, ale starý elastin obecně vypadá oteklý, téměř oteklý, často s roztříštěným vzhledem a s redukcí složky. „Amorfní“ (Pasquali Rochetti et al, 2004). Buňky hladkého svalstva a fibroblasty jsou hlavními producenty jeho prekurzoru, tropoelastinu, vylučovaného v extracelulárních prostorech.
Další články na téma "Kolagen a elastin, kolagenová vlákna v extracelulární matrix"
- Extracelulární matrix
- Fibronektin, glukosaminoglykany a proteoglykany
- Význam extracelulární matrice v buněčných rovnováhách
- Změny extracelulární matrix a patologie
- Pojivová tkáň a extracelulární matrix
- Hluboká fascie - pojivová tkáň
- Fasciální mechanoreceptory a myofibroblasty
- Biomechanika hluboké fascie
- Držení těla a dynamická rovnováha
- Tensegrity a šroubovicové pohyby
- Dolní končetiny a pohyb těla
- Podpora závěru a stomatognatický aparát
- Klinické případy, posturální změny
- Klinické případy, držení těla
- Posturální hodnocení - klinický případ
- Bibliografie - Od extracelulární matrix k držení těla. Je spojovací systém náš skutečný Deus ex machina?





















.jpg)
.jpg)