Aktivní složky: Kyselina listová (N5-methyltetrahydrofolát vápenatý)
15 mg enterosolventní tablety
Proč se používá Prefolic? K čemu to je?
FARMAKOTERAPEUTICKÁ KATEGORIE
Antianemické léky
TERAPEUTICKÉ INDIKACE
U všech forem nedostatku folátu v důsledku zvýšené poptávky, snížené absorpce, nedostatečného dietního příjmu.
V antidotické terapii nadměrných dávek antagonistů kyseliny listové a v boji proti vedlejším účinkům vyvolaným aminopterinem a methotrexátem.
Kontraindikace Kdy by přípravek Prefolic neměl být používán
Známá přecitlivělost na složky.
Pro intravenózní podání: souběžná léčba ceftriaxonem u novorozenců (ve věku ≤ 28 dní), a to i při použití oddělených infuzních linek. Viz oddíly „Interakce“, „Nežádoucí účinky“ a „Dávka, způsob a doba podání“.
Opatření pro použití Co potřebujete vědět před užitím přípravku Prefolic
V přítomnosti perniciózní anémie je dobrou praxí spojit vitamín B12 s přípravkem PREFOLIC, aby se zabránilo neurologickým komplikacím onemocnění. Pokud je přípravek PREFOLIC podáván jako pomalý odkapávací roztok, je třeba se vyvarovat dlouhodobé expozice kyslíku ve vzduchu a současnému podávání bikarbonátů.
U epileptických subjektů mohou antikonvulziva způsobit snížení folatemie; správa přípravku PREFOLIC, zatímco vyvažuje tento efekt, může zvýšit frekvenci přístupů.
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Prefolic
Pro intravenózní podání: stejně jako u jiných roztoků obsahujících vápník je současná léčba ceftriaxonem kontraindikována u novorozenců (ve věku <28 dní), a to i při použití oddělených infuzních linek (smrtelné riziko srážení vápenaté soli ceftriaxonu v proudu krve novorozence, viz bod „Nežádoucí účinky“).
U pacientů starších 28 dnů (včetně dospělých) by ceftriaxon neměl být podáván současně s intravenózními roztoky obsahujícími vápník včetně přípravku Prefolic stejnou infuzní linkou (např. Přes Y-konektor).
Pokud je pro sekvenční podávání použita stejná linie, měla by být linka mezi infuzemi propláchnuta kompatibilní kapalinou.
Varování Je důležité vědět, že:
Účinky na schopnost řídit a obsluhovat stroje
Nemá vliv na schopnost řídit a obsluhovat stroje.
Dávkování a způsob použití Jak používat Prefolic: Dávkování
Pokud se používá intravenózní podání, doporučuje se podávat pomalu.
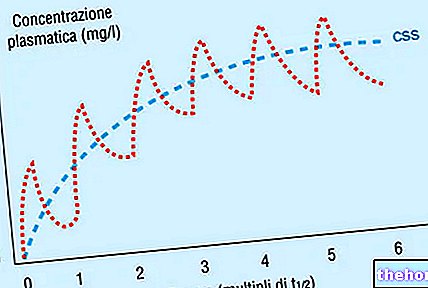
Po orálním podání přípravku PREFOLIC se dosáhne krevního maxima za 2–3 hodiny, které se pak v průběhu času pomalu rozpadá.
Průměrná dávka přípravku PREFOLIC pro orální i parenterální intramuskulární nebo intravenózní podání může být indikována v 15 mg denně nebo každý druhý den podle lékařského předpisu.
Léčba přípravkem PREFOLIC musí být prodloužena až do úplného ústupu symptomů nedostatku folikulu a rekonstituce endogenního dědictví. Ve výjimečných případech nebo při použití přípravku PREFOLIC pro antidotismus antifolických cytotoxických léků (například v případě podávání vysokých dávek methotrexátu) může dávkování zahrnovat použití vyšších dávek podávaných v intervalech několika hodin: 15 mg orálně každých 6-8 hodin nebo 50-100 mg intravenózně každých 3-8 hodin po dobu několika dnů podle parametrů „záchrany“.
Tablety jsou gastrorezistentní, tj. Uvolňují účinnou látku v proximálním střevě; nemají se žvýkat, ale musí se polykat celé, nejlépe ráno.
Vápenaté soli mohou tvořit komplexy s mnoha léčivy a to může vést k tvorbě sraženin. S ceftriaxonem byla hlášena fyzická nesnášenlivost (viz body „Kontraindikace“, „Interakce“ a „Nežádoucí účinky“).
Předávkování Co dělat, když jste užil příliš mnoho přípravku Prefolic
Klinické případy předávkování nejsou dosud známy.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Prefolic
Při použití přípravku jsou možné projevy přecitlivělosti (horečka, kopřivka, arteriální hypotenze, tachykardie, bronchospasmus, anafylaktický šok). Některé smrtelné případy u předčasně narozených a donošených kojenců (ve věku <28 dnů), kteří byli léčeni intravenózní ceftriaxon a vápník. Přítomnost srážení ceftriaxon-vápenaté soli byla detekována posmrtně v plicích a ledvinách. Vysoké riziko srážení u novorozenců je důsledkem jejich malého objemu krve a delšího poločasu ceftriaxonu ve srovnání s dospělými ( viz části „Kontraindikace“ a „Interakce“).
Byly hlášeny případy srážení ledvin, zejména u dětí starších 3 let léčených vysokými denními dávkami (např. ≥ 80 mg / kg / den) nebo celkovými dávkami vyššími než 10 gramů, kteří měli jiné rizikové faktory (např. Omezení tekutin , upoutaní na lůžko). U imobilizovaných nebo dehydratovaných pacientů se zvyšuje riziko tvorby sraženin. Tato událost může být symptomatická nebo asymptomatická, může způsobit selhání ledvin a anurii a je reverzibilní po přerušení podávání.
Srážení vápenato-ceftriaxonové soli ve žlučníku bylo pozorováno hlavně u pacientů léčených dávkami nad doporučenou standardní dávkou. U dětí prospektivní studie prokázaly variabilní výskyt srážek při intravenózním podání; v některých studiích byl výskyt vyšší než 30%. Zdá se, že tento výskyt je nižší u pomalých infuzí (20-30 minut). Tento účinek je obecně asymptomatický, ale ve vzácných případech jsou srážky doprovázeny klinickými příznaky, jako je bolest, nevolnost a zvracení. V těchto případech se doporučuje symptomatická léčba. Srážení je obecně reverzibilní po přerušení podávání.
Pokud se objeví jiné než výše popsané nežádoucí účinky, je vhodné je ohlásit lékaři.
Expirace a retence
Viz datum spotřeby uvedené na obalu.
Uvedené datum použitelnosti se vztahuje na produkt v neporušeném obalu, správně skladovaný.
Upozornění: přípravek nepoužívejte po uplynutí doby použitelnosti uvedené na obalu.
Chraňte před světlem a tablety uchovávejte při teplotě do 30 ° C.
KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
15mg enterosolventní tableta obsahuje: N5-methyltetrahydrofolát pentahydrát vápenatý 19,18 mg, což odpovídá 15 mg kyseliny. Pomocné látky: kukuřičný škrob, laktóza, stearan hořečnatý, polyethylenglykol 6000, polymetakryláty, polysorbát 80, simethikon, hydroxid sodný, mastek.
Jedna injekční lahvička s 15 mg prášku obsahuje: N5-methyltetrahydrofolát pentahydrát vápníku 19,18 mg, což odpovídá 15 mg kyseliny. Pomocné látky: kyselina citronová, glutathion, mannit, methyl p-hydroxybenzoát, hydroxid sodný.
Jedna ampulka rozpouštědla obsahuje: vodu na injekci.
Jedna injekční lahvička s práškem 50 mg obsahuje: N5-methyltetrahydrofolát pentahydrát vápníku 63,93 mg, což odpovídá 50 mg kyseliny. Pomocné látky: kyselina citronová, glutathion, mannit, methyl p-hydroxybenzoát, hydroxid sodný.
Jedna ampulka rozpouštědla obsahuje: vodu na injekci.
LÉKOVÁ FORMA
30 enterosolventních tablet po 15 mg
5 lahviček s 15 mg prášku + 5 lahviček se 3 ml rozpouštědla
6 lahviček s 50 mg prášku + 6 lahviček se 3 ml rozpouštědla
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Chcete-li mít přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
PREFOLICKÉ
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
• PREFOLIC 15 tablet
Jedna gastrorezistentní tableta obsahuje:
Aktivní princip:
Pentahydrát vápníku N5-methyltetrahydrofolát 19,18 mg odpovídá 15 mg kyseliny.
• PREFOLIC 15 mg / 3 ml prášek a rozpouštědlo pro injekční roztok
Jedna lahvička prášku obsahuje:
Aktivní princip:
Pentahydrát vápníku N5-methyltetrahydrofolát 19,18 mg odpovídá 15 mg kyseliny.
• PREFOLIC 50 mg / 3 ml prášek a rozpouštědlo pro injekční roztok
Jedna lahvička prášku obsahuje:
Aktivní princip:
Pentahydrát vápníku N5-methyltetrahydrofolát 63,93 mg odpovídá kyselině 50 mg.
03.0 LÉKOVÁ FORMA
Enterosolventní tablety.
Lahvičky s práškem + lahvičky s rozpouštědlem.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
U všech forem nedostatku folátu v důsledku zvýšené poptávky, snížené absorpce, nedostatečného dietního příjmu.
V antidotické terapii nadměrných dávek antagonistů kyseliny listové a v boji proti vedlejším účinkům vyvolaným aminopterinem a methotrexátem.
04.2 Dávkování a způsob podání
Po orálním podání přípravku PREFOLIC se dosáhne krevního maxima za 2–3 hodiny, které se pak v průběhu času pomalu rozpadá.
Průměrné dávkování přípravku PREFOLIC orálním i parenterálním intramuskulárním nebo intravenózním podáním lze indikovat v 15 mg denně nebo každý druhý den podle lékařského předpisu.
Léčba přípravkem PREFOLIC musí být prodloužena až do úplného ústupu symptomů nedostatku folikulu a rekonstituce endogenního dědictví. Ve výjimečných případech nebo při použití přípravku PREFOLIC pro antidotismus antifolických cytotoxických léků (například v případě podávání vysokých dávek methotrexátu) může dávkování zahrnovat použití vyšších dávek podávaných v intervalech několika hodin: 15 mg orálně každých 6-8 hodin nebo 50-100 mg intravenózně každých 3-8 hodin po dobu několika dnů podle parametrů „záchrany“.
04.3 Kontraindikace
Známá přecitlivělost na složky.
Pro intravenózní podání: souběžná léčba ceftriaxonem u novorozenců (ve věku ≤ 28 dní), a to i při použití oddělených infuzních linek. Viz body 4.5, 4.8 a 6.2.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Pokud se používá intravenózní podání, doporučuje se podávat injekci pomalu. U epileptických subjektů mohou antikonvulziva způsobit snížení folatemie; podávání přípravku PREFOLIC, zatímco vyvažuje tento účinek, může zvýšit frekvenci přístupů.
Tablety jsou gastrorezistentní, tj. Uvolňují účinnou látku v proximálním střevě; nemají se žvýkat, ale musí se polykat celé, nejlépe ráno.
V přítomnosti perniciózní anémie je dobrou praxí spojit vitamín B12 s přípravkem PREFOLIC, aby se zabránilo neurologickým komplikacím onemocnění.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Pro intravenózní podání: Stejně jako u jiných roztoků obsahujících vápník je souběžná léčba ceftriaxonem kontraindikována u novorozenců (ve věku ≤ 28 dní), a to i při použití oddělených infuzních linek (smrtelné riziko srážení soli ceftriaxonu). Vápník v krevním oběhu novorozence (viz bod 4.8).
U pacientů starších 28 dnů (včetně dospělých) by ceftriaxon neměl být podáván současně s intravenózními roztoky obsahujícími vápník včetně přípravku Prefolic stejnou infuzní linkou (např. Přes Y konektor).
Pokud je pro sekvenční podávání použita stejná linie, měla by být linka mezi infuzemi propláchnuta kompatibilní kapalinou.
04.6 Těhotenství a kojení
Jedná se o vitamínovou sloučeninu, normální složku našeho organismu, která nemá žádný vliv na matku a plod.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Nemá vliv na schopnost řídit a obsluhovat stroje.
04.8 Nežádoucí účinky
Při použití přípravku jsou možné projevy přecitlivělosti (horečka, kopřivka, arteriální hypotenze, tachykardie, bronchospasmus, anafylaktický šok).
Srážení vápenato-ceftriaxonové soli (pro intravenózní podání)
Vážné a v některých případech smrtelné nežádoucí účinky byly vzácně hlášeny u předčasně narozených a donošených dětí (nitrožilně stárnutých. Přítomnost srážení vápenato-ceftriaxonové soli byla zjištěna posmrtně v plicích a ledvinách. L "Vysoké riziko srážení u novorozenců je důsledkem jejich malého objemu krve a delšího poločasu ceftriaxonu ve srovnání s dospělými (viz body 4.3 a 4.5).
Byly hlášeny případy srážení ledvin, zejména u dětí starších 3 let léčených vysokými denními dávkami (např. ≥ 80 mg / kg / den) nebo celkovými dávkami vyššími než 10 gramů, kteří měli jiné rizikové faktory (např. Omezení tekutin , upoutaní na lůžko). U imobilizovaných nebo dehydratovaných pacientů se zvyšuje riziko tvorby sraženin. Tato událost může být symptomatická nebo asymptomatická, může způsobit selhání ledvin a anurii a je reverzibilní po přerušení podávání.
Srážení vápenato-ceftriaxonové soli ve žlučníku bylo pozorováno hlavně u pacientů léčených dávkami nad doporučenou standardní dávkou. U dětí prospektivní studie prokázaly variabilní výskyt srážek při intravenózním podání; v některých studiích byl výskyt vyšší než 30%. Zdá se, že tento výskyt je nižší u pomalých infuzí (20-30 minut). Tento účinek je obecně asymptomatický, ale ve vzácných případech jsou srážky doprovázeny klinickými příznaky, jako je bolest, nevolnost a zvracení. V těchto případech se doporučuje symptomatická léčba. Srážení je obecně reverzibilní po přerušení podávání.
04.9 Předávkování
Klinické případy předávkování nejsou dosud známy.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Calcium N5-methyltetrahydrofolate (5-MTHF), fyziologická molekula vitamínové povahy, je aktivní složkou, která zasahuje do živočišných organismů v řadě důležitých reakcí, z biochemicko-metabolického hlediska, zaměřených na přenos jednotka oxidu uhelnatého. Mezi těmito reakcemi je třeba pamatovat zejména na:
na. syntéza purinů a thymidylátu, základní krok pro biosyntézu nukleových kyselin;
b. ex novo syntéza labilních methylů vycházející ze serinu, glycinu, histidinu, mravenčanu;
C. syntéza methioninu vycházející z homocysteinu, reakce, která vyžaduje přítomnost vitaminu B12 jako kofaktoru, a proto představuje bod interakce mezi folátem a kobalaminem.
05.2 Farmakokinetické vlastnosti
5-MTHF je díky svým vlastnostem fyziologické molekuly používán organismem jako takovým, aniž by prošel dalšími biotransformačními procesy. Představuje fyziologickou formu transportu kyseliny listové v plazmě, kde představuje téměř všechny cirkulující foláty. Je snadno absorbován z trávicího traktu, a proto je distribuován do všech tkání včetně CNS; ve skutečnosti je zachycován chorioidními plexy v mozkomíšním moku, kde je jeho koncentrace rovna trojnásobku koncentrace krve.
T½ intravenózního 5-MTHF je přibližně 2 hodiny, orálně přibližně 2-3 hodiny. Je eliminován ledvinami a střevem.
05.3 Předklinické údaje vztahující se k bezpečnosti
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
• PREFOLIC 15 tablet
Kukuřičný škrob, laktóza, stearát hořečnatý, polyethylenglykol 6000, polymethakryláty, polysorbát 80, simethikon, hydroxid sodný, mastek.
• PREFOLIC 15 mg / 3 ml prášek a rozpouštědlo pro injekční roztok
Kyselina citronová, glutathion, mannit, methyl p-hydroxybenzoát, hydroxid sodný. Jedna ampulka rozpouštědla obsahuje: vodu na injekci.
• PREFOLIC 50 mg / 3 ml prášek a rozpouštědlo pro injekční roztok
Kyselina citronová, glutathion, mannit, methyl p-hydroxybenzoát, hydroxid sodný. Jedna ampulka rozpouštědla obsahuje: vodu na injekci.
06.2 Neslučitelnost
Neměl by být přidáván do roztoků obsahujících hydrogenuhličitan.
Vápenaté soli mohou tvořit komplexy s mnoha léčivy a to může vést k tvorbě sraženin. S ceftriaxonem byla hlášena fyzická inkompatibilita (viz body 4.3, 4.5 a 4.8).
06.3 Doba platnosti
• PREFOLIC 15 tablet: 36 měsíců
• PREFOLIC 15 mg / 3 ml a PREFOLIC 50 mg / 3 ml, prášek a rozpouštědlo pro injekční roztok: 30 měsíců
Rekonstituovaný přípravek je stabilní po dobu 10 hodin.
06.4 Zvláštní opatření pro skladování
Chraňte před světlem a tablety uchovávejte při teplotě do 30 ° C.
06.5 Charakter vnitřního obalu a obsah balení
- Karton obsahující 30 tablet po 15 mg v blistrech (polyetylen-hliník)
- Karton obsahující 5 hermeticky uzavřených lahviček z tmavého skla (gumová zátka a hliníkové kovové víčko) po 15 mg + 5 skleněných lahviček obsahujících 3 ml rozpouštědla
- Karton obsahující 6 lahviček z tmavého skla s hermetickým uzávěrem (gumová zátka a hliníkové kovové víčko) po 50 mg + 6 skleněných lahviček obsahujících 3 ml rozpouštědla
06.6 Návod k použití a zacházení
Jak otevřít lahvičku s rozpouštědlem:
- vyvíjejte tlak palcem přes barevný bod.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
ZAMBON ITALIA s.r.l. - Via Lillo del Duca, 10. 20091 Bresso (MI)
08.0 REGISTRAČNÍ ČÍSLO
- 30 tablet po 15 mg - A.I.C.: n. 024703124
- 5 lahviček s 15 mg prášku + 5 lahviček se 3 ml rozpouštědla - A.I.C.: n. 024703098
- 6 lahviček s 50 mg prášku + 6 lahviček se 3 ml rozpouštědla - A.I.C.: n. 024703112
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
- 30 tablet po 15 mg: 20.07.1989
- 5 lahviček s 15 mg prášku + 5 lahviček se 3 ml rozpouštědla: 30.04.1982
- 6 lahviček s 50 mg prášku + 6 lahviček se 3 ml rozpouštědla: 21.02.1985
Obnovení autorizace: 01.06.2010
10.0 DATUM REVIZE TEXTU
14. ledna 2015















----tiamfenicolo.jpg)