Co je Lucentis?
Lucentis je injekční roztok do oka. Obsahuje léčivou látku ranibizumab.
Na co se přípravek Lucentis používá?
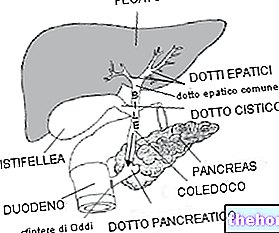
Lucentis je indikován k léčbě „mokré“ formy neovaskulární makulární degenerace související s věkem (AMD). Toto onemocnění postihuje centrální část sítnice (nazývanou „makula“), v nejniternější části „oka“, a způsobuje ztrátu „blízkého“ vidění. Makula poskytuje centrální vidění, nezbytné k rozlišení detailů a výkonu, proto , každodenní operace, jako je řízení, čtení a rozpoznávání tváří. „Mokrá“ forma AMD je způsobena tvorbou abnormálních cév pod makulou, které mohou krvácet nebo vytékat tekutina. Proto ztráta zraku. Výdej léku je vázán na lékařský předpis.
Jak se přípravek Lucentis používá?
Lucentis se podává jako jednorázová injekce do postiženého oka.První tři měsíce se injekce podává jednou za měsíc. Poté lékař kontroluje pacientovu vizi na měsíční bázi, pokud se stav zhorší, podá další injekci. Interval mezi dvěma dávkami by neměl být kratší než jeden měsíc. Lucentis musí být podáván kvalifikovaným oftalmologem (oftalmologem) se zkušenostmi s tímto typem injekce. Před každou injekcí dostane pacient lokální anestetikum ke snížení nebo prevenci bolesti; oko, oční víčko a kůže kolem oka jsou dezinfikovány. Kromě toho jsou předepsány antibiotické oční kapky k prevenci očních infekcí, které se užívají tři dny před injekcí a tři dny po ní. Pacient dostane potřebné pokyny, aby kapky nakapal sám.
Jak přípravek Lucentis působí?
Účinná látka přípravku Lucentis, ranibizumab, je malý fragment monoklonální protilátky. Monoklonální protilátka je protilátka (typ proteinu) navržená tak, aby rozpoznávala a připojovala se ke specifické struktuře, nazývané antigen, nacházející se v určitých buňkách těla.
Ranibizumab byl vytvořen k inhibici látky zvané vaskulární endoteliální růstový faktor A (VEGF-A). VEGF-A je přítomen ve vysokých koncentracích v očích pacientů s AMD a je zodpovědný za růst krevních cév a prosakování séra. Tyto účinky zhoršují onemocnění. Inhibicí tohoto faktoru ranibizumab snižuje růst krevních cév a únik nebo krvácení tekutin.
Jak byl přípravek Lucentis zkoumán?
Účinky přípravku Lucentis byly nejprve zkoumány na experimentálních modelech a poté na lidech.
Do tří hlavních studií přípravku Lucentis bylo zařazeno 1 323 pacientů s vlhkou formou AMD. Všem pacientům bylo více než 50 let a nikdy předtím nepodstoupili léčbu AMD. Byly studovány dvě dávky přípravku Lucentis: 0,3 mg a 0,5 mg. Studie měly trvat dva roky, ale pouze jeden skončil při hodnocení léku.
Ve dvou ze tří studií byl přípravek Lucentis srovnáván s falešnou injekcí, což je postup podobný injekci přípravku Lucentis, ale bez podávání léčiva a prováděný bez jehly.
je přitlačen na povrch oka, aniž by injekci skutečně provedl. Pacienti nejsou schopni určit, zda oční lékař podal Lucentis nebo použil fingovaný postup, který byl neúčinný. Třetí studie porovnávala přípravek Lucentis s fotodynamickou terapií verteporfinem (PDT, jiný typ léčby AMD).) Hlavním měřítkem účinnosti bylo zlepšení vidění v nemocném oku jeden rok po zahájení léčby, měřeno na základě standardního testu vidění se vzdálenou světelnou tabulí. Pokud počet písmen přečtených na tabuli vzrostl, zůstal tak, jak je, nebo se snížil o více než 15 písmen, nedošlo k žádnému výraznému zhoršení vidění.
Jaký přínos přípravku Lucentis byl prokázán v průběhu studií?
Lucentis byl v prevenci zhoršení zraku účinnější než kontrolní léky. Procento mezi 94% a 96% pacientů podstupujících měsíčně
léčba přípravkem Lucentis neodhalila zhoršení vidění ve srovnání se 62% pacientů léčených simulovanými injekcemi a 64% pacientů léčených PDT verteporfinem. Dávka 0,5 mg byla účinnější než dávka 0,3 mg. Vidění pacientů léčených přípravkem Lucentis také zůstalo lepší než vidění subjektů léčených falešnými injekcemi ve studii, kde byly injekce podávány méně často (jeden za měsíc po dobu prvních tří měsíců, poté jeden každé tři měsíce).
Jaká rizika jsou spojena s přípravkem Lucentis?
Nejčastějšími nežádoucími účinky pozorovanými u přípravku Lucentis (pozorovanými u více než 1 z 10 pacientů) jsou zvýšený nitrooční tlak (uvnitř oka), bolest hlavy, vitritida (zánět oka), odloučení sklivce (odtržení od oka) želé sítnice, která vyplňuje vnitřek oka), retinální krvácení (krvácení ze sítnice), poruchy zraku, bolest očí, plováky (létající mušky), krvácení do spojivky (krvácení z cév v přední části oka), podráždění oka, pocit cizího tělo v oku, zvýšené slzení, blephartitida (zánět očních víček), suché oči, oční hyperémie (červené oči), svědivé oči, artralgie (bolest kloubů) a nazofaryngitida (zánět nosu a hrdla) Pro celý seznam vedlejších účinků hlášených u přípravku Lucentis, viz příbalová informace.
Zřídka se po léčbě Lucentisem může objevit endoftalmitida („infekce zeměkoule), závažný zánět oka, poranění sítnice a šedý zákal (zákal čočky). V takovém případě je nutné zasáhnout co nejdříve. Pokyny k lékařskému postupu být zahájena u postižených pacientů jsou podávány v příbalové informaci Injekce do oka může také způsobit dočasné zvýšení očního tlaku. Oční lékař zkontroluje oční tlak po injekci a v případě potřeby provede nápravná opatření. Lucentis by neměly užívat osoby s přecitlivělostí (alergií) na ranibizumab nebo na kteroukoli jinou složku přípravku. Tento lék by také neměli používat pacienti, kteří mohou mít „infekci oka nebo okolí“ nebo těžký nitrooční zánět (uvnitř „oka“).
Na základě čeho byl přípravek Lucentis schválen?
Výbor pro humánní léčivé přípravky (CHMP) poznamenal, že přípravek Lucentis má vedlejší účinky, které jsou však kompenzovány přesvědčivě prokázanými přínosy léčiva, které trvaly až dva roky používání. Výbor rozhodl, že přínosy přípravku Lucentis při léčbě neovaskulární (vlhké) věkem podmíněné makulární degenerace převyšují její rizika. Vzhledem k tomu, že účinnost přípravku Lucentis byla o něco vyšší u pacientů, kteří dostávali dávku 0,5 mg, a nejběžnější vedlejší účinky nebyly závažné, výbor doporučil, aby registrace byla udělena v této síle.
Jaká opatření jsou přijímána k zajištění bezpečného používání přípravku Lucentis?
Společnost, která vyrábí přípravek Lucentis, poskytne lékařům informační balíčky (včetně informací o nezbytných krocích, které je třeba učinit, aby se minimalizovalo riziko infekce spojené s očními injekcemi) a pro pacienty (pomoci připravit se na léčbu přípravkem Lucentis, rozpoznat závažné nežádoucí účinky a vědět, kdy požádat o naléhavou návštěvu lékaře.) Společnost bude také pečlivě sledovat vedlejší účinky a bezpečnost léku.
Více informací o Lucentis
Dne 22. ledna 2007 udělila Evropská komise společnosti Novartis Europharm Limited „Marketing Authorisation“ Evropské unie pro Lucentis. Úplnou verzi hodnocení Lucentis Evaluation (EPAR) získáte kliknutím sem.
Poslední aktualizace tohoto souhrnu: 11-2008.
Informace o Lucentisranibizumabu zveřejněné na této stránce mohou být zastaralé nebo neúplné. Správné použití těchto informací najdete na stránce Prohlášení a užitečné informace.